Clear Sky Science · he
המוטציית המיסנס הקלינית E282K ב-PPP3CA/קלצינאורין משנה הדה-פוספורילציה של תת-מטרות על ידי שינוי גיוס לאתר הפעיל
כאשר שינוי זעיר באנזים מוחי גורם לבעיות גדולות
תאי המוח שלנו מדליקים וכבים איתותים ברצף על־ידי הוספה והסרה של תגיות כימיות זעירות שנקראות פוספטים. אנזים מרכזי בשם קלצינאורין אחראי על הסרת רבות מהתגיות האלה, ומוטציות תורשתיות או חדשות בגן שלו, PPP3CA, קשורות להפרעה בילדות קשה הכוללת אפילפסיה ועיכוב התפתחותי. המחקר שואל שאלה פשוטה אך חשובה: איך שינוי של יחידת בניין אחת בלבד בקלצינאורין עלול להפריע כל כך אף להתפתחות המוח?
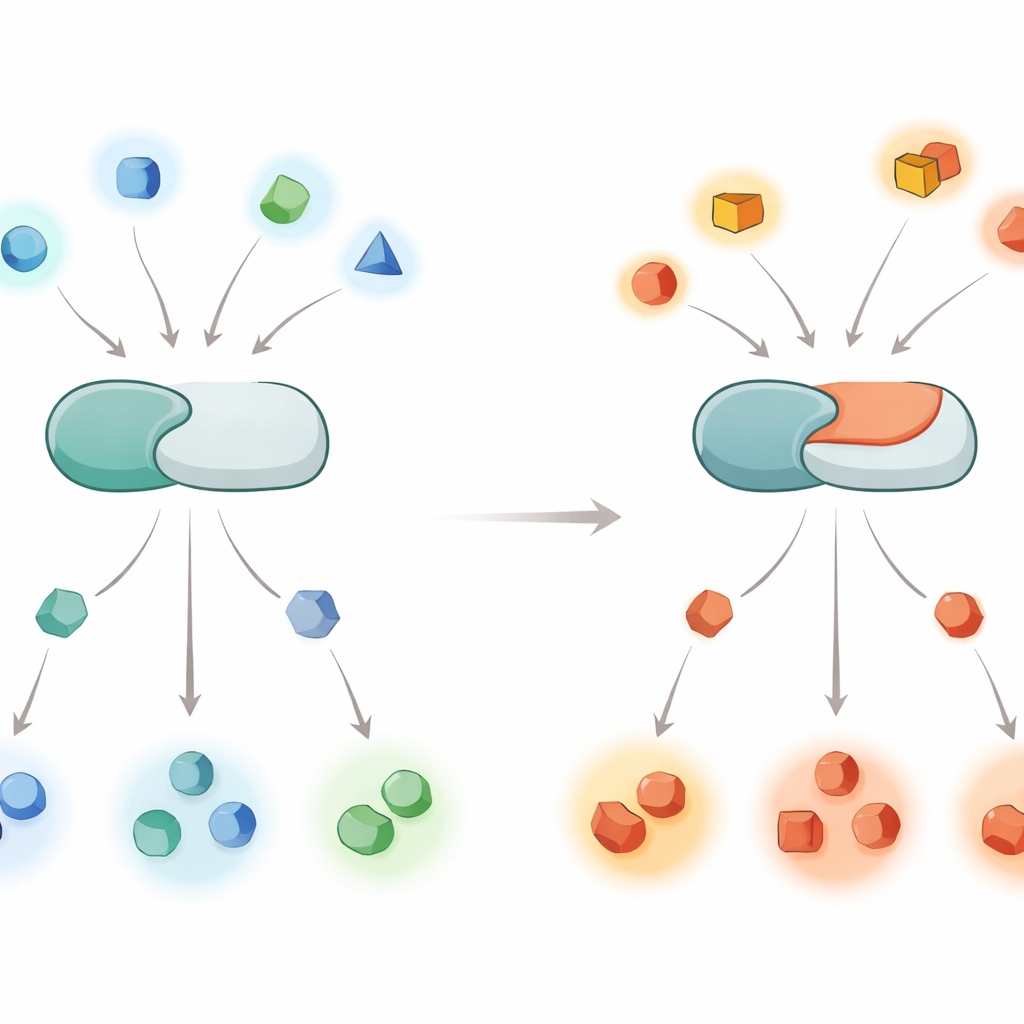
איך תאים משתמשים במפסקים כימיים
חלבונים בתוך תאים פועלים כמו עובדים בקו ייצור, ותוויות הפוספט הן מפסקים שמדליקים וכבים אותם. קינאזות מצמידות קבוצות פוספט, בעוד פוספטאזות מסירות אותן. קלצינאורין היא פוספטאזת תגובה לסיגנלי סידן והיא פעילה במיוחד במוח, שם היא מסייעת בוויסות התפתחות, למידה וזיכרון. מאחר שקלצינאורין נוגעת במאות עד אלפי מטרות חלבוניות שונות, גם טעויות קטנות בהעדפת המטרות עלולות להתפשט דרך מסלולי איתות רבים ולתרום להפרעות כמו אלצהיימר, פרקינסון ולמצב ההתפתחותי הנדיר הידוע כ-DEE91 הקשור ל-PPP3CA.
כיס גיוס חבוי בסמוך לאתר הפעיל
החוקרים התמקדו באופן שבו קלצינאורין מזהה את המקומות הספציפיים על חלבוני היעד שלו. הם גילו "כיס גיוס" שלא זוהה קודם ממש ליד אתר הפעולה של האנזים. חלבונים רבים שמותאמים תחילה על־ידי קינאזות מסוימות נושאים חומצה אמינית חיובית, ארגינין, מיד לפני תג הפוספט. באמצעות ביולוגיה מבנית, מדידות קשירה וניסויים מבחנה, הצוות הראה כי הארגינין מתמקם בתוך כיס בעל מטען שלילי שנבנה סביב שריד קלצינאורין שנקרא E282, ועוזר למשוך את האתר המסומן למקומו כדי שהאנזים יוכל להסיר את הפוספט ביעילות.
מה המוטציה E282K עושה בפועל
ב ילדים עם DEE91 הקשור ל-PPP3CA, השינוי השכיח ביותר בקלצינאורין מחליף את E282 בחומצה אמינית אחרת, ליזין, ויוצר את הווריאנט E282K. באופן מפתיע, מבני גביש הראו כי הצורה הכללית של האנזים נותרת כמעט ללא שינוי ואתרי הגיוס האחרים עדיין פועלים. ההבדל הקריטי טמון בכימיה המקומית: הכיס שהיה חומצי ופתוח סביב E282 הופך לבסיסי יותר ולחסום חלקית על־ידי גשר מלח פנימי חדש. כתוצאה מכך, פפטידים שתלוים בארגינין שמתקבע בכיס זה נקשרים כעת בצורה חלשה ומופחתת ההדפוספורילציה שלהם משמעותית.
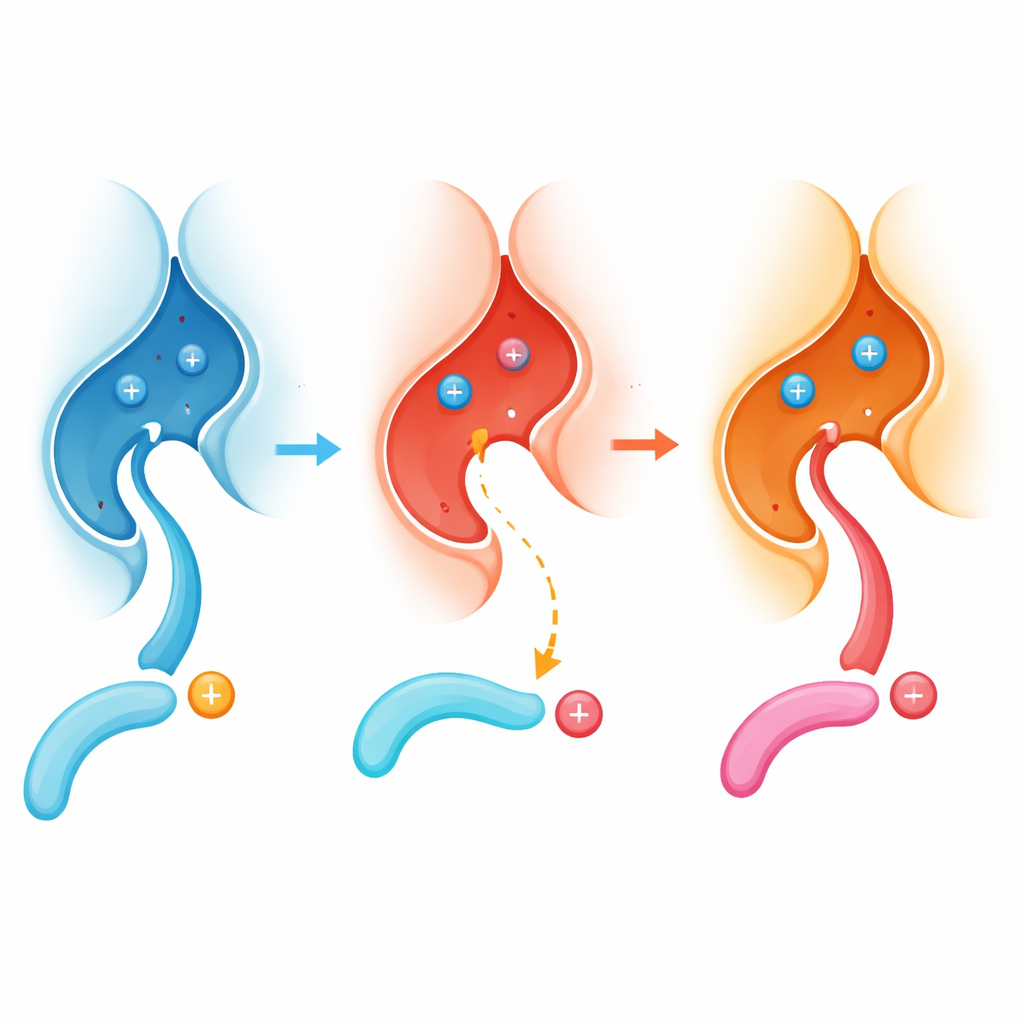
שינוי גלובלי במי שמכבים את האותות
כדי להעריך עד כמה השפעה זו מגיעה, המחברים בדקו אלפי פפטידים מזורחנים שמקורם בתאים אנושיים והשוו כיצד קלצינאורין תקין ומוטנטי פעלו עליהם לאורך זמן. קלצינאורין תקין העדיף בחוזקה אתרים עם שרידי חומצות אמיניות טעונות חיובית (כמו ארגינין או ליזין) בדיוק לפני הפוספט. לעומת זאת, גרסת E282K איבדה רבות מההעדפה הזו ובמקום זאת עיבדה ביתר קלות אתרים עם שרידי חומצות טעונות שלילית באותו מיקום. דפוסים דומים הופיעו כאשר הצוות הביע את שתי צורות האנזים בשורות תאים חיים, כולל שורה דמוית-נוירון, והשתמשו בספקטרומטריית מסה כדי לרשום אילו אתרי חלבון הודפוספורילו יותר או פחות. המוטציה למעשה מכווננת מחדש את טעמי האנזים — מהעדפת אתרי "בסיסיים" לעדפת אתרים "חומציים".
מדוע זה חשוב לילדים עם DEE91
המחקר מראה שהמוטציה E282K אינה פוגעת בקלצינאורין בכך שהיא פשוט מחלישה או מכבה אותו. במקום זאת, היא משנה אילו מפסקים חלבוניים האנזים מסוגל להפעיל, ומשבשת רשתות איתות ברחבי התא. בתאי מוח גדלים ומתפתחים, הטיית אותות רחבה זו — הרחק ממטרות עשירות בארגינין ואל מול אתרים אחרים — ככל הנראה מערערת את התכניות הדקיקות שמווסתות גדילה נוירונית, קישוריות ופעילות חשמלית. בזיהוי כיס הגיוס הספציפי הזה ובתיאור האופן שבו E282K משנה את המטען והנגישות שלו, המחקר מספק בסיס מולקולרי להבנת המחלה ומציע דרכים חדשות לחיפוש טיפולים שעשויים לשחזר בחירה נכונה של תת-מטרות, גם אם המוטציה עצמה לא ניתנת להפיכה.
ציטוט: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
מילות מפתח: קלצינאורין, מוטציה ב-PPP3CA, פוספורילציה של חלבונים, הפרעות בהתפתחות נוירולוגית, ספציפיות של אנזים