Clear Sky Science · sv
Den kliniska missense-varianten E282K i PPP3CA/calcineurin förskjuter substrat-defosforylering genom att ändra rekrytering till det aktiva sätet
När en liten förändring i ett hjärnenzym orsakar stora problem
Våra hjärnceller slår hela tiden signaler av och på genom att sätta dit och ta bort små kemiska markörer som kallas fosfater. Ett nyckelenzym som kallas calcineurin ansvarar för att ta bort många av dessa markörer, och ärvda eller nya mutationer i dess gen, PPP3CA, har kopplats till en allvarlig barndomssjukdom med epilepsi och utvecklingsförsening. Denna studie ställer en enkel men viktig fråga: hur kan utbyte av bara en byggsten i calcineurin så dramatiskt rubba hjärnans utveckling?
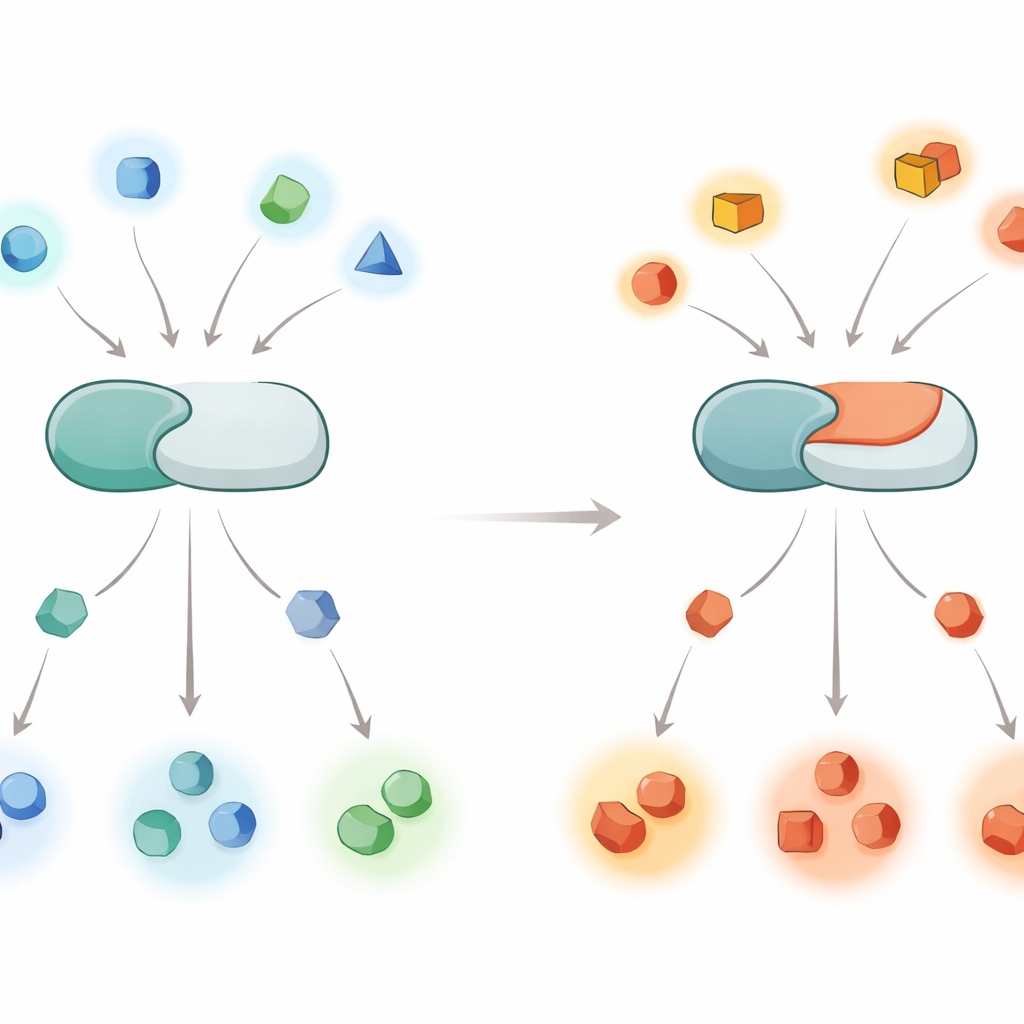
Hur celler använder kemiska strömbrytare
Proteiner i cellerna fungerar som arbetare på ett löpande band, och fosfatmarkörer är av/på-strömbrytarna som styr dem. Kinaser fäster fosfatgrupper medan fosfataser tar bort dem. Calcineurin är en fosfatas som svarar på kalciumsignaler och är särskilt aktiv i hjärnan, där den hjälper till att reglera utveckling, inlärning och minne. Eftersom calcineurin påverkar hundratals till tusentals olika proteintargets kan även små fel i vilka proteiner den agerar på få följdverkningar i många signalsystem och bidra till sjukdomar som Alzheimers, Parkinsons och det sällsynta utvecklingssyndromet känt som PPP3CA-relaterad DEE91.
En dold dockningsficka nära arbetsstället
Forskarna fokuserade på hur calcineurin känner igen specifika platser på sina proteintargets. De upptäckte en tidigare oigenkänd ”rekryteringsficka” precis intill enzymets aktiva yta. Många target-proteiner som först modifieras av vissa kinaser bär en positivt laddad aminosyra, arginin, omedelbart före fosfatmärket. Genom strukturbiofysik, bindningsmätningar och reaktioner i provrör visade teamet att denna arginin sluter sig till en negativt laddad ficka byggd runt ett calcineurinrest, E282, och hjälper till att dra den märkta platsen på plats så att enzymet effektivt kan ta bort fosfatet.
Vad E282K-mutation verkligen gör
Hos barn med PPP3CA-relaterad DEE91 är den vanligaste förändringen i calcineurin ett byte av E282 mot en annan aminosyra, lysin, vilket skapar varianten E282K. Förvånande nog visade kristallstrukturer att enzymets övergripande form förblir nästan oförändrad och dess andra dockningsställen fortfarande fungerar. Den avgörande skillnaden ligger i den lokala kemin: den tidigare sura, öppna fickan runt E282 blir mer basisk och delvis blockerad av en ny intern saltbrygga. Som ett resultat binder peptider som förlitar sig på att en arginin passar in i denna ficka nu dåligt och defosforyleras mycket mindre effektivt.
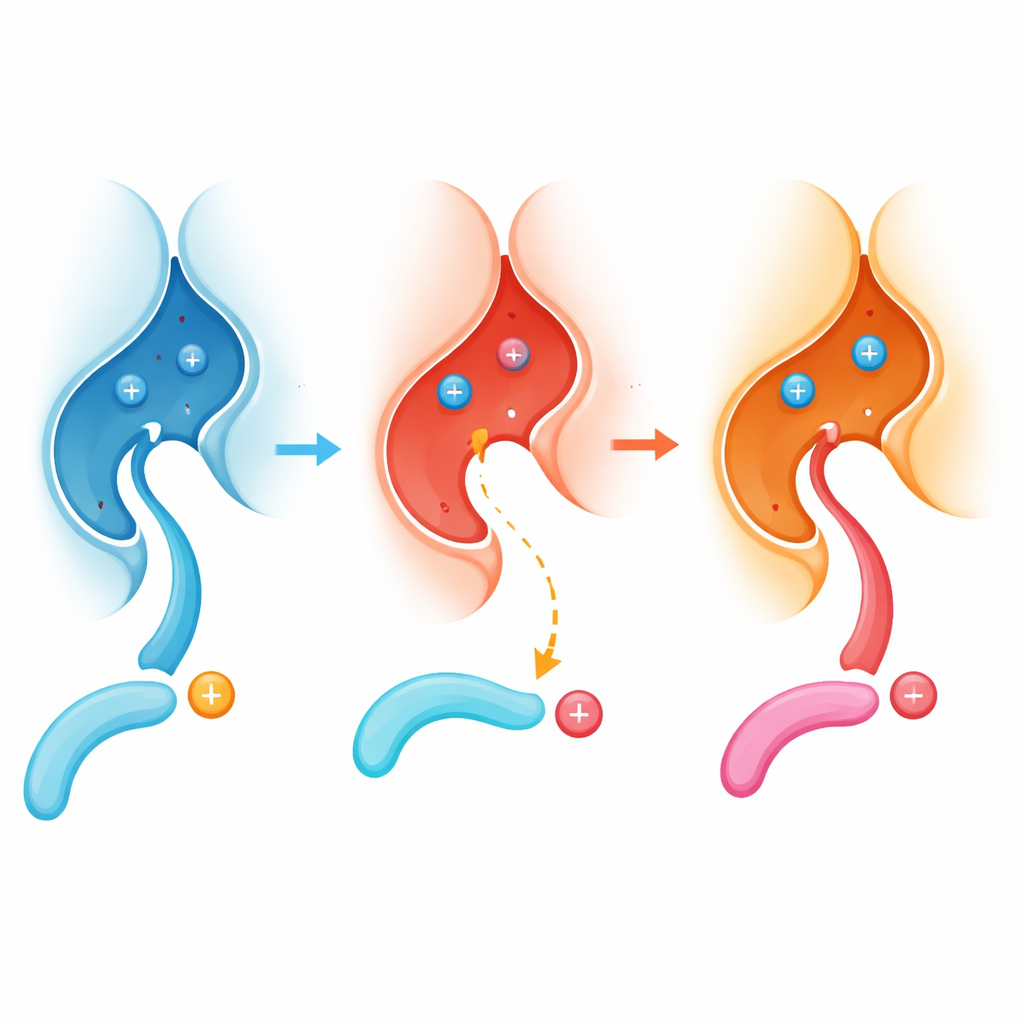
En global förskjutning i vilka som stängs av
För att se hur långt denna effekt sträcker sig undersökte författarna tusentals fosfopeptider härledda från mänskliga celler och jämförde hur normal respektive mutant calcineurin agerade på dem över tid. Normal calcineurin föredrog starkt platser med positivt laddade rester (såsom arginin eller lysin) direkt före fosfatet. I kontrast hade E282K-versionen förlorat mycket av denna preferens och bearbetade istället lättare platser med negativt laddade rester i den positionen. Liknande mönster framkom när teamet uttryckte de två enzymformerna i levande cellinjer, inklusive en neuronlik cellinje, och använde masspektrometri för att katalogisera vilka proteinställen som var mer eller mindre defosforylerade. Mutationen ställer effektivt om enzymet från att föredra ”basiska” platser till att gynna ”sura”.
Varför detta spelar roll för barn med DEE91
Arbetet visar att E282K-mutation inte helt enkelt försvagar calcineurin eller stänger av det. Istället omskriver den vilka proteinknappar enzymet kan trycka på, vilket förskjuter signalsystemen i hela cellen. I växande och utvecklande hjärnceller stör denna breda felriktning av signaler—bort från deras normala argininrika mål och mot andra platser—sannolikt de fint balanserade program som styr neuronernas tillväxt, kopplingar och elektriska aktivitet. Genom att peka ut just denna rekryteringsficka och hur E282K ändrar dess laddning och åtkomst lägger studien en molekylär grund för att förstå sjukdomen och föreslår nya sätt att söka efter terapier som kan återställa korrekt substratval, även om mutationen i sig inte kan ångras.
Citering: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Nyckelord: calcineurin, PPP3CA-mutation, proteinfosforylering, neurodevelopmentala störningar, enzym-specifikhet