Clear Sky Science · it
La variante missenso clinica E282K in PPP3CA/calcineurin altera la defosforilazione dei substrati modificando il reclutamento nel sito attivo
Quando una Piccola Modifica in un Enzima Cerebrale Provoca Grandi Problemi
Le cellule cerebrali regolano continuamente i segnali accendendo e spegnendo piccole etichette chimiche chiamate gruppi fosfato. Un enzima chiave, la calcineurina, è responsabile della rimozione di molti di questi gruppi e mutazioni ereditate o de novo nel suo gene, PPP3CA, sono state collegate a un grave disturbo infantile caratterizzato da epilessia e ritardo dello sviluppo. Questo studio pone una domanda semplice ma cruciale: come può la sostituzione di un solo mattoncino nella calcineurina perturbare così profondamente lo sviluppo cerebrale?
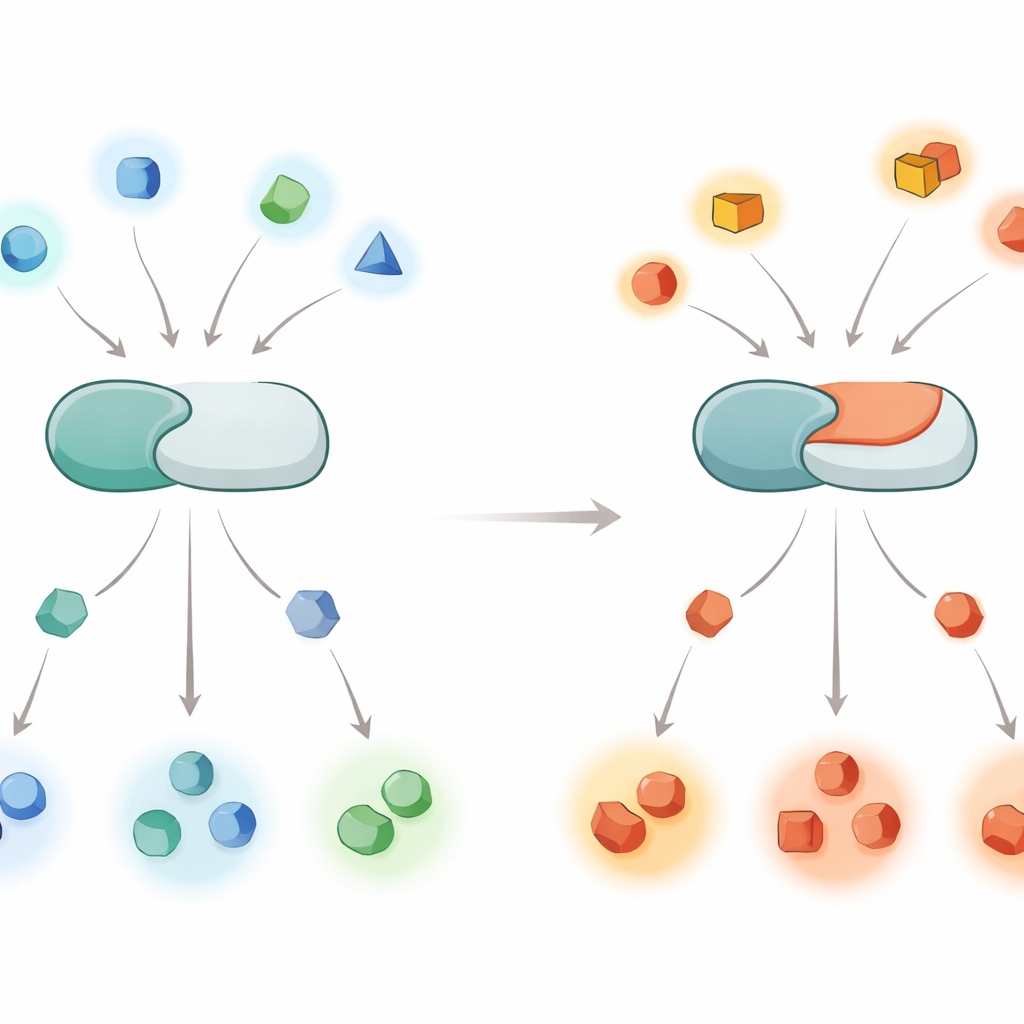
Come le Cellule Usano Interruttori Chimici
Le proteine all’interno delle cellule funzionano come operai su una catena di montaggio, e i gruppi fosfato sono gli interruttori on/off che le controllano. Le chinasi aggiungono gruppi fosfato, mentre le fosfatasi li rimuovono. La calcineurina è una fosfatasi che risponde ai segnali di calcio ed è particolarmente attiva nel cervello, dove contribuisce allo sviluppo, all’apprendimento e alla memoria. Poiché la calcineurina agisce su centinaia o migliaia di proteine bersaglio diverse, anche piccoli errori nella selezione dei bersagli possono propagarsi attraverso molte vie di segnalazione, contribuendo a malattie come Alzheimer, Parkinson e alla rara condizione dello sviluppo nota come DEE91 correlata a PPP3CA.
Una Tasca di Reclutamento Nascosta Vicino al Sito Attivo
I ricercatori si sono concentrati su come la calcineurina riconosce siti specifici sulle sue proteine bersaglio. Hanno scoperto una tasca di “reclutamento” finora non riconosciuta proprio accanto al sito attivo dell’enzima. Molte proteine bersaglio che vengono inizialmente modificate da determinate chinasi portano un amminoacido carico positivamente, l’arginina, immediatamente prima del gruppo fosfato. Attraverso biologia strutturale, misure di legame e reazioni in provetta, il gruppo ha dimostrato che questa arginina si inserisce in una tasca carica negativamente costruita intorno a una residuo della calcineurina chiamato E282, contribuendo a tirare il sito fosforilato nella posizione corretta affinché l’enzima possa rimuovere efficacemente il fosfato.
Cosa Fa Davvero la Mutazione E282K
Nei bambini con DEE91 correlata a PPP3CA, la modifica più comune nella calcineurina sostituisce E282 con un diverso amminoacido, la lisina, creando la variante E282K. Con sorpresa, le strutture cristalline hanno rivelato che la forma complessiva dell’enzima rimane quasi invariata e i suoi altri siti di ancoraggio funzionano ancora. La differenza cruciale risiede nella chimica locale: la tasca attorno a E282, una volta acida e aperta, diventa più basica e parzialmente ostruita da un nuovo ponte salino interno. Di conseguenza, i peptidi che dipendono dall’inserimento di un’arginina in quella tasca si legano male e vengono defosforilati con molta meno efficienza.
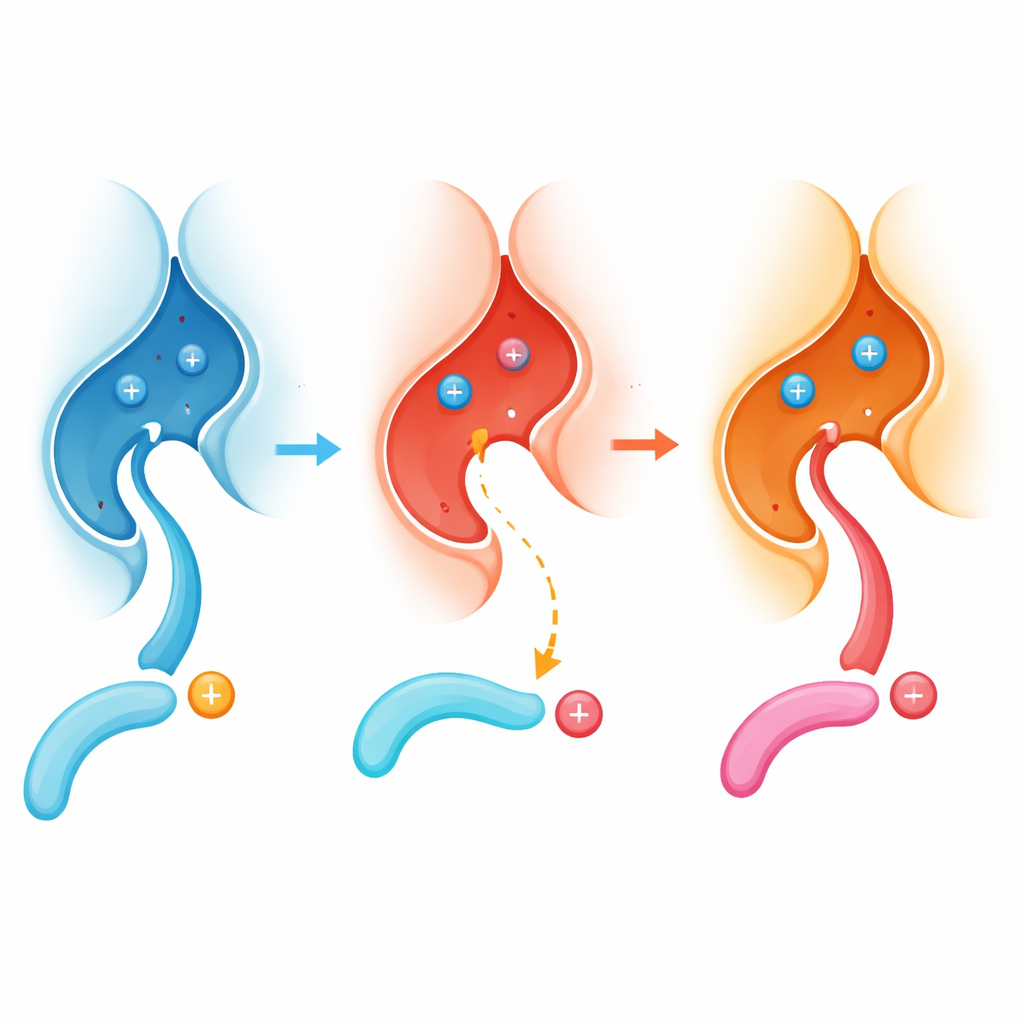
Un Cambiamento Globale di Chi Viene Spento
Per valutare l’estensione di questo effetto, gli autori hanno esaminato migliaia di fosfopeptidi derivati da cellule umane e hanno confrontato come la calcineurina normale e la mutata agivano su di essi nel tempo. La calcineurina normale preferiva nettamente siti con residui carichi positivamente (come arginina o lisina) immediatamente prima del fosfato. Al contrario, la versione E282K ha perso gran parte di questa preferenza e ha invece processato più agevolmente siti con residui carichi negativamente in quella posizione. Schemi simili sono apparsi quando il team ha espresso le due forme enzimatiche in linee cellulari viventi, inclusa una linea neuronale, e ha usato la spettrometria di massa per catalogare quali siti proteici erano più o meno defosforilati. La mutazione ricalibra di fatto l’enzima, che passa dal preferire siti ‘basici’ al favorire quelli ‘acidi’.
Perché Questo è Importante per i Bambini con DEE91
Il lavoro dimostra che la mutazione E282K non si limita a indebolire la calcineurina o a spegnerla. Piuttosto, riorienta quali interruttori proteici l’enzima può attivare o disattivare, modificando le reti di segnalazione in tutta la cellula. Nelle cellule cerebrali in crescita e in sviluppo, questo ampio scostamento dei segnali — lontano dai loro normali bersagli ricchi di arginina e verso siti differenti — probabilmente altera i programmi finemente bilanciati che controllano la crescita neuronale, la connettività e l’attività elettrica. Identificando con precisione questa tasca di reclutamento e come E282K ne altera la carica e l’accessibilità, lo studio pone le basi molecolari per comprendere la malattia e suggerisce nuovi approcci per cercare terapie in grado di ripristinare la corretta selezione dei substrati, anche se la mutazione stessa non può essere invertita.
Citazione: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Parole chiave: calcineurina, mutazione PPP3CA, fosforilazione proteica, disturbi dello sviluppo neurologico