Clear Sky Science · nl
De klinische missense‑variant E282K in PPP3CA/calcineurin verschuift substraat‑defosforylering door wijziging van de rekrutering in het actieve centrum
Wanneer een Kleine Wijziging in een Hersenenzym Grote Problemen Veroorzaakt
Onze hersencellen schakelen voortdurend signalen aan en uit door kleine chemische labels, fosfaatgroepen, toe te voegen en te verwijderen. Een belangrijk enzym, calcineurine, is verantwoordelijk voor het verwijderen van veel van deze labels, en erfelijke of nieuwe mutaties in het bijbehorende gen PPP3CA zijn in verband gebracht met een ernstige kinderstoornis met epilepsie en ontwikkelingsachterstand. Deze studie stelt een eenvoudige maar cruciale vraag: hoe kan het veranderen van slechts één bouwsteen in calcineurine de hersenontwikkeling zo dramatisch verstoren?
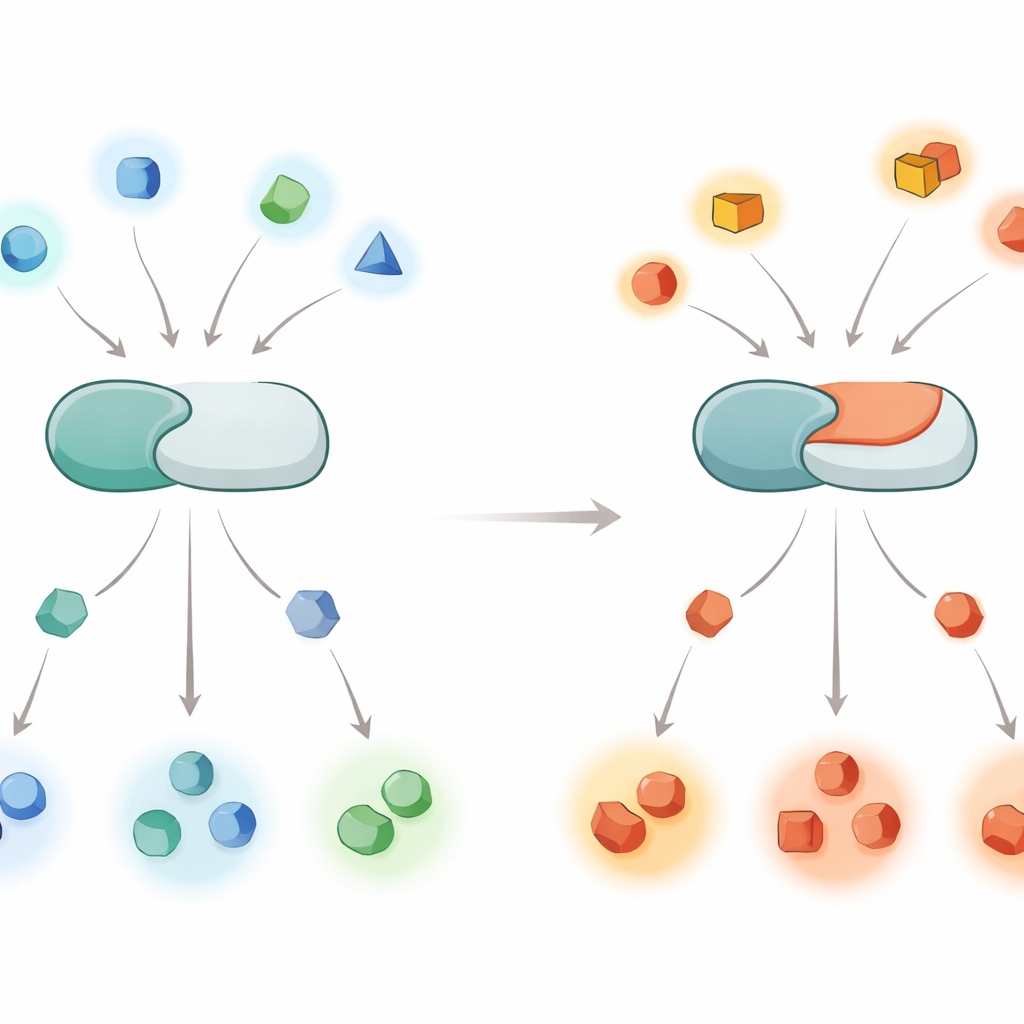
Hoe Cellen Chemische Schakelaars Gebruiken
Eiwitten in cellen functioneren als arbeiders op een lopende band, en fosfaatlabels zijn de aan/uit‑schakelaars die hen regelen. Kinases voegen fosfaatgroepen toe, terwijl fosfatases ze verwijderen. Calcineurine is een fosfatase die reageert op calciumsignalen en vooral actief is in de hersenen, waar het bijdraagt aan ontwikkeling, leren en geheugen. Omdat calcineurine honderden tot duizenden verschillende eiwitdoelen raakt, kunnen zelfs kleine fouten in welke eiwitten het aanpakt door veel signaalpaden heen doorwerken en bijdragen aan aandoeningen zoals Alzheimer, de ziekte van Parkinson en de zeldzame ontwikkelingsaandoening bekend als PPP3CA‑gerelateerde DEE91.
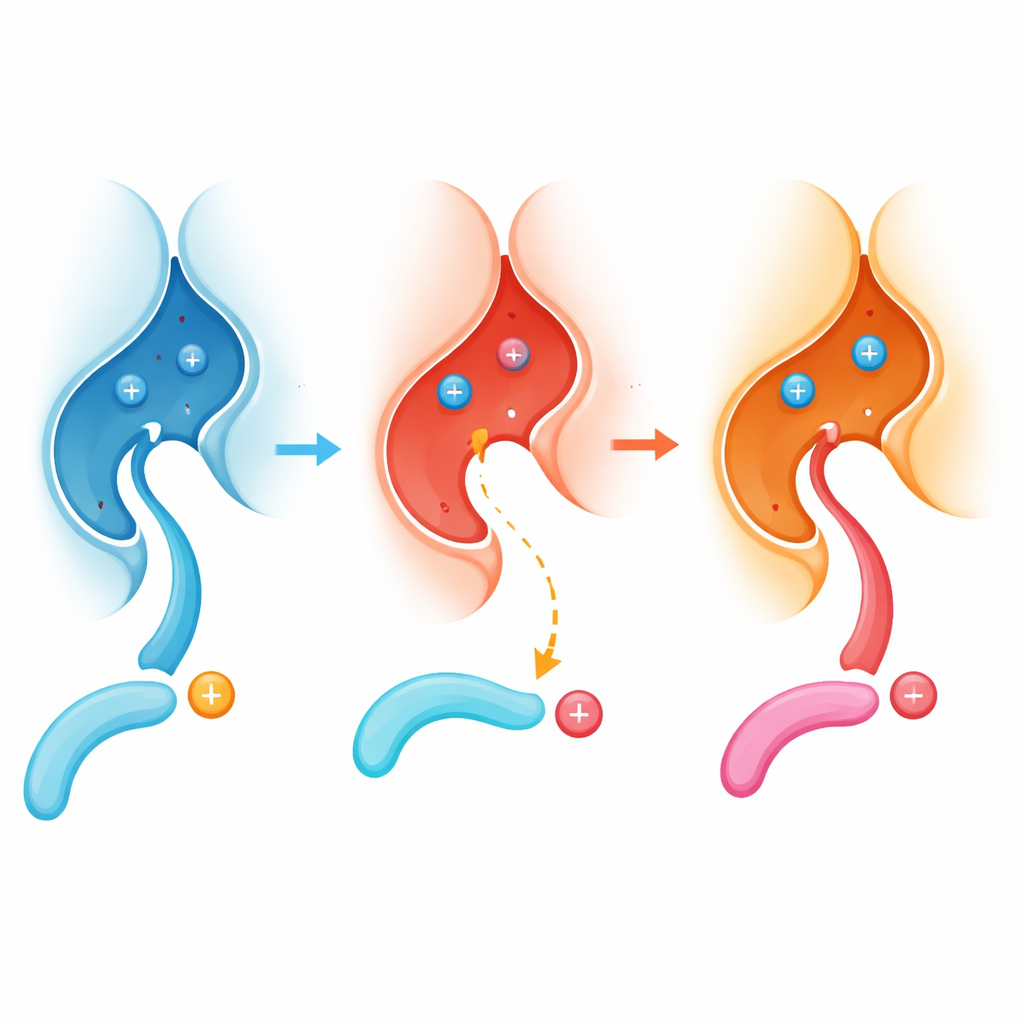
Een Verborgen Andockingsplekje Dichtbij het Werkingsgebied
De onderzoekers richtten zich op hoe calcineurine specifieke plekken op zijn eiwitdoelen herkent. Ze ontdekten een eerder onopgemerkt "rekruteringspocket" direct naast het actieve centrum van het enzym. Veel doelwiteiwitten die eerst door bepaalde kinases worden gemodificeerd, dragen een positief geladen aminozuur, arginine, direct voor het fosfaatlabel. Met structurele biologie, bindingsmetingen en proefbuisreacties toonde het team aan dat deze arginine in een negatief geladen pocket rond een calcineurineresidu genaamd E282 past, en zo het gelabelde gebied naar de juiste positie trekt zodat het enzym het fosfaat efficiënt kan verwijderen.
Wat de E282K‑mutatie Werkelijk Doet
Bij kinderen met PPP3CA‑gerelateerde DEE91 valt de meest voorkomende verandering in calcineurine samen met het verwisselen van E282 voor een ander aminozuur, lysine, wat de E282K‑variant creëert. Verrassend genoeg lieten kristalstructuren zien dat de algehele vorm van het enzym vrijwel ongewijzigd blijft en dat zijn andere andockplaatsen nog functioneren. Het cruciale verschil zit in de lokale chemie: de ooit zure, open pocket rond E282 wordt meer basisch en deels geblokkeerd door een nieuwe interne zoutbrug. Daardoor binden peptiden die afhankelijk zijn van een arginine dat in deze pocket past nu slecht en worden veel minder efficiënt gedephosphoryleerd.
Een Wereldwijde Verschuiving in Wie Wordt Uitgeschakeld
Om te onderzoeken hoe ver dit effect reikt, onderzochten de auteurs duizenden fosfopeptiden afgeleid van humane cellen en vergeleken hoe het normale en het gemuteerde calcineurine zich in de loop van de tijd gedragen. Normaal calcineurine gaf sterk de voorkeur aan plekken met positief geladen residuen (zoals arginine of lysine) direct voor het fosfaat. In contrast verloor de E282K‑versie veel van deze voorkeur en verwerkte in plaats daarvan gemakkelijker plekken met negatief geladen residuen op die positie. Vergelijkbare patronen verschenen toen het team de twee enzymvormen tot expressie bracht in levende cellijnen, waaronder een neuron‑achtige lijn, en massaspectrometrie gebruikte om te inventariseren welke eiwitplaatsen meer of minder gedephosphoryleerd werden. De mutatie stelt het enzym effectief terug van het prefereren van "basische" plekken naar het bevoordelen van "zure" plekken.
Waarom Dit Belangrijk Is voor Kinderen met DEE91
Het werk toont aan dat de E282K‑mutatie calcineurine niet simpelweg verzwakt of uitschakelt. In plaats daarvan herschakelt het welke eiwitschakelaars het enzym kan omslaan, en verlegt zo signaalnetwerken door de hele cel. In groeiende en ontwikkelende hersencellen verstoort deze brede misrichting van signalen—weg van hun normale arginine‑rijke doelen en naar andere plekken—waarschijnlijk de fijn afgestelde programma’s die neuronale groei, connectiviteit en elektrische activiteit regelen. Door deze specifieke rekruteringspocket te identificeren en te laten zien hoe E282K diens lading en toegankelijkheid verandert, legt de studie een moleculaire basis voor het begrijpen van de ziekte en suggereert ze nieuwe wegen om naar therapieën te zoeken die de juiste substrate‑selectie kunnen herstellen, zelfs als de mutatie zelf niet kan worden teruggedraaid.
Bronvermelding: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Trefwoorden: calcineurine, PPP3CA‑mutatie, eiwitfosforylering, neuro‑ontwikkelingsstoornissen, enzym‑specificiteit