Clear Sky Science · pt
A variante clínica de missense E282K em PPP3CA/calcineurina altera a desfosforilação de substratos ao modificar o recrutamento no sítio ativo
Quando uma Pequena Mudança em uma Enzima Cerebral Causa Grandes Problemas
Nossas células cerebrais ligam e desligam sinais constantemente ao adicionar e remover pequenas marcas químicas chamadas fosfatos. Uma enzima-chave, chamada calcineurina, é responsável por remover muitas dessas marcas, e mutações herdadas ou novas em seu gene, PPP3CA, têm sido associadas a um distúrbio infantil grave com epilepsia e atraso no desenvolvimento. Este estudo investiga uma pergunta simples, porém importante: como a troca de apenas um bloco construtor na calcineurina pode perturbar tão dramaticamente o desenvolvimento cerebral?
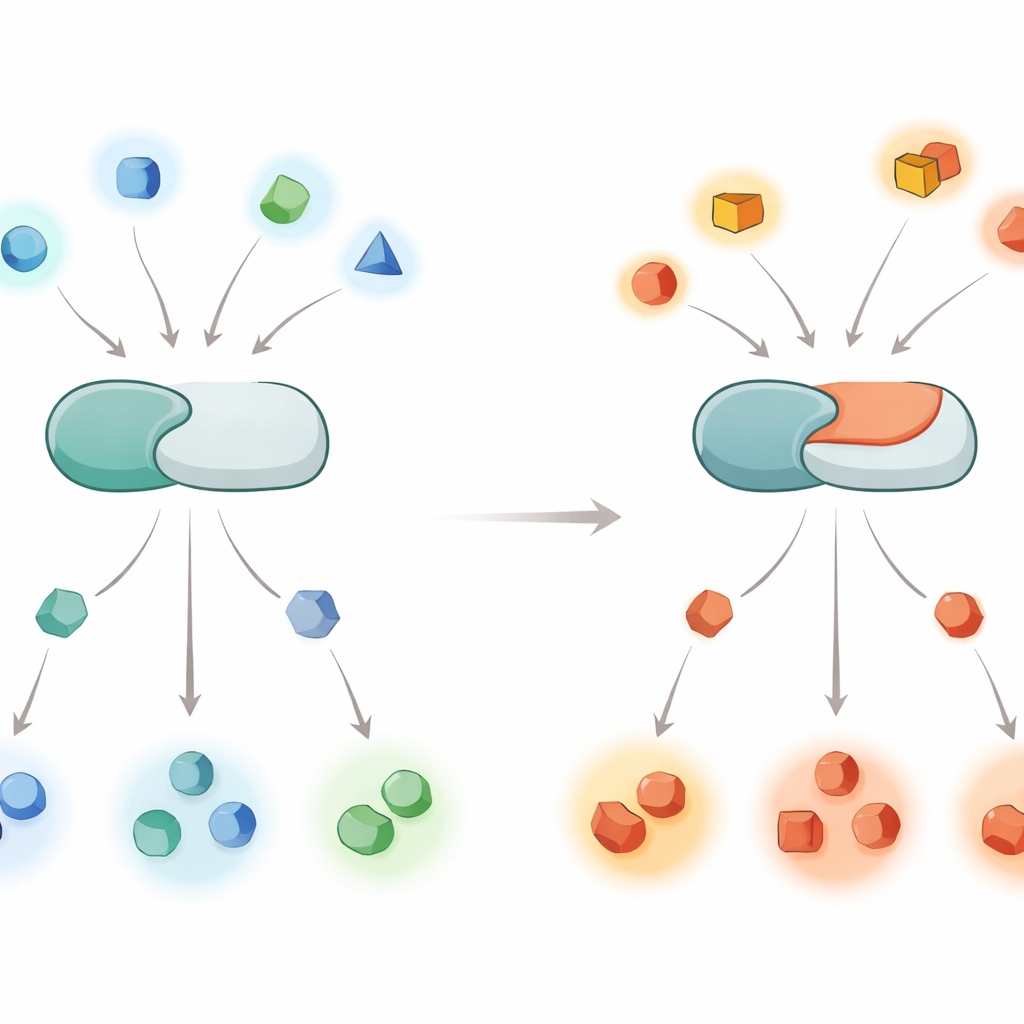
Como as Células Usam Interruptores Químicos
As proteínas dentro das células atuam como operários em uma linha de montagem, e as marcas de fosfato são os interruptores que as controlam. Quinases anexam grupos fosfato, enquanto fosfatases os removem. A calcineurina é uma fosfatase que responde a sinais de cálcio e é especialmente ativa no cérebro, onde ajuda a regular o desenvolvimento, a aprendizagem e a memória. Como a calcineurina atua sobre centenas a milhares de alvos proteicos diferentes, mesmo pequenos erros em quais proteínas ela escolhe podem repercutir por muitas vias de sinalização, contribuindo para doenças como Alzheimer, Parkinson e a rara condição de desenvolvimento conhecida como DEE91 relacionada a PPP3CA.
Um Bolso de Ancoragem Oculto Perto do Sítio de Trabalho
Os pesquisadores se concentraram em como a calcineurina reconhece pontos específicos em suas proteínas-alvo. Eles descobriram um “bolso de recrutamento” anteriormente não reconhecido bem ao lado do sítio ativo da enzima. Muitas proteínas-alvo que são primeiro modificadas por certas quinases carregam um aminoácido com carga positiva, a arginina, imediatamente antes da marca de fosfato. Usando biologia estrutural, medidas de ligação e reações em tubo de ensaio, a equipe mostrou que essa arginina se encaixa em um bolso carregado negativamente, construído ao redor de um resíduo da calcineurina chamado E282, ajudando a puxar o sítio fosforilado para a posição correta para que a enzima possa remover o fosfato eficientemente.
O Que a Mutação E282K Realmente Faz
Em crianças com DEE91 relacionada a PPP3CA, a alteração mais comum na calcineurina troca o resíduo E282 por outro aminoácido, lisina, criando a variante E282K. Surpreendentemente, estruturas cristalinas revelaram que a forma geral da enzima permanece quase inalterada e seus outros sítios de ancoragem continuam funcionais. A diferença crucial está na química local: o bolso antes ácido e aberto ao redor de E282 torna-se mais básico e parcialmente bloqueado por uma nova ponte salina interna. Como resultado, peptídeos que dependem da arginina encaixar-se nesse bolso agora se ligam mal e são desfosforilados com muito menos eficiência.
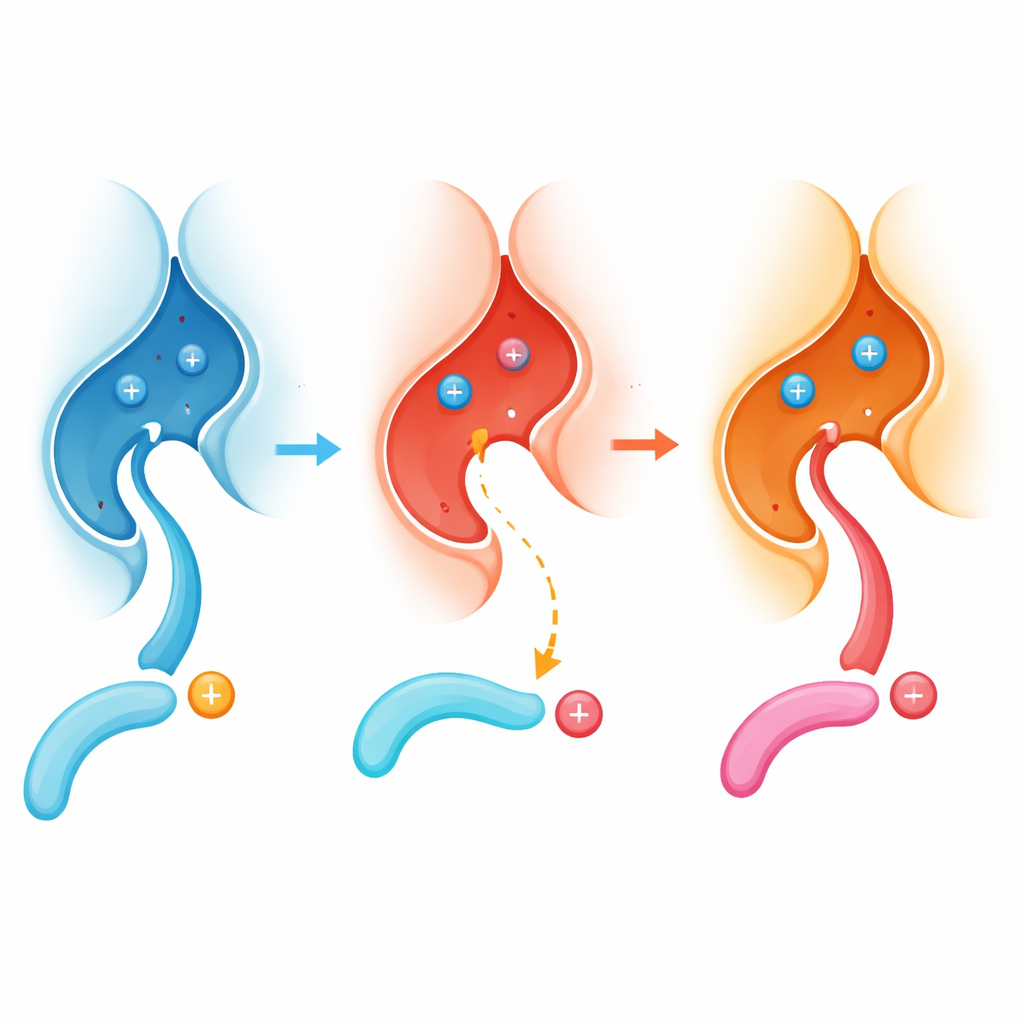
Uma Mudança Global em Quem é Desligado
Para avaliar a extensão desse efeito, os autores examinaram milhares de fosfopeptídeos derivados de células humanas e compararam como a calcineurina normal e a mutante agiam sobre eles ao longo do tempo. A calcineurina normal favorecia fortemente sítios com resíduos carregados positivamente (como arginina ou lisina) imediatamente antes do fosfato. Em contraste, a versão E282K perdeu grande parte dessa preferência e passou a processar mais prontamente sítios com resíduos carregados negativamente nessa posição. Padrões semelhantes surgiram quando a equipe expressou as duas formas da enzima em linhagens celulares vivas, incluindo uma linha do tipo neuronal, e usou espectrometria de massa para catalogar quais sítios proteicos foram mais ou menos desfosforilados. A mutação efetivamente recalibra a enzima, que deixa de favorecer sítios “básicos” e passa a preferir os “ácidos”.
Por Que Isso Importa para Crianças com DEE91
O trabalho mostra que a mutação E282K não simplesmente enfraquece a calcineurina ou a desliga. Em vez disso, ela reorganiza quais interruptores proteicos a enzima pode acionar, deslocando redes de sinalização por toda a célula. Em células cerebrais em crescimento e desenvolvimento, essa má orientação ampla dos sinais — afastando-se de seus alvos normais ricos em arginina e indo em direção a locais diferentes — provavelmente perturba os programas finamente equilibrados que controlam o crescimento neuronal, a conectividade e a atividade elétrica. Ao identificar esse bolso de recrutamento específico e como E282K altera sua carga e acessibilidade, o estudo estabelece uma base molecular para entender a doença e sugere novas maneiras de buscar terapias que possam restaurar a seleção adequada de substratos, mesmo que a mutação em si não possa ser revertida.
Citação: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Palavras-chave: calcineurina, mutação PPP3CA, fosforilação de proteínas, transtornos do neurodesenvolvimento, especificidade enzimática