Clear Sky Science · de
Die klinische Missense-Variante E282K in PPP3CA/Calcineurin verschiebt die Substrat-Dephosphorylierung durch veränderte Rekrutierung am aktiven Zentrum
Wenn eine winzige Veränderung in einem Hirnenzym großen Schaden anrichtet
Unsere Nervenzellen schalten Signale ständig an und aus, indem sie winzige chemische Markierungen, sogenannte Phosphate, anbringen oder entfernen. Ein wichtiges Enzym namens Calcineurin ist für das Entfernen vieler dieser Markierungen verantwortlich; vererbte oder neu auftretende Mutationen in seinem Gen PPP3CA werden mit einer schweren kindlichen Erkrankung mit Epilepsie und Entwicklungsverzögerung in Verbindung gebracht. Diese Studie stellt eine einfache, aber wichtige Frage: Wie kann der Austausch nur eines einzigen Bausteins in Calcineurin die Gehirnentwicklung so dramatisch stören?
Wie Zellen chemische Schalter verwenden
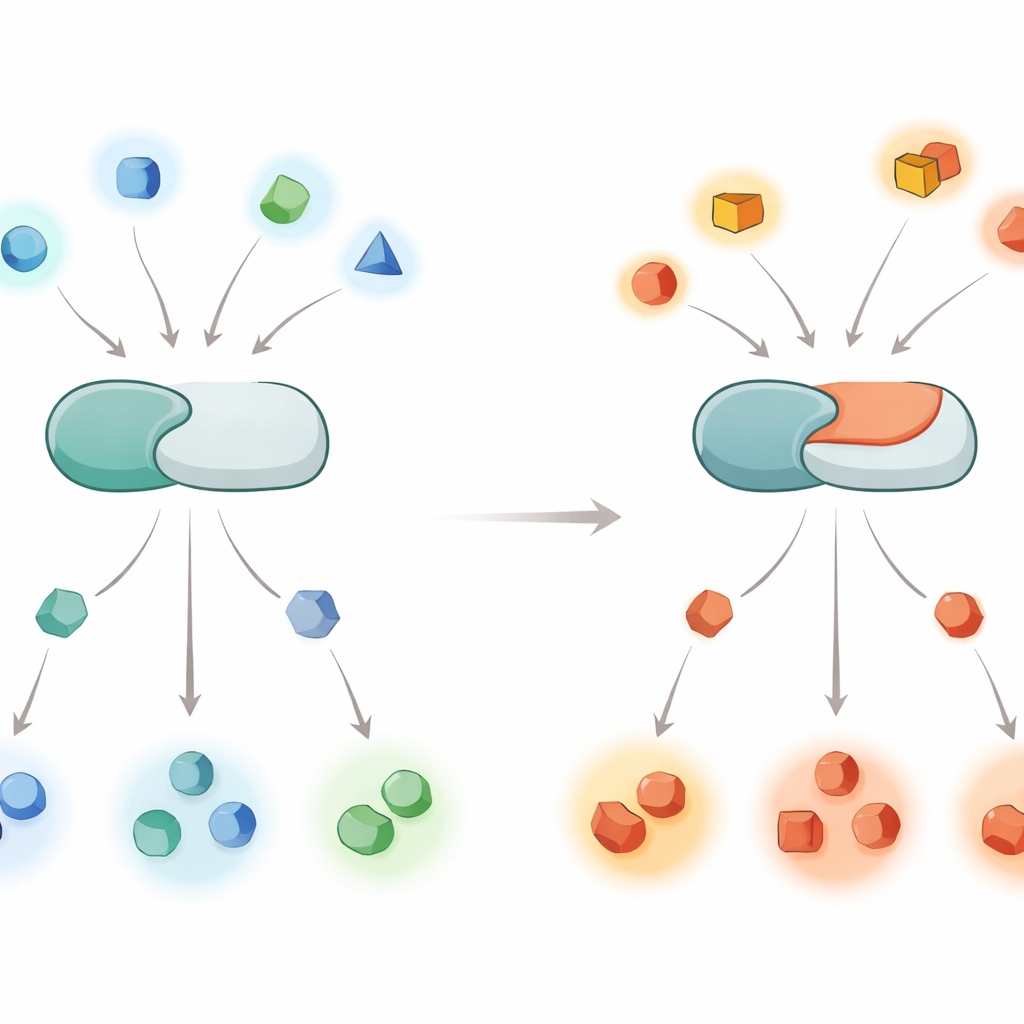
Proteine in Zellen arbeiten wie Arbeiter an einem Fließband, und Phosphatmarken sind die Ein-/Ausschalter, die sie steuern. Kinasen fügen Phosphatgruppen hinzu, während Phosphatasen sie entfernen. Calcineurin ist eine Phosphatase, die auf Kalziumsignale reagiert und besonders im Gehirn aktiv ist, wo sie Entwicklung, Lernen und Gedächtnis mitsteuert. Da Calcineurin Hunderte bis Tausende verschiedene Proteinziele berührt, können schon kleine Fehler darin, welche Proteine es bearbeitet, viele Signalwege durchdringen und zu Erkrankungen wie Alzheimer, Parkinson und der seltenen Entwicklungsstörung PPP3CA-assoziiertes DEE91 beitragen.
Eine versteckte Andocktasche nahe der Wirkstelle
Die Forschenden konzentrierten sich darauf, wie Calcineurin bestimmte Stellen auf seinen Protein‑Zielen erkennt. Sie entdeckten eine bislang unerkannte „Rekrutierungs‑Tasche“ direkt neben dem aktiven Zentrum des Enzyms. Viele Zielproteine, die zuvor von bestimmten Kinasen modifiziert wurden, tragen eine positiv geladene Aminosäure, Arginin, unmittelbar vor der Phosphatmarke. Mithilfe von Strukturbiologie, Bindungsmessungen und Reaktionen im Reagenzglas zeigte das Team, dass dieses Arginin in eine negativ geladene Tasche rund um die Calcineurin‑Restseite E282 hineinschlüpft und so die markierte Stelle positioniert, damit das Enzym das Phosphat effizient entfernen kann.
Was die E282K‑Mutation tatsächlich bewirkt
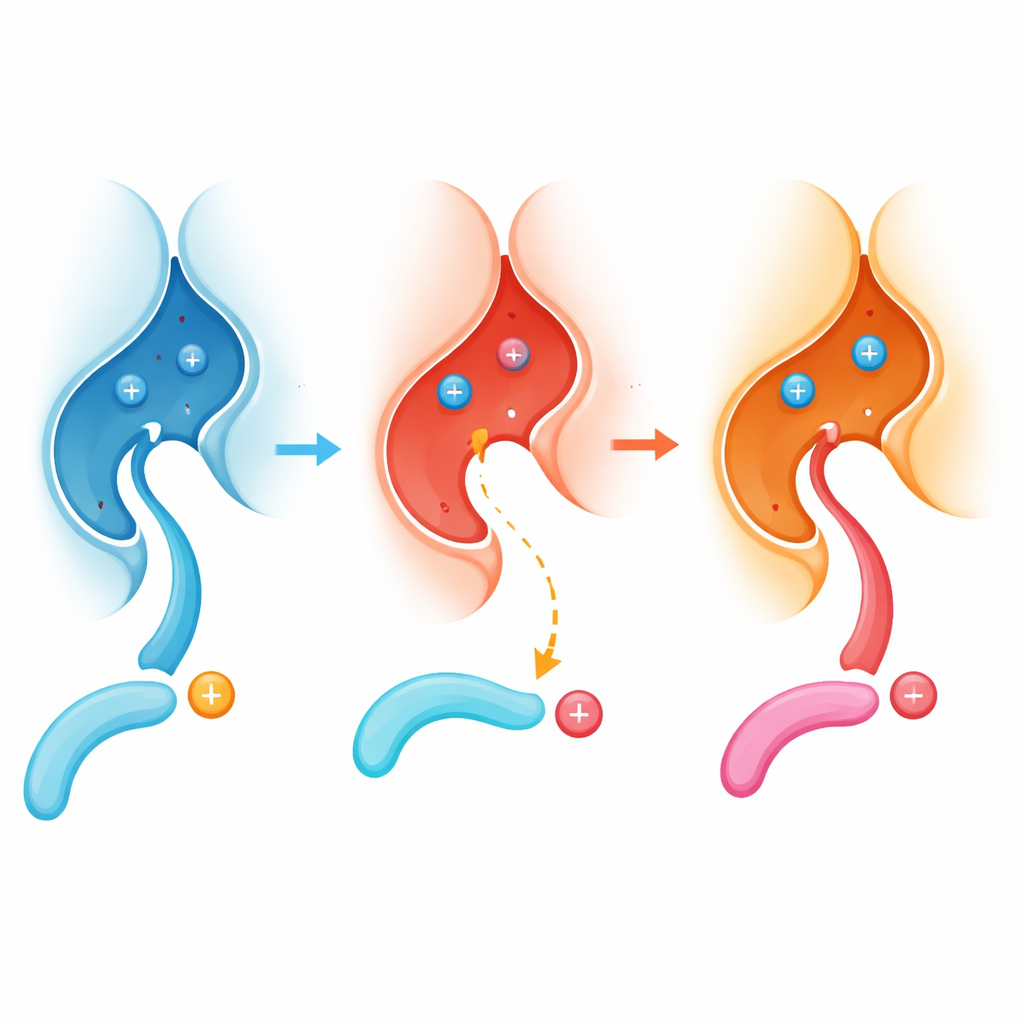
Bei Kindern mit PPP3CA‑assoziiertem DEE91 ist die häufigste Veränderung in Calcineurin der Austausch von E282 gegen eine andere Aminosäure, Lysin, was die Variante E282K erzeugt. Überraschenderweise zeigten Kristallstrukturen, dass die Gesamtgestalt des Enzyms nahezu unverändert bleibt und seine anderen Andockstellen weiter funktionieren. Der entscheidende Unterschied liegt in der lokalen Chemie: Die ehemals saure, offene Tasche um E282 wird basischer und ist teilweise durch eine neue interne Salzbrücke blockiert. Infolgedessen binden Peptide, die auf das Einpassen eines Arginins in diese Tasche angewiesen sind, nun schlecht und werden deutlich weniger effizient dephosphoryliert.
Eine globale Verschiebung dessen, was abgeschaltet wird
Um zu untersuchen, wie weitreichend dieser Effekt ist, analysierten die Autorinnen und Autoren Tausende von Phosphopeptiden aus menschlichen Zellen und verglichen, wie normales und mutiertes Calcineurin diese im Zeitverlauf bearbeiteten. Das normale Calcineurin bevorzugte stark Stellen mit positiv geladenen Resten (wie Arginin oder Lysin) direkt vor dem Phosphat. Im Gegensatz dazu hatte die E282K‑Variante einen Großteil dieser Präferenz verloren und bearbeitete stattdessen leichter Stellen mit negativ geladenen Resten an dieser Position. Ähnliche Muster zeigten sich, als das Team die beiden Enzymformen in lebenden Zelllinien, darunter eine neuronähnliche Linie, exprimierte und Massenspektrometrie nutzte, um zu katalogisieren, welche Proteinstellen stärker oder weniger dephosphoryliert wurden. Die Mutation stimmt das Enzym effektiv von einer Bevorzugung „basischer“ Stellen auf eine Vorliebe für „saure“ um.
Warum das für Kinder mit DEE91 wichtig ist
Die Arbeit zeigt, dass die E282K‑Mutation Calcineurin nicht einfach nur schwächt oder ausschaltet. Stattdessen verändert sie, welche Proteinschalter das Enzym umlegen kann, und verschiebt dadurch Signalnetzwerke in der Zelle. In wachsenden und sich entwickelnden Nervenzellen stört diese weitreichende Fehlleitung von Signalen — weg von ihren normalen argininreichen Zielen und hin zu anderen Stellen — wahrscheinlich die fein austarierten Programme, die neuronales Wachstum, Konnektivität und elektrische Aktivität steuern. Indem die Studie genau diese Rekrutierungs‑Tasche und beschreibt, wie E282K deren Ladung und Zugänglichkeit verändert, legt sie eine molekulare Grundlage zum Verständnis der Erkrankung und gibt Hinweise für neue Therapieansätze, die die richtige Substratauswahl wiederherstellen könnten, auch wenn die Mutation selbst nicht rückgängig gemacht werden kann.
Zitation: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Schlüsselwörter: Calcineurin, PPP3CA-Mutation, Proteinphosphorylierung, neuroentwicklungsstörungen, Enzymspezifität