Clear Sky Science · fr
La variante clinique missense E282K de PPP3CA/calcineurine modifie la déphosphorylation des substrats en altérant le recrutement au site actif
Quand un tout petit changement dans une enzyme cérébrale provoque de grands dégâts
Nos cellules cérébrales activent et désactivent en permanence des signaux en ajoutant ou en retirant de minuscules marqueurs chimiques appelés phosphates. Une enzyme clé, la calcineurine, est responsable du retrait de nombreux de ces marqueurs, et des mutations héritées ou de novo dans son gène, PPP3CA, ont été associées à un grave trouble infantile avec épilepsie et retard du développement. Cette étude pose une question simple mais essentielle : comment le remplacement d’un seul acide aminé dans la calcineurine peut-il perturber à ce point le développement cérébral ?
Comment les cellules utilisent des interrupteurs chimiques
Les protéines à l’intérieur des cellules fonctionnent comme des ouvriers sur une chaîne de montage, et les marques de phosphate sont les interrupteurs marche/arrêt qui les contrôlent. Les kinases ajoutent des phosphates, tandis que les phosphatases les enlèvent. La calcineurine est une phosphatase qui répond aux signaux calciques et qui est particulièrement active dans le cerveau, où elle aide à réguler le développement, l’apprentissage et la mémoire. Parce que la calcineurine cible des centaines à des milliers de protéines différentes, de petites erreurs dans le choix de ses cibles peuvent se répercuter sur de nombreuses voies de signalisation, contribuant à des maladies comme Alzheimer, la maladie de Parkinson et la rare affection développementale connue sous le nom de DEE91 liée à PPP3CA.
Une poche d’accostage cachée près du site actif
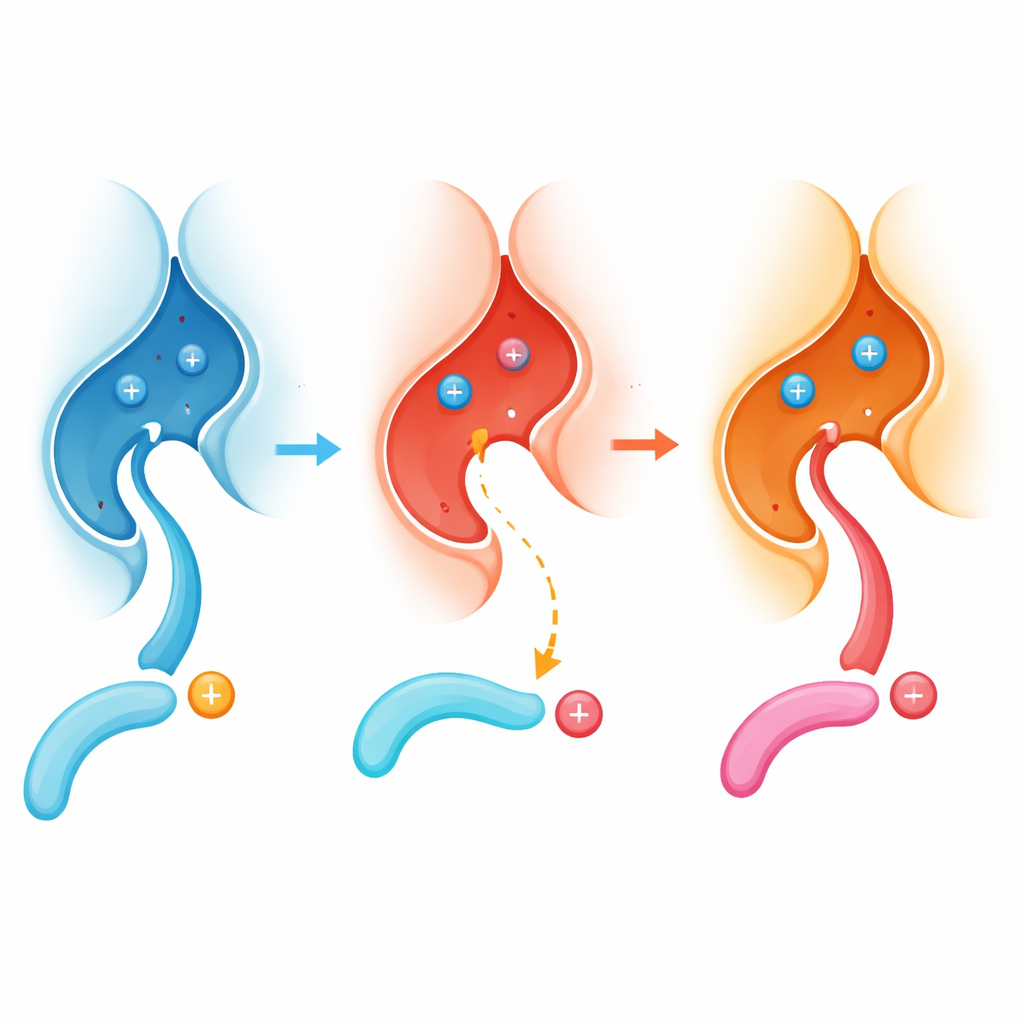
Les chercheurs se sont intéressés à la façon dont la calcineurine reconnaît des sites spécifiques sur ses protéines cibles. Ils ont découvert une « poche de recrutement » jusqu’alors méconnue, juste à côté du site de travail de l’enzyme. De nombreuses protéines cibles préalablement modifiées par certaines kinases portent un acide aminé chargé positivement, l’arginine, immédiatement avant le site phosphorylé. Grâce à la biologie structurale, à des mesures d’affinité et à des réactions in vitro, l’équipe a montré que cette arginine s’insère dans une poche chargée négativement construite autour d’un résidu de la calcineurine nommé E282, aidant ainsi à attirer le site phosphorylé pour que l’enzyme puisse efficacement retirer le phosphate.
Ce que fait réellement la mutation E282K
Chez les enfants atteints de DEE91 lié à PPP3CA, le changement le plus fréquent dans la calcineurine remplace E282 par un autre acide aminé, la lysine, créant la variante E282K. De manière surprenante, les structures cristallines ont révélé que la conformation globale de l’enzyme reste presque inchangée et que ses autres sites d’accostage fonctionnent toujours. La différence cruciale réside dans la chimie locale : la poche auparavant acide et ouverte autour de E282 devient plus basique et partiellement obstruée par une nouvelle liaison ionique interne. En conséquence, les peptides qui nécessitent qu’une arginine se loge dans cette poche se lient désormais mal et sont beaucoup moins efficacement déphosphorylés.
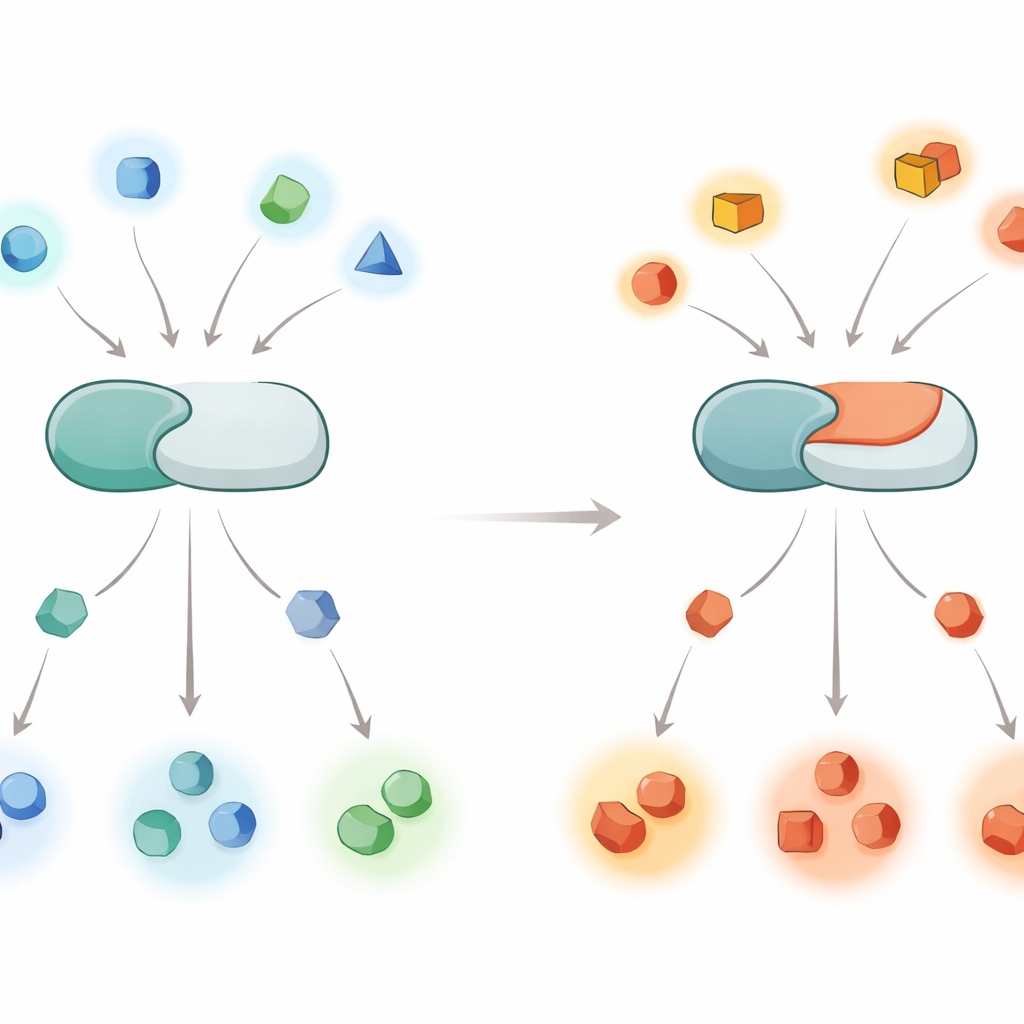
Un basculement global des cibles déphosphorylées
Pour mesurer l’étendue de cet effet, les auteurs ont examiné des milliers de phosphopeptides dérivés de cellules humaines et comparé l’action de la calcineurine normale et de la variante mutée sur ces peptides au fil du temps. La calcineurine normale favorisait fortement les sites comportant des résidus chargés positivement (comme l’arginine ou la lysine) juste avant le phosphate. En revanche, la version E282K avait perdu une grande partie de cette préférence et traitait plus facilement les sites présentant des résidus chargés négativement à cette position. Des schémas similaires sont apparus lorsque l’équipe a exprimé les deux formes enzymatiques dans des lignées cellulaires vivantes, y compris une lignée de type neuronale, et a utilisé la spectrométrie de masse pour inventorier les sites protéiques plus ou moins déphosphorylés. La mutation réoriente effectivement l’enzyme, qui passe d’une préférence pour les sites « basiques » à une préférence pour les sites « acides ».
Pourquoi cela importe pour les enfants atteints de DEE91
Cette étude montre que la mutation E282K n’affaiblit pas simplement la calcineurine ni ne l’éteint. Elle réécrit plutôt la sélection des protéines que l’enzyme peut modifier, décalant les réseaux de signalisation à travers la cellule. Dans les cellules cérébrales en croissance et en développement, cette mauvaise orientation globale des signaux — s’éloignant des cibles normales riches en arginine vers d’autres sites — perturbe vraisemblablement les programmes finement équilibrés qui contrôlent la croissance neuronale, la connectivité et l’activité électrique. En identifiant précisément cette poche de recrutement et la manière dont E282K modifie sa charge et son accessibilité, l’étude établit une base moléculaire pour comprendre la maladie et suggère de nouvelles pistes pour rechercher des thérapies susceptibles de restaurer la sélection correcte des substrats, même si la mutation elle‑même ne peut pas être réversible.
Citation: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Mots-clés: calcineurine, mutation PPP3CA, phosphorylation des protéines, troubles du développement neurologique, spécificité enzymatique