Clear Sky Science · pl
Klasyczny wariant missense E282K w PPP3CA/calcineurinie przesuwa dehydroksylację substratów poprzez zmianę rekrutacji w miejscu aktywnym
Kiedy drobna zmiana w enzymie mózgowym powoduje poważne kłopoty
Komórki naszego mózgu nieustannie włączają i wyłączają sygnały przez dodawanie i usuwanie małych chemicznych znaczników zwanych grupami fosforanowymi. Kluczowy enzym zwany kalcyneuryną odpowiada za usuwanie wielu z tych znaczników, a dziedziczne lub de novo mutacje w jego genie, PPP3CA, powiązano z ciężkim zaburzeniem dziecięcym objawiającym się epilepsją i opóźnieniem rozwoju. W tym badaniu postawiono proste, lecz istotne pytanie: jak zmiana zaledwie jednego elementu budulcowego w kalcyneurynie może tak dramatycznie zakłócić rozwój mózgu?
Jak komórki wykorzystują chemiczne przełączniki
Białka wewnątrz komórek działają jak pracownicy na taśmie produkcyjnej, a znaczniki fosforanowe są przełącznikami włącz/wyłącz, które nimi sterują. Kinazy przyłączają grupy fosforanowe, natomiast fosfatazy je usuwają. Kalcyneuryna jest fosfatazą reagującą na sygnały wapniowe i jest szczególnie aktywna w mózgu, gdzie pomaga kontrolować rozwój, uczenie się i pamięć. Ponieważ kalcyneuryna oddziałuje z setkami do tysięcy różnych celów białkowych, nawet drobne błędy w tym, na które białka działa, mogą rozlać się na wiele ścieżek sygnałowych, przyczyniając się do chorób takich jak Alzheimer, choroba Parkinsona oraz rzadkie zaburzenie rozwojowe znane jako DEE91 związane z PPP3CA.
Ukryta kieszonka dokująca blisko miejsca aktywnego
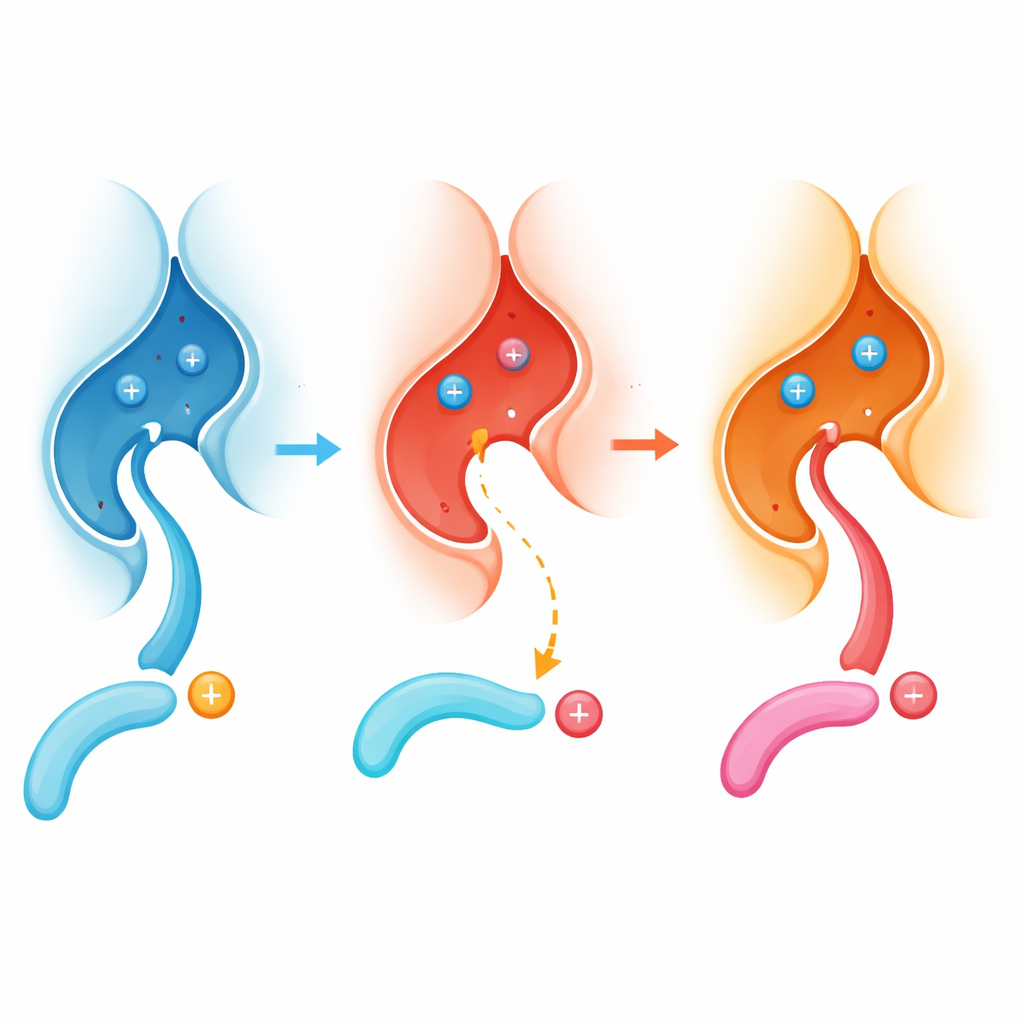
Naukowcy skupili się na tym, jak kalcyneuryna rozpoznaje konkretne miejsca na swoich celach białkowych. Odkryli wcześniej nieznane „kieszonkowe miejsce rekrutacji” tuż obok miejsca aktywnego enzymu. Wiele białek-celów, które najpierw są modyfikowane przez pewne kinazy, nosi dodatnio naładowany aminokwas, argininę, bezpośrednio przed miejscem fosforylacji. Dzięki biologii strukturalnej, pomiarom wiązania i reakcjom in vitro zespół wykazał, że ta arginina wsuwa się w ujemnie naładowaną kieszeń zbudowaną wokół reszty kalcyneuryny oznaczonej jako E282, pomagając przyciągnąć znakowane miejsce tak, by enzym mógł efektywnie usunąć fosforan.
Co tak naprawdę robi mutacja E282K
U dzieci z DEE91 związanym z PPP3CA najczęstszą zmianą w kalcyneurynie jest podstawienie E282 na inny aminokwas, lizynę, tworząc wariant E282K. Ku zaskoczeniu, struktury krystaliczne wykazały, że ogólny kształt enzymu pozostaje niemal niezmieniony, a jego inne miejsca dokujące nadal funkcjonują. Kluczowa różnica leży w lokalnej chemii: niegdyś kwaśna, otwarta kieszeń wokół E282 staje się bardziej zasadowa i częściowo zablokowana przez nowy wewnętrzny mostek solny. W rezultacie peptydy polegające na umieszczeniu argininy w tej kieszeni teraz słabo wiążą się i są de-fosforylowane znacznie mniej efektywnie.
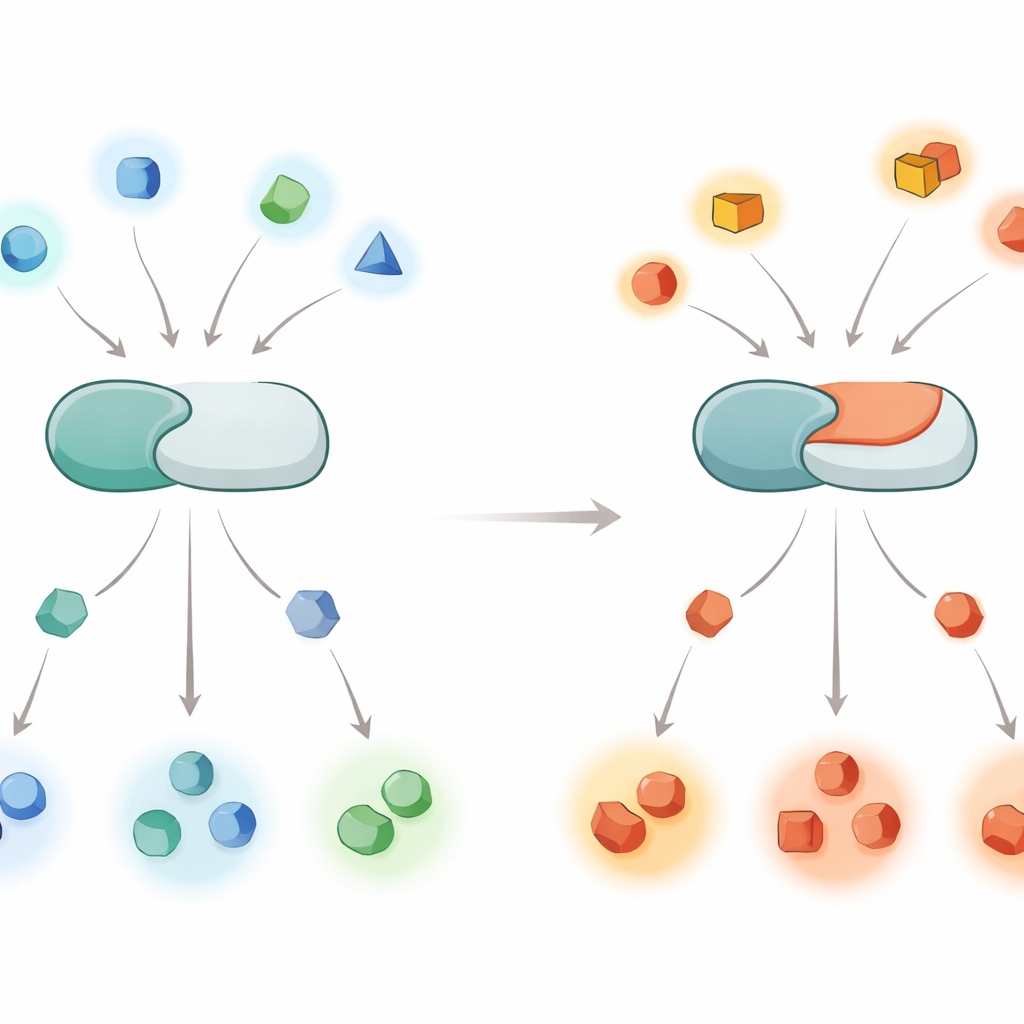
Globalne przesunięcie tego, co zostaje wyłączone
Aby sprawdzić zasięg tego efektu, autorzy przeanalizowali tysiące fosfopeptydów pochodzących z komórek ludzkich i porównali, jak normalna i zmutowana kalcyneuryna działały na nie w czasie. Normalna kalcyneuryna wyraźnie faworyzowała miejsca z dodatnio naładowanymi resztami (takimi jak arginina lub lizyna) tuż przed fosforanem. W przeciwieństwie do tego wersja E282K utraciła dużą część tej preferencji i zamiast tego chętniej przetwarzała miejsca z ujemnie naładowanymi resztami na tej pozycji. Podobne wzorce pojawiły się, gdy zespół ekspresjonował obie formy enzymu w żywych liniach komórkowych, w tym w linii neuronopodobnej, i użył spektrometrii mas do katalogowania, które miejsca białkowe były bardziej lub mniej de-fosforylowane. Mutacja skutecznie przestroiła enzym z upodobań do „zasadowych” miejsc na faworyzowanie „kwasowych”.
Dlaczego to ma znaczenie dla dzieci z DEE91
Praca pokazuje, że mutacja E282K nie osłabia po prostu kalcyneuryny ani jej nie wyłącza. Zamiast tego przestawia, które przełączniki białkowe enzym może odwrócić, przesuwając sieci sygnałowe w całej komórce. W rosnących i rozwijających się komórkach mózgowych takie szerokie przekierowanie sygnałów — z dala od normalnych celów bogatych w argininę i w kierunku innych miejsc — prawdopodobnie zaburza precyzyjnie wyważone programy kontrolujące wzrost neuronów, łączność i aktywność elektryczną. Poprzez zidentyfikowanie tej konkretnej kieszeni rekrutacyjnej i tego, jak E282K zmienia jej ładunek i dostęp, badanie kładzie molekularne podstawy do zrozumienia choroby i sugeruje nowe drogi poszukiwania terapii, które mogłyby przywrócić prawidłowy wybór substratów, nawet jeśli sama mutacja nie może zostać odwrócona.
Cytowanie: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Słowa kluczowe: kalcyneuryna, mutacja PPP3CA, fosforylacja białek, zaburzenia rozwoju neurologicznego, specyficzność enzymu