Clear Sky Science · ar
الطفرة السينية السريرية E282K في PPP3CA/الكالسينورين تغير إزالة الفسفرة من الركائز عن طريق تعديل تجنيد الموقع الفعّال
عندما يتسبب تغيير طفيف في إنزيم دماغي بمشاكل كبيرة
تقوم خلايانا العصبية باستمرار بتشغيل وإيقاف الإشارات عن طريق إضافة وإزالة علامات كيميائية صغيرة تُسمى الفوسفات. إنزيم رئيسي يُدعى الكالسينورين مسؤول عن إزالة الكثير من هذه العلامات، وقد ارتبطت طفرات موروثة أو جديدة في جينه PPP3CA باضطراب طفولي شديد يتضمن الصرع وتأخر التطور. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهمّاً: كيف يمكن لتغيير كتلة بناء واحدة فقط في الكالسينورين أن يُعطّل تطور الدماغ بشكل درامي؟
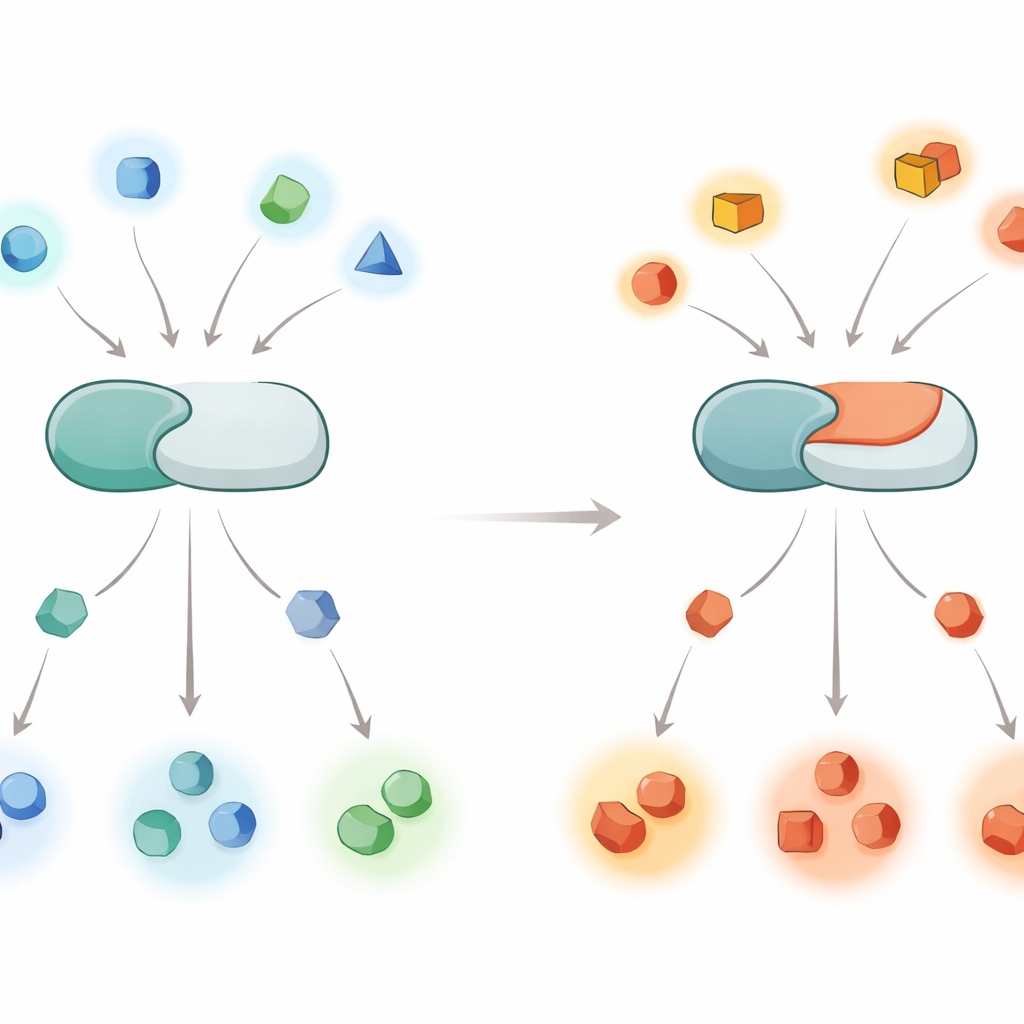
كيف تستخدم الخلايا مفاتيح كيميائية
تعمل البروتينات داخل الخلايا مثل عمال على خط تجميع، وعلامات الفوسفات هي مفاتيح التشغيل/الإيقاف التي تُتحكم بها. تُلحق الكينازات مجموعات الفوسفات، بينما تزيل الفسفاتازات هذه المجموعات. الكالسينورين هو فسفاتاز يستجيب لإشارات الكالسيوم ونشط خصوصاً في الدماغ، حيث يساعد في التحكم بالتطور والتعلم والذاكرة. وبما أن الكالسينورين يتعامل مع مئات إلى آلاف الأهداف البروتينية المختلفة، فإن أخطاء صغيرة في أي من البروتينات التي يؤثر عليها يمكن أن تمتد عبر العديد من شبكات الإشارة، مساهِمةً في اضطرابات مثل مرض ألزهايمر وباركنسون والحالة النادرة المعروفة بخلل التطور الناجم عن PPP3CA أو DEE91.
جيب إرساء مخفي قرب موقع العمل
ركز الباحثون على كيفية تعرف الكالسينورين على مواقع محددة في بروتيناته الهدف. اكتشفوا "جيب تجنيد" لم يُلاحَظ سابقاً بجوار موقع عمل الإنزيم مباشرة. العديد من البروتينات الهدف التي تُعدّل أولاً بواسطة بعض الكينازات تحمل حمضاً أمينياً موجب الشحنة، الأرغينين، مباشرة قبل علامة الفوسفات. باستخدام علم البنية، وقياسات الارتباط، وتجارب أنبوب الاختبار، أظهر الفريق أن هذا الأرغينين يستقر في جيب سالب الشحنة مبني حول البقايا E282 في الكالسينورين، مما يساعد على سحب الموقع الموسوم إلى موضع مناسب لكي يزيله الإنزيم بكفاءة.
ما الذي تفعله طفرة E282K فعلاً
في الأطفال المصابين بمتلازمة DEE91 المرتبطة بـ PPP3CA، التغيير الأكثر شيوعاً في الكالسينورين يستبدل E282 بحمض أميني مختلف، الليسين، مكوّناً المتغير E282K. بشكل مفاجئ، كشفت الهياكل البلورية أن الشكل العام للإنزيم يبقى شبه دون تغيير وأن مواقع الإرساء الأخرى لا تزال تعمل. الفرق الحاسم يكمن في الكيمياء المحلية: الجيب الذي كان حمضياً ومفتوحاً حول E282 يصبح أكثر قاعدية ومُسدود جزئياً بجسر ملحي داخلي جديد. ونتيجة لذلك، الببتيدات التي تعتمد على ملاءمة أرغينين داخل هذا الجيب ترتبط ضعيفاً الآن وتُزال فسفراتها بكفاءة أقل بكثير.
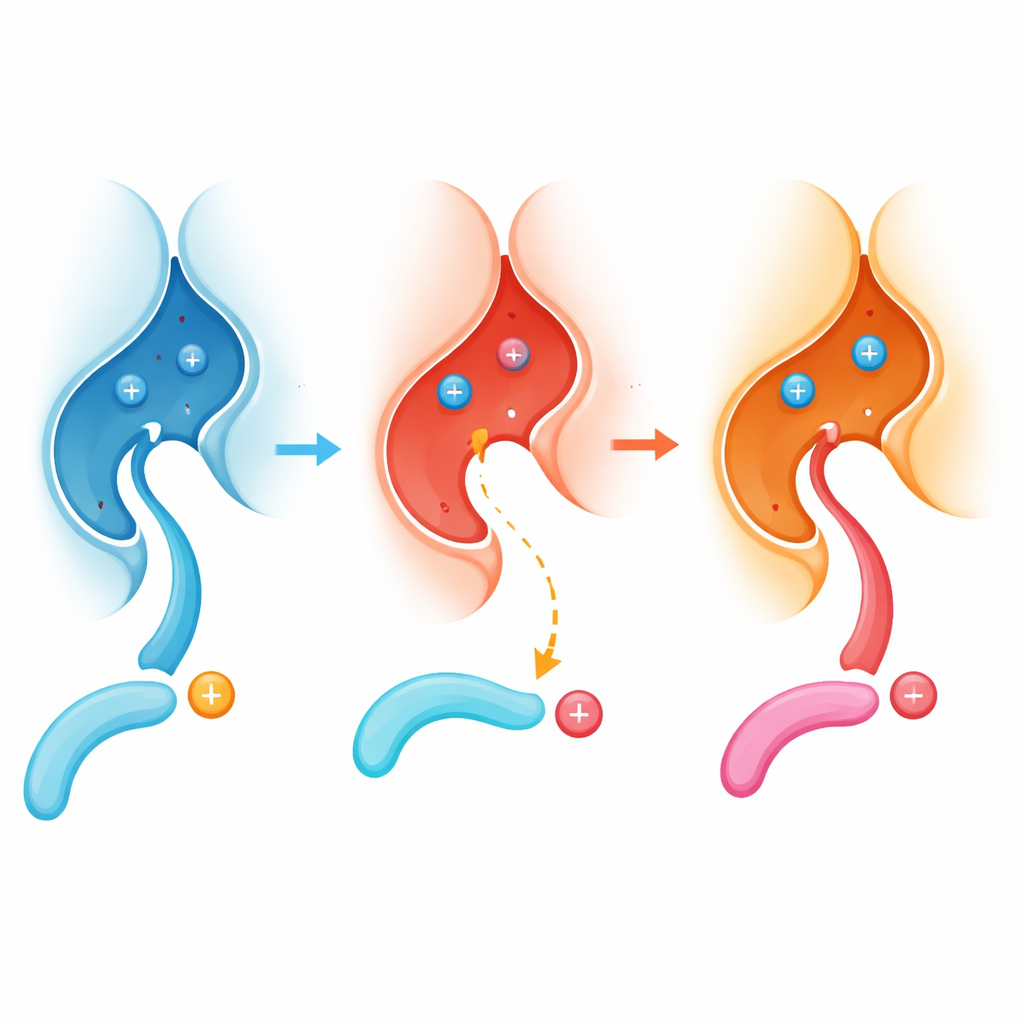
تحوّل شامل في من يتم إيقافه
لفحص مدى انتشار هذا التأثير، فحص المؤلفون آلاف الببتيدات المفسفرة المأخوذة من خلايا بشرية وقارنوا كيف يتعامل الكالسينورين الطبيعي والمطفّر مع هذه الببتيدات عبر الزمن. كان الكالسينورين الطبيعي يفضّل بقوة المواقع التي تسبقها بقايا موجبة الشحنة (مثل الأرغينين أو الليسين) مباشرة قبل الفوسفات. بالمقابل، فقد الإصدار E282K جزءاً كبيراً من هذا التفضيل وبات يعالج بسهولة أكبر المواقع التي تحوي بقايا سالبة الشحنة في ذلك الموضع. ظهرت أنماط مماثلة عندما عبّر الفريق عن الصيغتين الإنزيميتين في خطوط خلوية حية، بما في ذلك خط يشبه الخلايا العصبية، واستخدموا قياس طيف الكتلة لحصر مواقع البروتين التي أزيلت منها الفسفرة أكثر أو أقل. تعمل الطفرة عملياً على إعادة ضبط إنزيم من تفضيل المواقع "القاعدية" إلى تفضيل المواقع "الحمضية".
لماذا هذا مهم للأطفال المصابين بـ DEE91
تُظهر الدراسة أن طفرة E282K لا تضعف الكالسينورين ببساطة أو تطفئه. بل إنها تعيد توجيه أي مفاتيح بروتينية يستطيع الإنزيم قلبها، مما يغيّر شبكات الإشارة في الخلية بأكملها. في خلايا الدماغ النامية والمتطورة، من المحتمل أن يؤدي هذا التضليل الواسع للإشارات — بعيداً عن أهدافها الغنية بالأرغينين وباتجاه مواقع مختلفة — إلى اضطراب البرامج الدقيقة المتوازنة التي تتحكم في نمو الخلايا العصبية وتواصلها ونشاطها الكهربائي. من خلال تحديد هذا الجيب الخاص بالتجنيد وكيف يغيّر E282K شحنتَه ووصوله، تضع الدراسة أساساً جزيئياً لفهم المرض وتقترح طرقاً جديدة للبحث عن علاجات قد تستعيد اختيار الركائز المناسب، حتى لو تعذر عكس الطفرة نفسها.
الاستشهاد: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
الكلمات المفتاحية: الكالسينورين, طفرة PPP3CA, فسفرة البروتين, اضطرابات نمو عصبي, تخصيص الإنزيم