Clear Sky Science · es
La variante clínica de cambio de sentido E282K en PPP3CA/calcineurina desplaza la desfosforilación de sustratos al alterar el reclutamiento en el sitio activo
Cuando un pequeño cambio en una enzima cerebral causa grandes problemas
Nuestras células cerebrales activan y desactivan señales de forma continua añadiendo y quitando pequeñas marcas químicas llamadas fosfatos. Una enzima clave llamada calcineurina se encarga de eliminar muchas de estas marcas, y mutaciones heredadas o de novo en su gen, PPP3CA, se han relacionado con un trastorno infantil grave con epilepsia y retraso del desarrollo. Este estudio plantea una pregunta simple pero importante: ¿cómo puede cambiar un solo bloque constructivo en la calcineurina perturbar de forma tan dramática el desarrollo cerebral?
Cómo usan las células los interruptores químicos
Las proteínas dentro de las células actúan como operarios en una línea de montaje, y las marcas de fosfato son los interruptores encendido/apagado que las controlan. Las quinasas añaden grupos fosfato, mientras que las fosfatasas los eliminan. La calcineurina es una fosfatasa que responde a señales de calcio y es especialmente activa en el cerebro, donde ayuda a controlar el desarrollo, el aprendizaje y la memoria. Dado que la calcineurina actúa sobre cientos o miles de dianas proteicas distintas, incluso pequeños errores en qué proteínas reconoce pueden propagarse por muchas vías de señalización, contribuyendo a trastornos como el Alzheimer, el Parkinson y la rara condición de desarrollo conocida como DEE91 relacionada con PPP3CA.
Un bolsillo de reclutamiento oculto junto al sitio de trabajo
Los investigadores se centraron en cómo la calcineurina reconoce puntos específicos en sus proteínas diana. Descubrieron un “bolsillo de reclutamiento” previamente no reconocido justo al lado del sitio activo de la enzima. Muchas proteínas diana que primero son modificadas por ciertas quinasas llevan un aminoácido cargado positivamente, arginina, inmediatamente antes de la marca de fosfato. Mediante biología estructural, medidas de afinidad y reacciones en tubo de ensayo, el equipo mostró que esa arginina encaja en un bolsillo cargado negativamente construido alrededor de un residuo de la calcineurina llamado E282, ayudando a situar el sitio fosforilado para que la enzima pueda eliminar el fosfato de forma eficiente.
Lo que realmente hace la mutación E282K
En niños con DEE91 relacionado con PPP3CA, el cambio más común en la calcineurina sustituye la E282 por otro aminoácido, lisina, creando la variante E282K. Sorprendentemente, las estructuras cristalinas revelaron que la forma global de la enzima permanece casi sin cambios y que sus otros sitios de acoplamiento siguen funcionando. La diferencia crucial radica en la química local: el bolsillo que antes era ácido y abierto alrededor de E282 se vuelve más básico y queda parcialmente bloqueado por un nuevo puente salino interno. Como resultado, los péptidos que dependen de que una arginina encaje en ese bolsillo ahora se unen mal y se desfosforilan con mucha menos eficiencia.
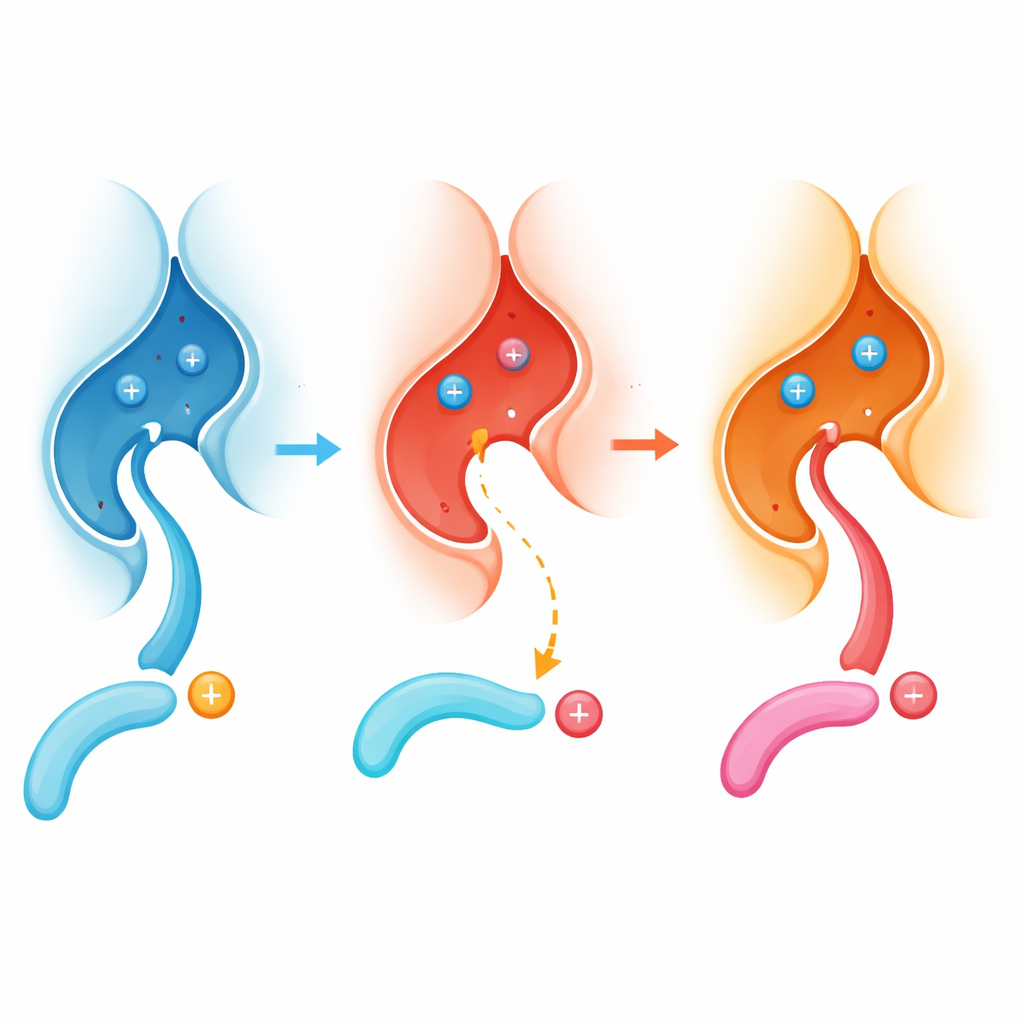
Un cambio global en quién se apaga
Para evaluar hasta dónde llega este efecto, los autores examinaron miles de fosfopéptidos derivados de células humanas y compararon cómo actuaban la calcineurina normal y la mutante sobre ellos a lo largo del tiempo. La calcineurina normal prefería con fuerza los sitios con residuos cargados positivamente (como arginina o lisina) justo antes del fosfato. En contraste, la versión E282K había perdido gran parte de esa preferencia y, en su lugar, procesaba más fácilmente los sitios con residuos cargados negativamente en esa posición. Patrones similares aparecieron cuando el equipo expresó las dos formas en líneas celulares vivas, incluida una línea neuronal, y usó espectrometría de masas para catalogar qué sitios proteicos se desfosforilaban más o menos. La mutación efectivamente retunea la enzima, pasando de preferir sitios “básicos” a favorecer los “ácidos”.
Por qué esto importa para los niños con DEE91
El trabajo muestra que la mutación E282K no limita simplemente la calcineurina ni la apaga. En cambio, reconfigura qué interruptores proteicos puede accionar la enzima, desplazando las redes de señalización en toda la célula. En las células cerebrales en crecimiento y desarrollo, esta amplia mala dirección de señales —alejándolas de sus dianas normales ricas en arginina y llevándolas hacia sitios distintos— probablemente perturba los programas finamente equilibrados que controlan el crecimiento neuronal, la conectividad y la actividad eléctrica. Al identificar este bolsillo de reclutamiento específico y cómo la E282K altera su carga y acceso, el estudio sienta una base molecular para entender la enfermedad y sugiere nuevas vías para buscar terapias que puedan restaurar la selección adecuada de sustratos, incluso si la mutación en sí no puede revertirse.
Cita: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Palabras clave: calcineurina, mutación PPP3CA, fosforilación de proteínas, trastornos del neurodesarrollo, especificidad enzimática