Clear Sky Science · tr
SFPQ, DNA tekrarlarındaki R-döngülerine histon H3.3 birikimini yönlendirerek genom kararlılığını korur
DNA Tekrarlarımızın Koruyucuları
DNA’mızın büyük bölümü bir zamanlar “gereksiz” olarak nitelendirilen uzun, tekrarlayan dizilerden oluşur. Bugün bu bölgelerin düzensiz davranabildiğini, R-döngüleri adı verilen sıra dışı üç zincirli düğümler oluşturduğunu; bunların DNA kopyalanmasını engellediğini ve hasara yol açtığını biliyoruz. Bu çalışma, SFPQ adındaki bir proteinin bu tekrarlayan bölgelerde devriye gezdiğini, paketlemelerini düzenlediğini ve böylece genom kararlılığını gizlice korurken belirli kanserlerin bağışıklık sistemiyle etkileşimlerini bile şekillendirdiğini ortaya koyuyor.
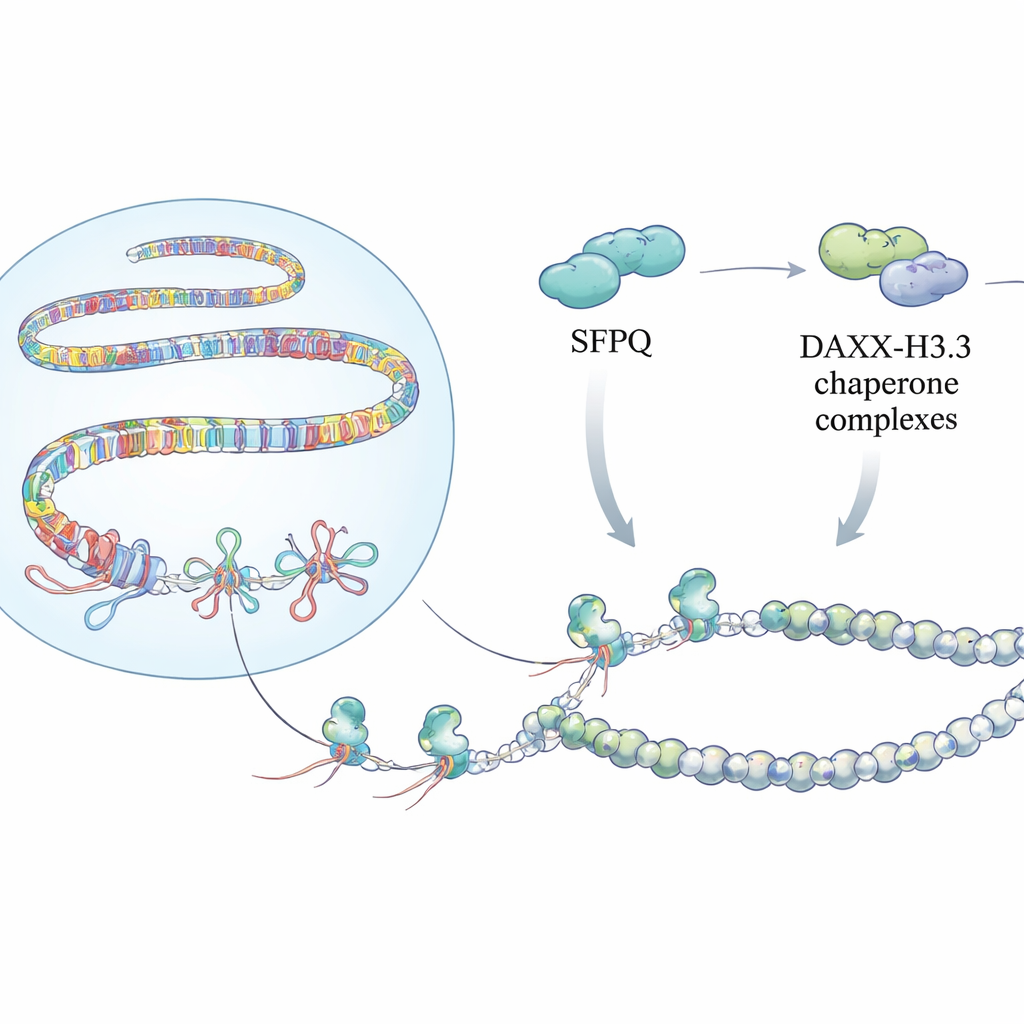
Genomdaki Gizli Düğümler
Bir gen okunduğunda, DNA’dan geçici bir RNA kopyası üretilir. Özellikle kromozom uçlarındaki telomerler, ortadaki sentromerlere yakın peri-sentromerik uydu dizileri ve LINE/SINE gibi hareketli elementler gibi tekrarlayan DNA bölgelerinde, yeni RNA geri kıvrılıp DNA’ya hibridleşebilir. Bu, RNA–DNA hibriti ile eşleşmiş kısa bir R-döngüsü ve yerinden çıkmış tek iplikli bir DNA oluşturarak meydana gelir. R-döngüleri küçük, kontrollü miktarlarda faydalı olabilirken; kalıcı olanlar DNA’yı kopyalayan makine için engel işlevi görerek kromozom kırılmalarına, hatalı hücre bölünmesine ve genom kararsızlığına—kanser ve genetik hastalıkların ana özelliklerine—yol açar.
R-Döngü Devriye Proteini
Araştırmacılar, uzun süredir bir RNA-bağlayıcı ve ekson kesim faktörü olarak bilinen SFPQ’nin, tekrarlayan bölgelerdeki R-döngülerinin adanmış bir sensörü olduğunu gösteriyor. SFPQ azaltılan hücrelerde ekip, hibrit-spesifik antikorlar ve dizileme tabanlı haritalama kullanarak telomerler, peri-sentromerik uydular ve retroelementler boyunca daha fazla R-döngüsü tespit etti. Bu sıcak noktalar, güçlü replikasyon stresi ve DNA hasarı sinyalleriyle örtüştü. Saflaştırılmış SFPQ ile yapılan biyokimyasal deneyler nedenini ortaya koydu: SFPQ olağan çift sarmallı DNA veya RNA–DNA duplekslerine iyi bağlanmaz, ancak özellikle doğal tekrar RNA’larına benzer açık RNA uçları taşıyan üç zincirli yapıları, yani R-döngülerini kuvvetle tercih eder. Bu seçicilik SFPQ’yi genomun en tekrar içeren yerlerinde problemli R-döngülerini tanıyan ilk müdahale görevlisi yapar.
Koruyucu Kromatin Zırhı İnşa Etmek
Bu düğümleri tespit etmek hikâyenin yalnızca bir kısmı. Ekip, SFPQ’nin kromatina özel bir histon varyantı olan H3.3’ü teslim eden DAXX ile fiziksel olarak etkileştiğini keşfetti. H3.3, tekrarlayan DNA’yı susturan ve kontrolsüz rekombinasyonu önleyen kararlı nükleozomlar oluşturulmasına yardımcı olur. Genom çapında yapılan haritalama deneyleri SFPQ ve DAXX’in klasik gen promotörlerinden ziyade genler arası ve intronik tekrar bölgelerinde sıkça ortak bağlanma bölgeleri paylaştığını gösterdi. SFPQ kaybolduğunda DAXX tekrar bölgelerinden düzenleyici bölgelere kaydı ve H3.3 tekrar zengin bölgelerine verimli biçimde yerleştirilemedi; oysa toplam H3.3 protein düzeyleri değişmemişti. Sonuç olarak, bu tekrarların üzerindeki kromatin şablonu düzensizleşti ve R-döngüleri ile replikasyon stresi birikimine izin verdi.
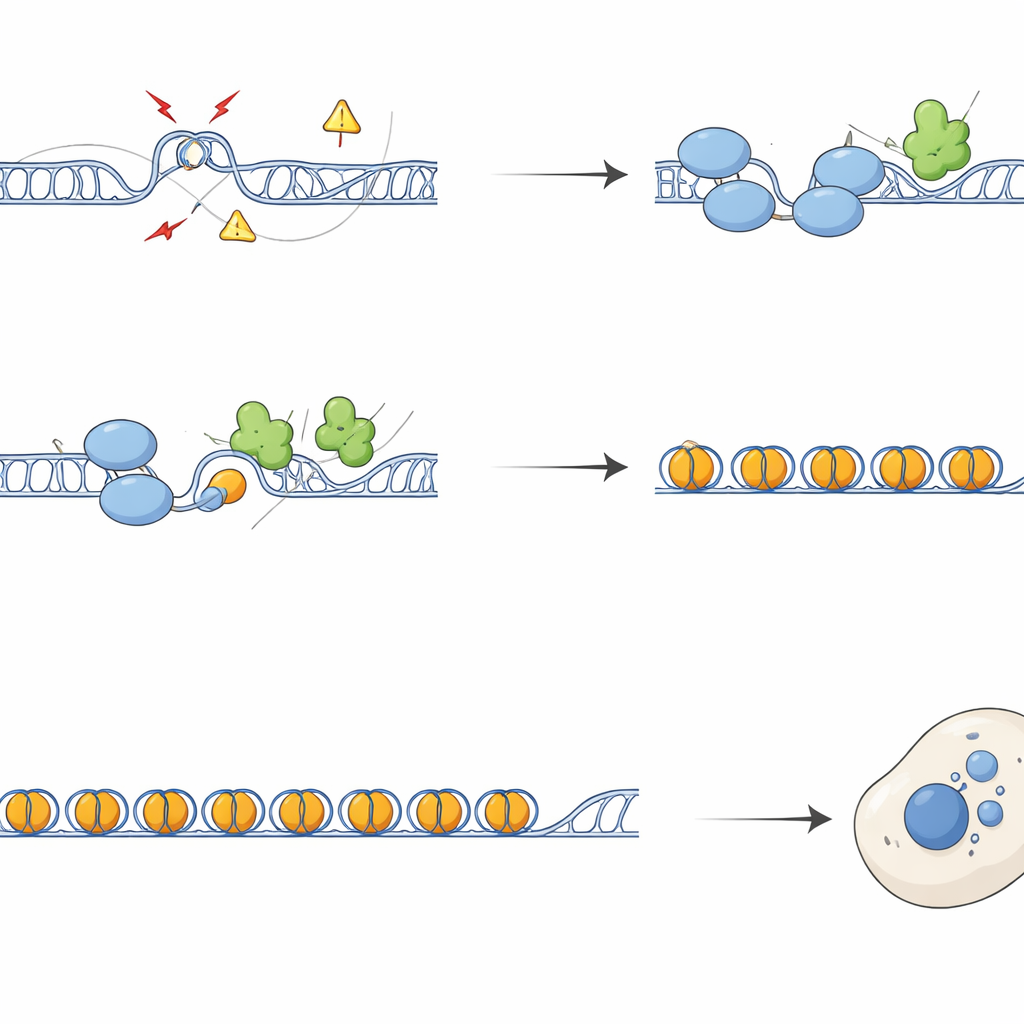
Kırık Kromozomlardan Harekete Geçen Bağışıklığa
SFPQ olmadan tekrarlayan bölgeler DNA hasarı belirteçleri ve tamir faktörleri biriktirdi; kromozomlarda daha fazla kırık ve kardeş kromatitler arasında değişim görüldü. Hücre bölünmesi sırasında bu hasar hatalı segregasyona dönüştü ve kromatin köprüleri ile ana çekirdeğin dışında küçük ekstra DNA içeren cisimcikler olan mikronükleiler oluştu. Bu mikronükleiler sıklıkla telomerik ve sentromerik diziler içeriyor ve yanlış yerdeki DNA’yı algılayan cGAS ile kaplanıyordu; cGAS–STING yolunu aktive eden bir sensör. SFPQ veya DAXX eksik hücreler interferon ve inflamatuvar genleri aktive etti; bu etki büyük ölçüde R-döngülerini gideren RNaseH1’in aşırı eksprese edilmesiyle veya STING’in bloke edilmesiyle geri çevrilebildi. Böylece tekrar bölgelerindeki aşırı R-döngüleri, sitoplazmik DNA kalıntılarının üretimi yoluyla doğrudan bağışıklık sinyaline Beslenir.
Kanser ve Hasta Sonuçları İçin Çıkarımlar
Sarkom hasta verilerinde yüksek SFPQ ekspresyonu daha kötü sağkalımla korele olurken; SFPQ kaybında görülen türde güçlü doğal bağışıklık aktivasyonunu yansıtan bir gen imzası daha iyi sonuçlarla ilişkilendirildi. Düşük SFPQ ama yüksek bağışıklık-imzası ekspresyonuna sahip hastalar en iyi düzeyde geçti; bu, tümörlerde tekrarlarda bu koruyucu eksenin devre dışı bırakılmasının kanser hücrelerini istemeden bağışıklık sistemine açabileceğini gösteriyor. Çalışma, SFPQ’nin R-döngülerini algılamasından DAXX–H3.3 aracılı kromatin korumasına, genom kararsızlığının önlenmesine ve doğal bağışıklığın baskılanmasına uzanan mekanik zinciri ortaya koyuyor. Genel okuyucu için temel mesaj şudur: SFPQ tekrarlayan DNA için bir bakım ekibi gibidir—tehlikeli RNA–DNA düğümlerini tespit eder, bu bölgeleri düzleştirmek ve zırhlamak için paketleme yardımcılarını çağırır, böylece kromozomları sağlam ve bağışıklık alarmlarını sessiz tutar; kanserler bu dengeyi sömürebilir, ama gelecekteki tedaviler bu dengeyi hastanın lehine çevirebilir.
Atıf: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Anahtar kelimeler: R-döngüleri, genom kararlılığı, histon H3.3, doğal bağışıklık, sarkom