Clear Sky Science · pt
SFPQ direciona a deposição da histona H3.3 a R-loops em repetições de DNA para proteger a estabilidade do genoma
Guardas das Nossas Repetições de DNA
Grande parte do nosso DNA é composta por longas sequências repetidas antes descartadas como “lixo”. Hoje sabemos que essas regiões podem se comportar mal, formando nós incomuns de três fios chamados R-loops, que travam a cópia do DNA e desencadeiam danos. Este estudo revela como uma proteína chamada SFPQ patrulha esses trechos repetitivos, organiza seu empacotamento e, ao fazê-lo, protege silenciosamente a estabilidade do genoma e até influencia como certos cânceres interagem com o sistema imunológico.
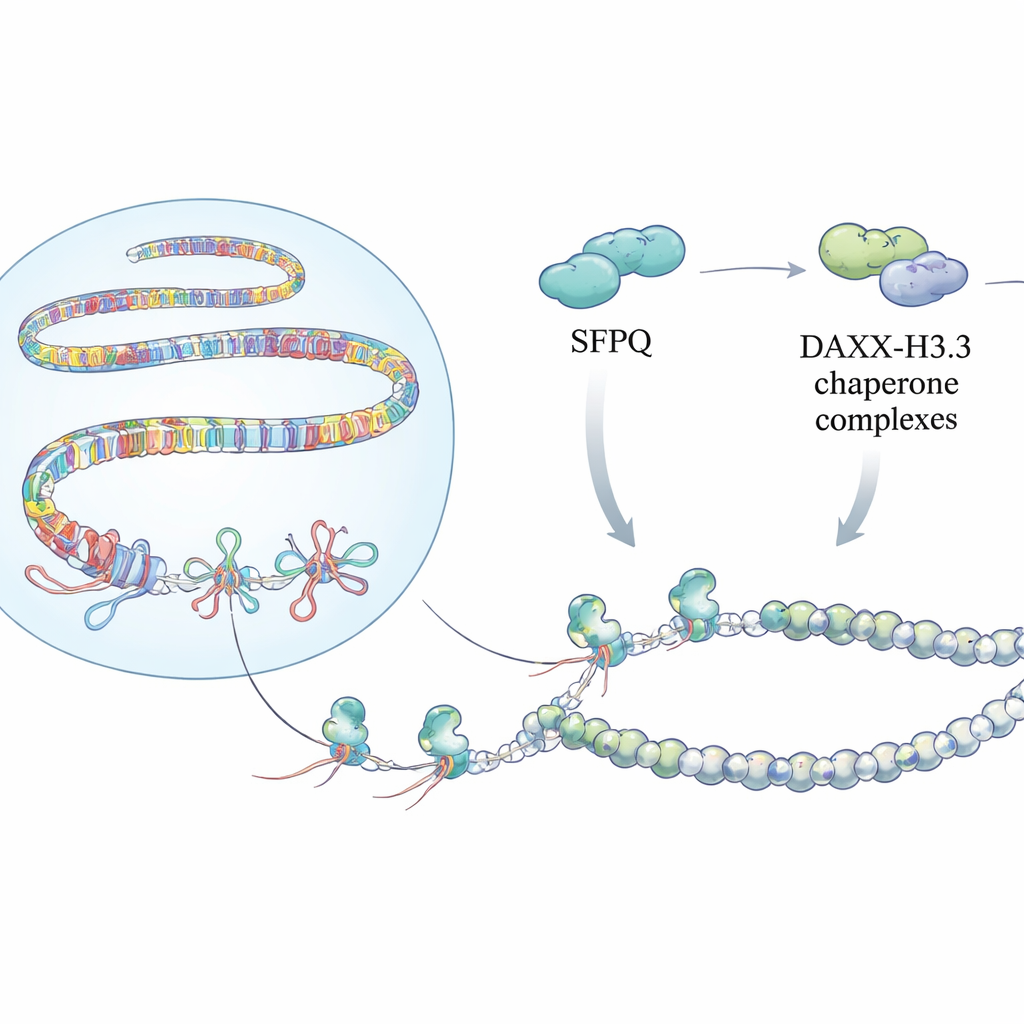
Nós Ocultos no Genoma
Quando um gene é lido, uma cópia temporária em RNA é feita a partir do DNA. Em alguns locais, especialmente em DNA repetitivo como telômeros nas extremidades dos cromossomos, centrômeros perto do centro e elementos móveis como LINEs e SINEs, o novo RNA pode se dobrar e hibridizar com o DNA. Isso cria um R-loop: um híbrido RNA–DNA curto emparelhado com uma fita simples de DNA deslocada. Embora R-loops possam ser úteis em doses pequenas e controladas, os persistentes atuam como barreiras para a maquinaria que replica o DNA, levando a cromossomos quebrados, divisão celular defeituosa e instabilidade genômica — características centrais do câncer e de doenças genéticas.
A Proteína Patrulheira de R-Loops
Os pesquisadores mostram que SFPQ, conhecida há muito tempo como fator de ligação a RNA e de splicing, também é um sensor dedicado de R-loops em regiões repetitivas. Em células com níveis reduzidos de SFPQ, a equipe detectou mais R-loops em telômeros, satélites pericentroméricos e retroelementos usando anticorpos específicos para híbridos e mapeamento por sequenciamento. Esses pontos quentes coincidiram com sinais fortes de estresse de replicação e dano ao DNA. Experimentos bioquímicos com SFPQ purificada revelaram o porquê: SFPQ não se liga bem a DNA duplo comum nem a dúplexes RNA–DNA, mas prefere fortemente estruturas de três fios, especialmente R-loops que carregam caudas de RNA expostas semelhantes aos RNAs naturais de repetições. Essa seletividade posiciona SFPQ como um respondededor inicial que reconhece R-loops problemáticos precisamente onde o genoma é mais repetitivo.
Construindo uma Armadura Protetora de Cromatina
Detectar esses nós é apenas parte da história. A equipe descobriu que SFPQ interage fisicamente com DAXX, uma proteína que entrega uma variante especial de histona chamada H3.3 à cromatina. H3.3 ajuda a formar nucleossomos estáveis que silenciam DNA repetitivo e impedem recombinações descontroladas. Experimentos de mapeamento ao longo do genoma mostraram que SFPQ e DAXX frequentemente compartilham locais de ligação em repetições intergênicas e intrônicas, em vez de promotores clássicos de genes. Quando SFPQ foi perdido, DAXX deslocou-se das repetições para regiões regulatórias, e H3.3 deixou de ser depositada de forma eficiente em trechos ricos em repetições, mesmo que os níveis totais de proteína H3.3 não tenham mudado. Como resultado, o molde de cromatina nessas repetições tornou-se mal organizado, permitindo o acúmulo de R-loops e estresse de replicação.
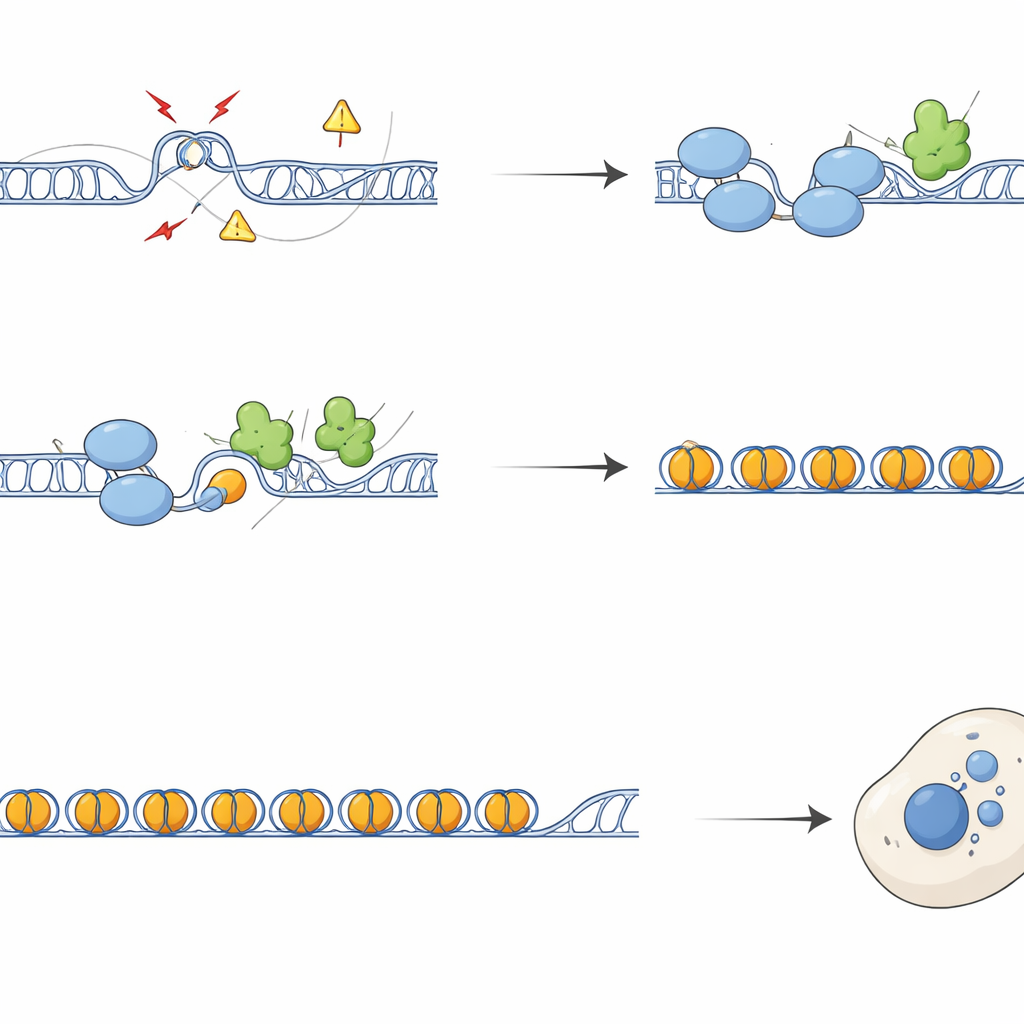
De Cromossomos Quebrados à Imunidade Alarmada
Na ausência de SFPQ, regiões repetitivas acumularam marcadores de dano ao DNA e fatores de reparo, e os cromossomos apresentaram mais quebras e permutas entre fitas irmãs. Durante a divisão celular, esse dano se traduziu em segregação defeituosa, formando pontes de cromatina e micronúcleos — pequenos corpos extras contendo DNA fora do núcleo principal. Esses micronúcleos frequentemente continham sequências teloméricas e centroméricas e foram revestidos por cGAS, um sensor de DNA fora do lugar que ativa a via imune inata cGAS–STING. Células sem SFPQ ou DAXX ativaram genes de interferon e inflamatórios, um efeito que pôde ser amplamente revertido pela superexpressão de RNaseH1, uma enzima que remove R-loops, ou pelo bloqueio de STING. Assim, o excesso de R-loops em repetições alimenta diretamente a sinalização imune por meio da produção de destroços de DNA citoplasmático.
Implicações para o Câncer e Desfechos de Pacientes
Em dados de pacientes com sarcoma, alta expressão de SFPQ correlacionou-se com pior sobrevivência, enquanto uma assinatura gênica refletindo forte ativação da imunidade inata — semelhante à observada quando SFPQ é perdido — esteve ligada a desfechos melhores. Pacientes com baixa expressão de SFPQ, mas alta expressão da assinatura imune, tiveram os melhores resultados, sugerindo que, em tumores, desativar esse eixo protetor nas repetições pode, involuntariamente, expor as células cancerosas ao sistema imunológico. O trabalho delineia uma cadeia mecanicista desde a detecção de R-loops por SFPQ, passando pela proteção da cromatina mediada por DAXX–H3.3, até a prevenção da instabilidade genômica e a atenuação da imunidade inata. Para um público leigo, a mensagem central é que SFPQ age como uma equipe de manutenção do DNA repetitivo: detecta nós perigosos RNA–DNA, chama ajudantes de empacotamento para alisar e blindar essas regiões e, assim, mantém os cromossomos intactos e os alarmes imunes baixos — um equilíbrio que os cânceres podem explorar, mas que futuras terapias poderiam reverter em favor do paciente.
Citação: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Palavras-chave: R-loops, estabilidade genômica, histona H3.3, imunidade inata, sarcoma