Clear Sky Science · he
חלבון SFPQ מכוון ריכוז של היסטון H3.3 ל-R-loops בחזרות של ה-DNA כדי להגן על יציבות הגנום
שומרי החזרות שב-DNA שלנו
חלק גדול מה-DNA שלנו בנוי מרצפים ארוכים וחוזרים שהיו פעם מוזנחים כ"אשפה" גנטית. היום אנחנו יודעים שהאזורים האלה יכולים להתנהג בצורה בעייתית, ולהיווצר בהם קשרים תלת–גדיליים בלתי רגילים שנקראים R-loops, שמעכבים את שכפול ה-DNA ומעשירים נזק. המחקר הזה חושף כיצד חלבון בשם SFPQ סורק את הקטעים החוזרים הללו, מארגן את האריזה שלהם, ובכך שומר בשקט על יציבות הגנום ואף מעצב את האינטראקציה של סוגי סרטן מסוימים עם מערכת החיסון.
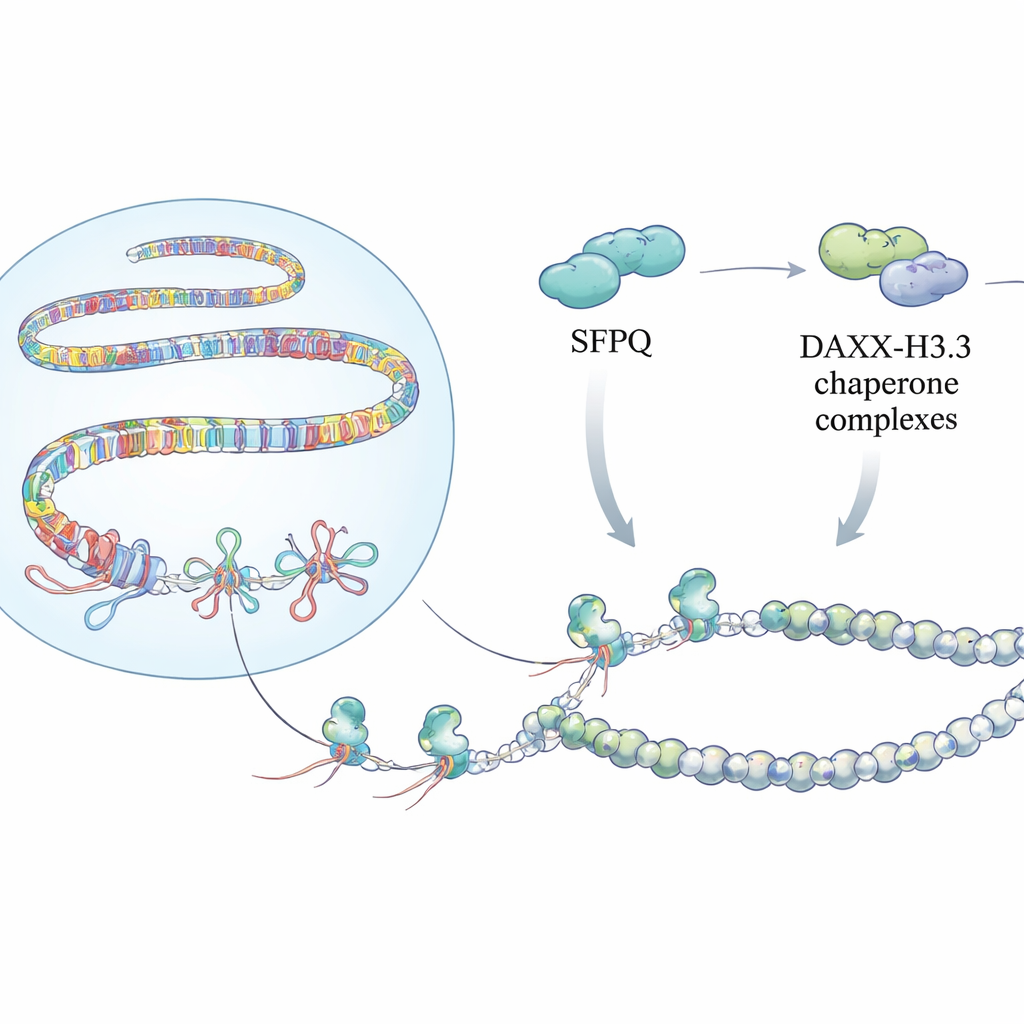
קשרים נסתרים בגנום
כשגֶן נקרא, נוצר העתיק זמני של RNA מה-DNA. במקומות מסוימים, במיוחד ב-DNA חוזר כמו טלומרים בקצוות הכרומוזומים, צנטרומרים בקרבת האזור המרכזי, ואלמנטים ניידים כמו LINE ו-SINE, ה-RNA החדש עלול להתקפל ולהידבק בחזרה ל-DNA. זה יוצר R-loop: היבריד קצר של RNA–DNA שמלווה בגדיל DNA בודד מוסט. בעוד ש-R-loops יכולים להיות מועילים במינונים קטנים ומבוקרים, כאלה שנשארים לאורך זמן פועלים כחסמים עבור מכונת השכפול של ה-DNA, מה שמוביל לשבירת כרומוזומים, חלוקה תאית לקויה ויציבות גנום לקויה — סימנים מובהקים של סרטן ומחלות גנטיות.
חלבון הסיור של ה-R-loop
החוקרים מראים כי SFPQ, שידוע מזה זמן רב כחלבון הקשור לקשירת RNA ולעיבוד חיתוך (splicing), הוא גם חיישן ייעודי של R-loops באזורי חזרה. בתאים שבהם הפחיתו את רמת SFPQ, הצוות זיהה יותר R-loops בטלומרים, בסאטליטים סביב הצנטרומר ובאלמנטים רטרו בעזרת נוגדנים ספציפיים להיברידים ומיפוי מבוסס רצף. נקודות החום הללו התאמו לאותות חזקים של לחץ שכפול ונזק ל-DNA. ניסויים ביוכימיים עם SFPQ מטוהר הסבירו למה: SFPQ לא נקשר היטב ל-DNA דו-גדילי רגיל או לדופלקסים RNA–DNA, אבל מראה העדפה חזקה למבנים תלת–גדיליים, ובמיוחד ל-R-loops שנושאים זנבות RNA חשופים הדומים ל-RNA של חזרות טבעיות. סלקטיביות זו מציבה את SFPQ ככוח תגובה ראשוני שמזהה R-loops בעייתיים בדיוק במקומות שהגנום החוזר רווי בהם.
בנייה של שריון כרומטין מגן
זיהוי הקשרים האלה הוא רק חלק מהסיפור. הצוות גילה כי SFPQ יוצר אינטראקציה פיזית עם DAXX, חלבון שמספק וריאנט היסטוני מיוחד הנקרא H3.3 לתוך הכרומטין. H3.3 מסייע ביצירת נוקלאוזומים יציבים שמדכאים DNA חוזר ומונעים רקומבינציה בלתי מבוקרת. ניסויי מיפוי ברחבי הגנום הראו ש-SFPQ ו-DAXX חולקים לעיתים קרובות אתרי קשירה בחזרות אינטרגניות ואינטרוניות, ולא במקדם גנים קלאסי. כאשר SFPQ איבד את נוכחותו, DAXX נדד מהחזרות לכיוון אזורים רגולטוריים, ו-H3.3 כבר לא הוכנס ביעילות לרצועות עשירות בחזרות, אף כי רמות החלבון הכוללות של H3.3 לא השתנו. כתוצאה מכך, תבנית הכרומטין באותם חזרות הפכה לפחות מאורגנת, מה שאפשר הצטברות של R-loops ולחץ שכפול.
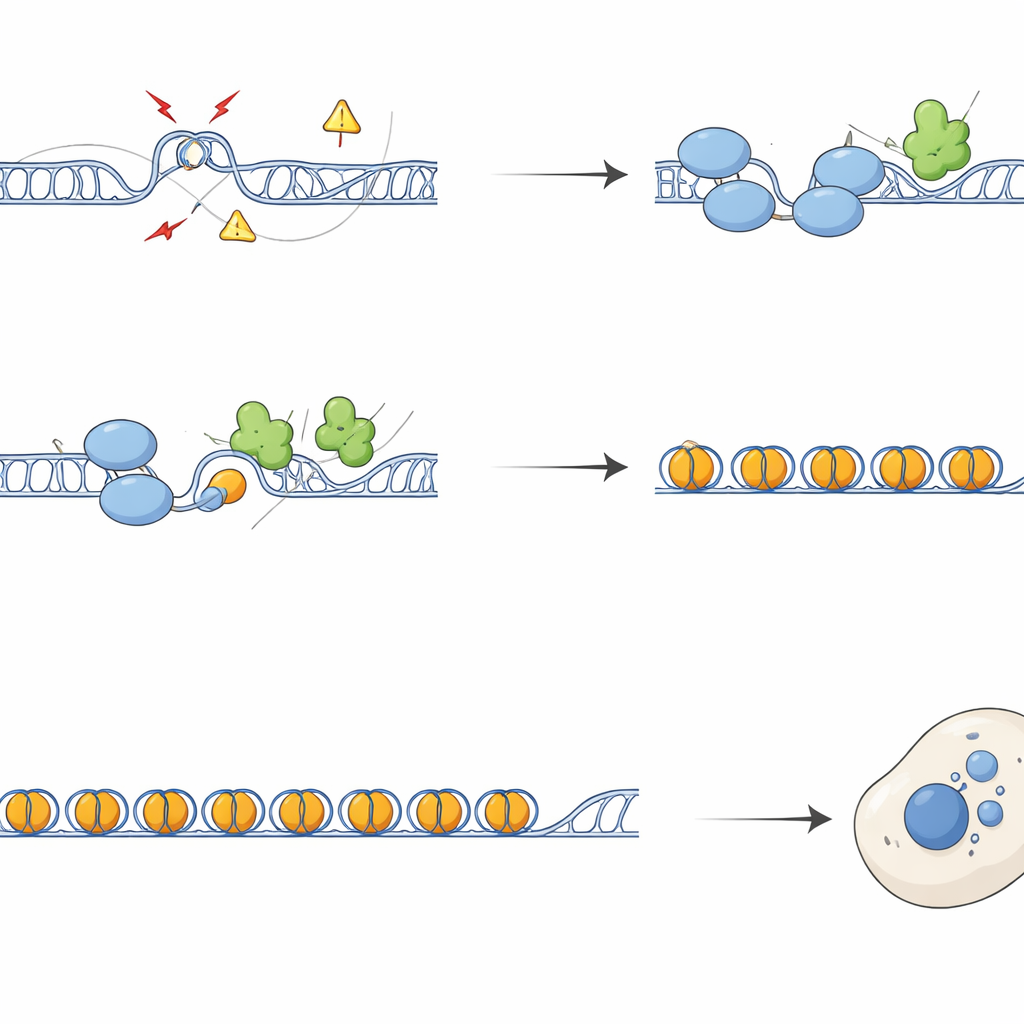
מהכרומוזומים השבורים לחיסון מופעל
בغي absence של SFPQ, אזורים חוזרים הצטברו בסמנים של נזק ל-DNA וגורמי תיקון, והכרומוזומים הראו יותר שברים והחלפות בין גדילים אחיות. במהלך חלוקת התא, נזק זה התבטא בהפרדה לקויה, ביצירת גשרים כרומטיניים ובמיקרו-גרעינים — גופים קטנים נוספים שמכילים DNA מחוץ לגרעין הראשי. מיקרו-גרעינים אלה לעיתים קרובות נשאו רצפים טלומריים וצנטרומריים ולבשו שכבה של cGAS, חיישן DNA במיקום שגוי שמפעיל את מסלול החיסון המולד cGAS–STING. תאים חסרי SFPQ או DAXX הפעילו גנים של אינטרפרון ודלקת, השפעה שניתן היה להפחית במידה רבה על ידי הבעה יתרה של RNaseH1, אנזים שמסיר R-loops, או על ידי חסימת STING. לפיכך, עודפי R-loops בחזרות מזינים ישירות איתות חיסוני דרך יצירת שברי DNA ציטופלזמיים.
השלכות על סרטן ותוצאי מטופלים
בנתוני חולים עם סרקומה, ביטוי גבוה של SFPQ נקשר להישרדות חלשה יותר, בעוד שחתימת גנים המשקפת הפעלה חזקה של המערכת החיסונית המולדת — בדומה למה שנצפה אצל חוסר SFPQ — נקשרה לתוצאים טובים יותר. מטופלים עם SFPQ נמוך אך ביטוי גבוה של חתימת חיסון נהנו מהתוצאות הטובות ביותר, מה שמרמז כי בגידולים, השבתה של ציר המגן הזה בחזרות עשויה באופן בלתי מכוון לחשוף את תאי הסרטן למערכת החיסון. העבודה מציגה שרשרת מכניסטית מאיתור R-loop על ידי SFPQ, דרך הגנה כרומטינית מתווכת על ידי DAXX–H3.3, ועד למניעת יציבות גנום ולהשתקת איתות החיסון המולדת. לקהל הרחב, המסר המרכזי הוא ש-SFPQ מתפקד כצוות תחזוקה עבור ה-DNA החוזר: הוא מזהה קשרי RNA–DNA מסוכנים, מזעיק עוזרי אריזה כדי להחליק ולחמש אזורים אלה, ובכך שומר על שלמות הכרומוזומים ועל השקט של אזעקות החיסון — איזון שסרטנים עשויים לנצל אך שטיפולים עתידיים עשויים להטות בחזרה לטובת המטופל.
ציטוט: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
מילות מפתח: R-loops, יציבות הגנום, היסטון H3.3, חיסון מולד, סרקומה