Clear Sky Science · ar
توجيه SFPQ لترسيب الهيستون H3.3 إلى حلقات R في تكرارات الحمض النووي لحماية استقرار الجينوم
حراس تكرارات حمضنا النووي
جزء كبير من حمضنا النووي يتكون من تسلسلات طويلة متكررة كانت تُعتبر سابقًا «نفاية». نعلم الآن أن هذه المناطق يمكن أن تتصرف بشكل غير منتظم، فتكوّن عُقدًا غير اعتيادية ثلاثية الخيوط تُسمى حلقات R تَعُوق آلية نسخ الحمض النووي وتؤدي إلى تلفه. تكشف هذه الدراسة كيف يقوم بروتين اسمه SFPQ بدور الدورية على هذه المقاطع المتكررة، وينظم تعبئتها، وبذلك يحمي بهدوء استقرار الجينوم وحتى يؤثر على كيفية تفاعل بعض السرطانات مع الجهاز المناعي.
عُقد خافتة في الجينوم
عندما يُقرأ جين، يُنسخ منه نسخة مؤقتة من الرنا. في بعض المواقع، خاصة في الحمض النووي المتكرر مثل التيلوميرات عند أطراف الكروموسومات، والمراكز القريبة من الوسط المعروفة بالمراكز المَركزية (centromeres)، والعناصر المتنقلة مثل LINEs وSINEs، يمكن للرنا الجديد أن يطوى ويهاجم الحمض النووي مكوّنًا هجين رنا–دنا. هذا يكوّن حلقة R: هجين قصير رنا–دنا مصاحبًا لشريط مفروز من دنا مفرد. بينما قد تكون حلقات R مفيدة بجرعات صغيرة ومتحكم بها، فإن استمرارها يشبه الحواجز الآنية لآليات نسخ الحمض النووي، مما يؤدي إلى كروموسومات مكسورة، وانقسام خلوي معطوب، وعدم استقرار جينومي — وهي سمات أساسية للسرطان والأمراض الوراثية.
بروتين دورية حلقات R
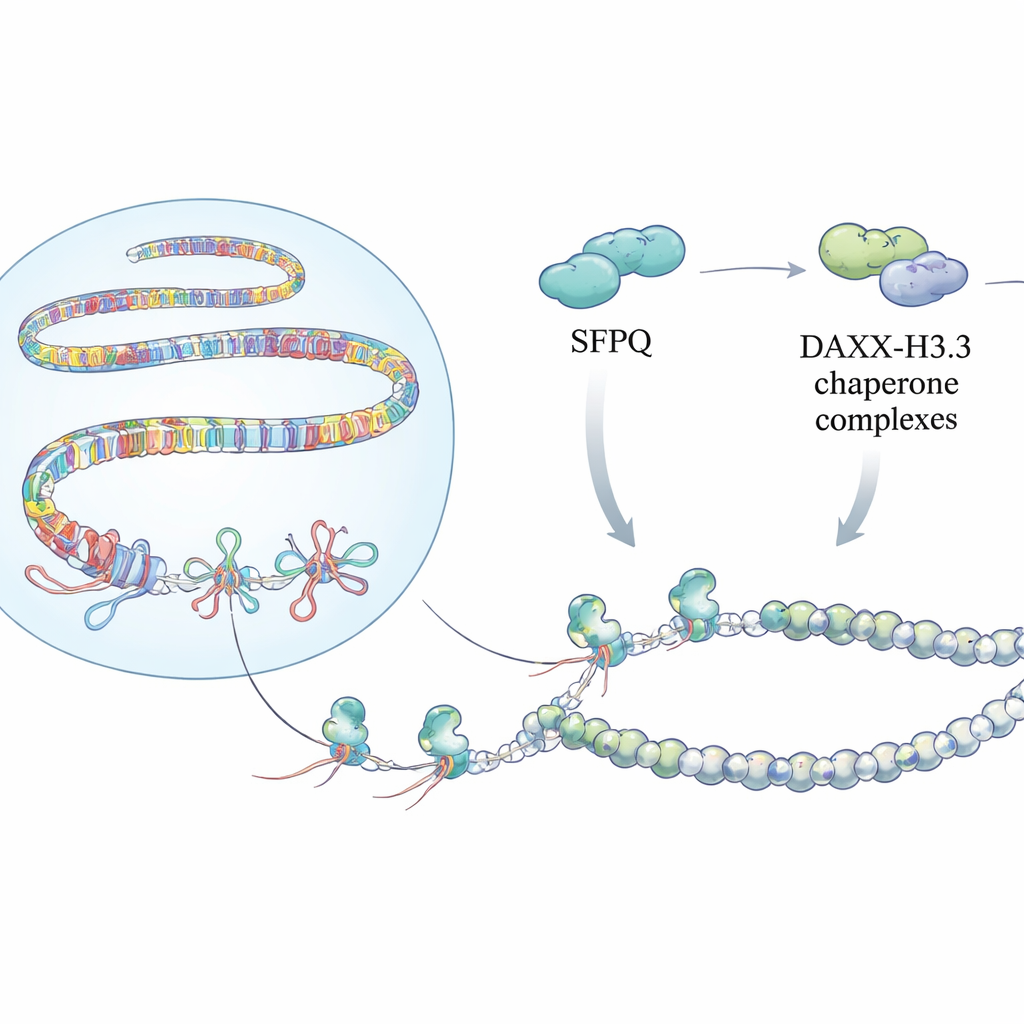
يُظهر الباحثون أن SFPQ، المعروف منذ زمن طويل كبروتين رابط للرنا ومشارك في التطويع (splicing)، هو أيضًا جهاز استشعار مخصص لحلقات R في المناطق المتكررة. في خلايا نُقص فيها SFPQ، رصد الفريق المزيد من حلقات R عبر التيلوميرات والأقمار الصناعية المحيطة بالمركز والعناصر الراجعة بواسطة أجسام مضادة متخصصة للهجائن وبخرائط تسلسلية. توافقت هذه البؤر الساخنة مع إشارات قوية لإجهاد الاستنساخ وتلف الحمض النووي. أظهرت تجارب كيميائية حيوية مع SFPQ المنقى السبب: SFPQ لا يرتبط جيدًا بالحمض النووي ثنائي الشريط العادي أو الهجائن رنا–دنا، لكنه يفضّل بشدة الهياكل ثلاثية الخيوط، وبخاصة حلقات R التي تحمل ذيول رنا مكشوفة تشبه رنات التكرارات الطبيعية. هذا الانتقائية تضع SFPQ كأول مستجيب يتعرف على حلقات R المشكلة تمامًا حيث يكون الجينوم أكثر تكرارًا.
بناء درع كروماتيني واقٍ
اكتشاف هذه العُقد هو جزء من القصة فقط. اكتشف الفريق أن SFPQ يتفاعل فعليًا مع DAXX، بروتين يُسلم نسخة هيستون خاصة تُدعى H3.3 إلى الكروماتين. يساعد H3.3 على تشكيل نواكلوزومات مستقرة تُسكت الحمض النووي المتكرر وتمنع إعادة التركيب غير المنضبطة. أظهرت تجارب الترابط عبر الجينوم أن SFPQ وDAXX يتشاركان كثيرًا مواقع الارتباط في التكرارات بين الجينات وداخل الإنترونات، بدلاً من محرّكات الجينات التقليدية. عندما فُقد SFPQ، تحول DAXX بعيدًا عن التكرارات نحو المناطق المنظمة، ولم يعد H3.3 يُرسَل بفعالية إلى المقاطع الغنية بالتكرارات، رغم أن مستويات بروتين H3.3 العامة لم تتغير. نتيجة لذلك، أصبح قالب الكروماتين في هذه التكرارات سيئ التنظيم، مما سمح بتراكم حلقات R وإجهاد الاستنساخ.
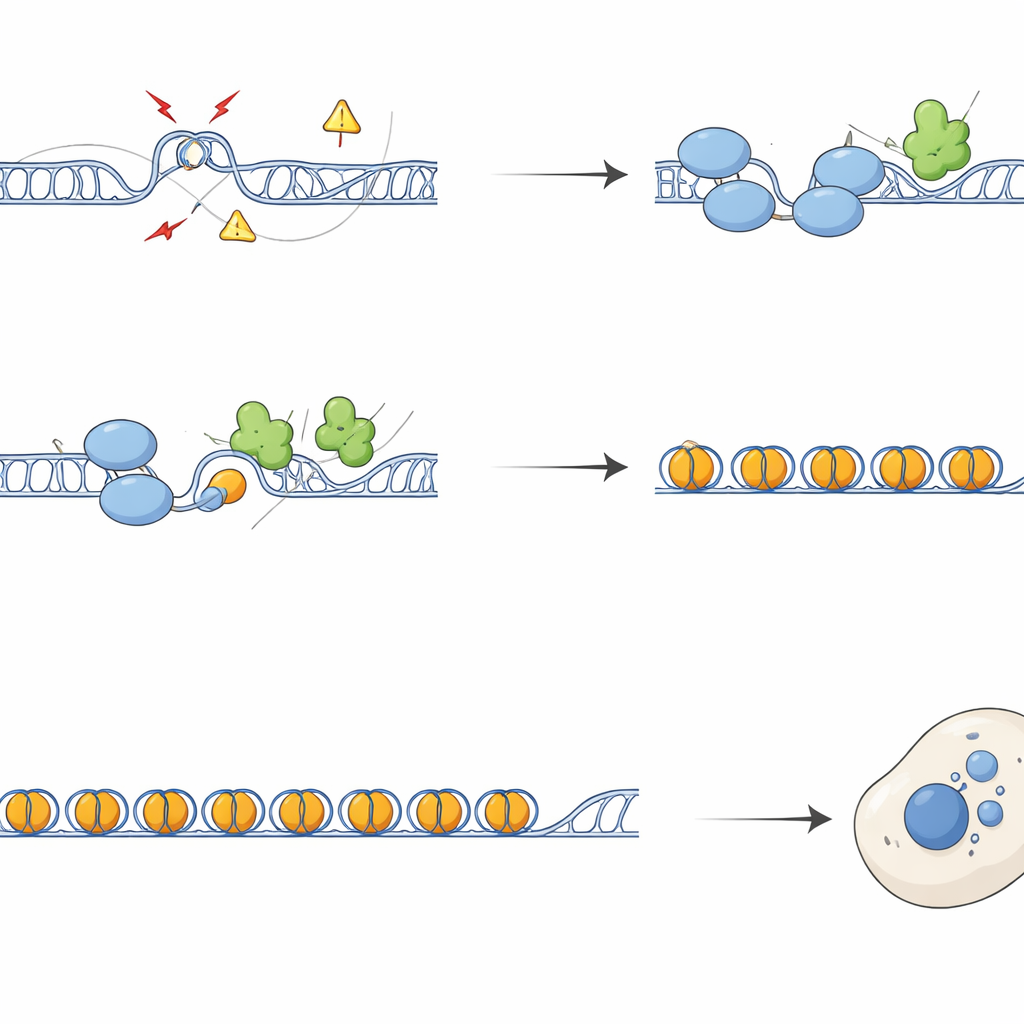
من كروموسومات مكسورة إلى تنبيه مناعي
بدون SFPQ، تراكمت في المناطق المتكررة علامات تلف الحمض النووي وعوامل الإصلاح، وأظهرت الكروموسومات مزيدًا من الكسور والتبادلات بين الخيوط الشقيقة. أثناء انقسام الخلايا، تُرجم هذا التلف إلى فصل معيب، مكوّنًا جسورًا كروماتينية ونوى صغيرة (micronuclei) — أجسام صغيرة إضافية تحوي دنا خارج النواة الرئيسية. غالبًا ما حملت هذه النوى الصغيرة تسلسلات تيلومرية ومركزية وغطّت بمستشعر cGAS، وهو كاشف للدنا الموضع في غير محله ويشعل مسار المناعة الفطرية cGAS–STING. فعلت الخلايا التي تفتقر إلى SFPQ أو DAXX جينات الإنترفيرون والالتهاب، وهو تأثير يمكن عكسه إلى حد كبير بزيادة تعبير RNaseH1، إنزيم يزيل حلقات R، أو بحجب STING. هكذا، تغذي حلقات R الزائدة في التكرارات الإشارات المناعية مباشرة عبر إنتاج حطام دنا خلوي سائبة في السيتوبلازم.
تداعيات للسرطان ونتائج المرضى
في بيانات مرضى الساركومة، ارتبط التعبير العالي لـ SFPQ ببقاء أسوأ، بينما ارتبطت بصمة جينية تعكس تنشيطًا قويًا للمناعة الفطرية — مشابهة لتلك المرصودة عند فقدان SFPQ — بنتائج أفضل. أظهر المرضى ذوو SFPQ المنخفض ولكن بتعبير بصمة مناعية مرتفع أفضل نتائج، ما يوحي بأنه في الأورام قد يؤدي تعطيل هذا المحور الوقائي في التكرارات إلى كشف الخلايا السرطانية أمام الجهاز المناعي. توضح الدراسة سلسلة آلية بدءًا من استشعار حلقات R بواسطة SFPQ، إلى حماية الكروماتين بوساطة DAXX–H3.3، إلى منع عدم استقرار الجينوم وكتم الاستجابة المناعية الفطرية. للقراء غير المتخصصين، الرسالة الأساسية أن SFPQ يعمل كفريق صيانة للتكرارات: يكتشف عقد الرنا–دنا الخطرة، يستدعي مساعدي التعبئة لتنعيم وتدريع هذه المناطق، ومن ثم يحافظ على سلامة الكروموسومات ويسكت إنذارات المناعة — توازن قد تستغله السرطانات لكن يمكن للعلاجات المستقبلية أن تعيده لصالح المريض.
الاستشهاد: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
الكلمات المفتاحية: حلقة R, استقرار الجينوم, الهيستون H3.3, المناعة الفطرية, ساركومة