Clear Sky Science · fr
La protéine SFPQ dirige le dépôt de l’histone H3.3 vers les R-boucles des séquences répétées pour protéger la stabilité du génome
Gardiens de nos séquences répétées
Une grande partie de notre ADN est constituée de longues séquences répétées autrefois qualifiées de « déchets ». Nous savons aujourd’hui que ces régions peuvent se dérégler et former des nœuds inhabituels à trois brins appelés R-boucles, qui bloquent la réplication de l’ADN et déclenchent des lésions. Cette étude révèle comment une protéine nommée SFPQ patrouille ces zones répétitives, organise leur empaquetage, et protège ainsi discrètement la stabilité du génome tout en influençant la manière dont certains cancers interagissent avec le système immunitaire.
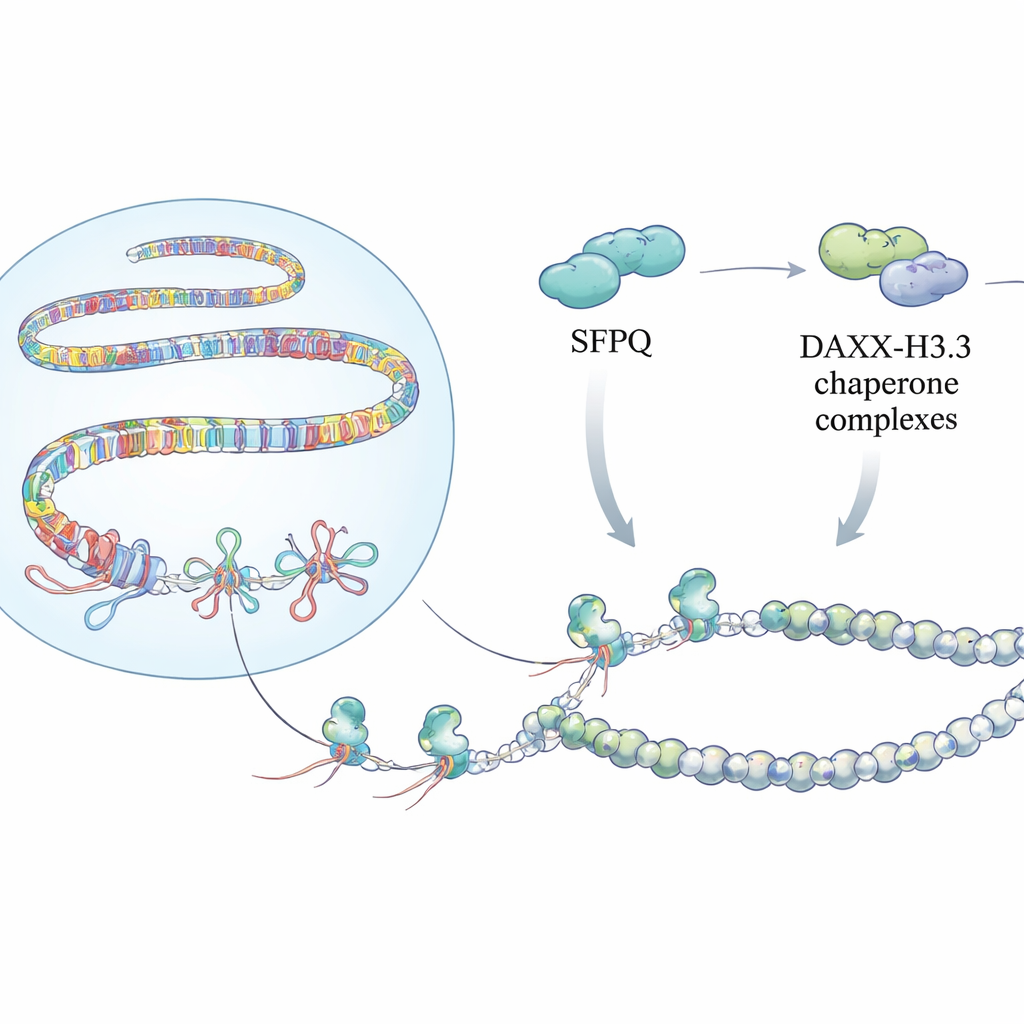
Nœuds cachés dans le génome
Lorsqu’un gène est lu, une copie d’ARN transitoire est synthétisée à partir de l’ADN. En certains endroits, notamment dans l’ADN répétitif comme les télomères aux extrémités des chromosomes, les centromères près du centre, et les éléments mobiles tels que les LINE et SINE, l’ARN nouvellement formé peut se replier et s’hybrider avec l’ADN. Cela crée une R-boucle : un hybride ARN–ADN associé à un brin d’ADN simple déplacé. Si les R-boucles sont utiles en petites quantités contrôlées, celles qui persistent forment des obstacles pour les machines de réplication, entraînant des chromosomes fracturés, des divisions cellulaires défectueuses et une instabilité du génome — des caractéristiques majeures du cancer et des maladies génétiques.
La protéine patrouilleuse des R-boucles
Les chercheurs montrent que SFPQ, connue depuis longtemps comme une protéine liant l’ARN et un facteur d’épissage, est également un détecteur dédié des R-boucles dans les régions répétitives. Dans des cellules où SFPQ était réduit, l’équipe a détecté davantage de R-boucles aux télomères, aux satellites péri-centromériques et aux rétroéléments grâce à des anticorps spécifiques des hybrides et à des cartographies par séquençage. Ces points chauds coïncidaient avec des signes marqués de stress de réplication et de dommages à l’ADN. Des expériences biochimiques avec SFPQ purifié expliquent pourquoi : SFPQ ne se lie pas bien à l’ADN double brin ordinaire ni aux duplex ARN–ADN, mais préfère fortement les structures à trois brins, en particulier les R-boucles portant des queues d’ARN exposées similaires aux ARN des répétitions naturelles. Cette sélectivité place SFPQ comme un premier intervenant reconnaissant précisément les R-boucles problématiques là où le génome est le plus répétitif.
Assembler une armure chromatinienne protectrice
Détecter ces nœuds ne suffit pas. L’équipe a découvert que SFPQ interagit physiquement avec DAXX, une protéine qui apporte une variante d’histone spéciale appelée H3.3 dans la chromatine. H3.3 contribue à former des nucléosomes stables qui silencient l’ADN répétitif et empêchent des recombinaisons incontrôlées. Des cartographies génomiques ont montré que SFPQ et DAXX partagent fréquemment des sites de liaison dans les répétitions intergéniques et introniques, plutôt qu’aux promoteurs géniques classiques. Lors de la perte de SFPQ, DAXX s’est déplacé des répétitions vers des régions régulatrices, et H3.3 n’a plus été déposé efficacement sur les régions riches en répétitions, même si les niveaux globaux de H3.3 restaient inchangés. En conséquence, le modèle de chromatine de ces répétitions devenait mal organisé, permettant l’accumulation de R-boucles et du stress de réplication.
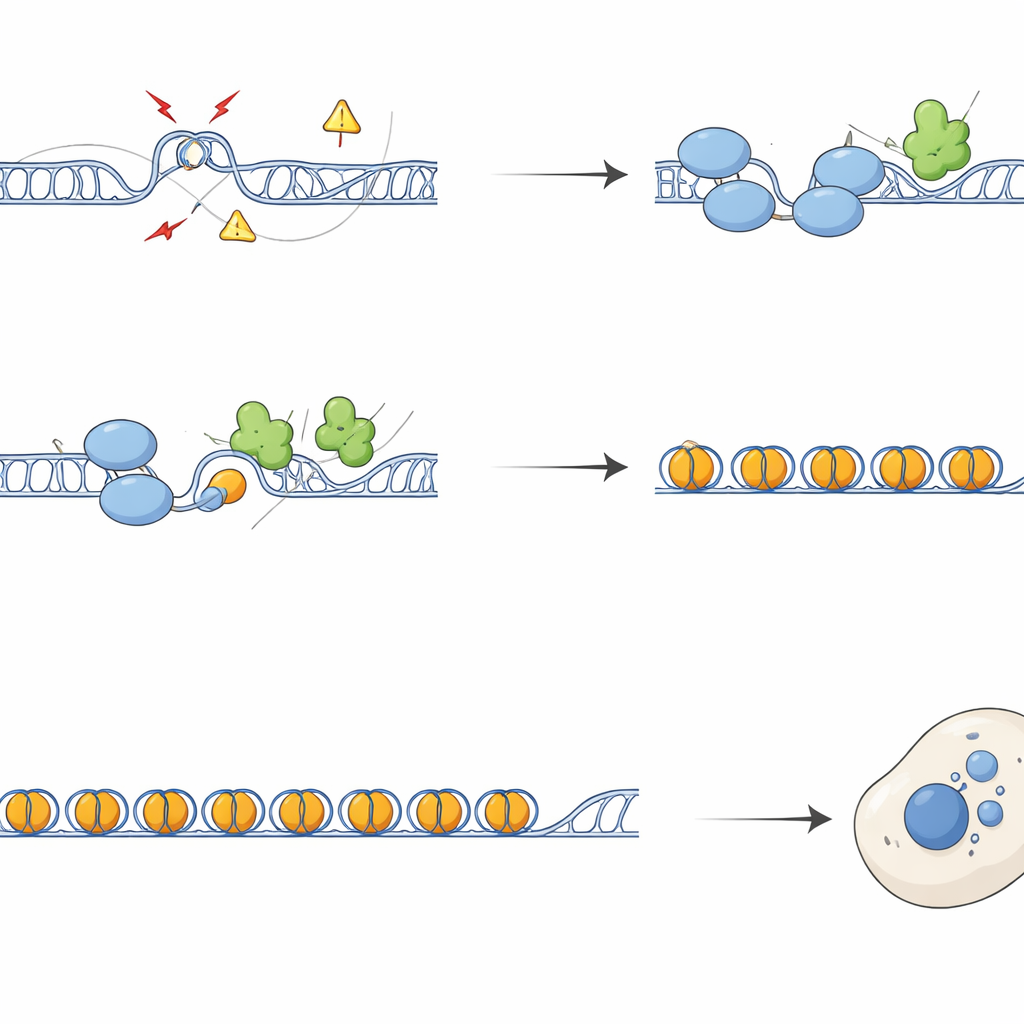
Des chromosomes fracturés à une immunité déclenchée
En l’absence de SFPQ, les régions répétées accumulaient des marqueurs de dommages à l’ADN et des facteurs de réparation, et les chromosomes présentaient davantage de cassures et d’échanges entre chromatides sœurs. Lors de la division cellulaire, ces lésions se traduisaient par une ségrégation défectueuse, formant des ponts de chromatine et des micronoyaux — de petits corps contenant de l’ADN en dehors du noyau principal. Ces micronoyaux contenaient fréquemment des séquences télomériques et centromériques et étaient recouverts par cGAS, un détecteur d’ADN déplacé qui active la voie immunitaire innée cGAS–STING. Les cellules dépourvues de SFPQ ou de DAXX activeaient des gènes d’interféron et d’inflammation, un effet largement réversible par la surexpression de RNaseH1, une enzyme qui élimine les R-boucles, ou par le blocage de STING. Ainsi, l’excès de R-boucles dans les répétitions alimente directement la signalisation immunitaire via la production de débris d’ADN cytoplasmiques.
Implications pour le cancer et le pronostic des patients
Dans les données de patients atteints de sarcome, une forte expression de SFPQ corrélait avec une survie plus mauvaise, tandis qu’un profil génique reflétant une forte activation de l’immunité innée — semblable à celui observé lors de la perte de SFPQ — était associé à de meilleurs résultats. Les patients présentant une faible expression de SFPQ mais une signature immunitaire élevée étaient ceux qui s’en sortaient le mieux, ce qui suggère que, dans les tumeurs, la désactivation de cet axe protecteur au niveau des répétitions peut involontairement exposer les cellules cancéreuses au système immunitaire. Le travail décrit une chaîne mécanistique allant de la détection des R-boucles par SFPQ, au système de protection chromatinienne DAXX–H3.3, en passant par la prévention de l’instabilité génomique et la modulation de l’immunité innée. Pour un public non spécialiste, le message essentiel est que SFPQ agit comme une équipe de maintenance des ADN répétitifs : elle détecte les nœuds dangereux ARN–ADN, fait intervenir des agents d’empaquetage pour lisser et renforcer ces régions, et maintient ainsi l’intégrité des chromosomes tout en calmant les alarmes immunitaires — un équilibre que les cancers peuvent exploiter mais que de futures thérapies pourraient potentiellement renverser en faveur du patient.
Citation: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Mots-clés: R-boucles, stabilité du génome, histone H3.3, immunité innée, sarcome