Clear Sky Science · sv
SFPQ styr depositionen av histon H3.3 till R-loopar i DNA-repetitioner för att skydda genomets stabilitet
Våra DNA-repetitioners väktare
En stor del av vårt DNA består av långa, upprepade sekvenser som tidigare avfärdades som ”skräp”. Vi vet nu att dessa regioner kan ställa till problem genom att bilda ovanliga tresträngade knutar kallade R-loopar som hämmar DNA-replikation och utlöser skador. Denna studie visar hur ett protein vid namn SFPQ patrullerar dessa repetitiva partier, organiserar deras paketering och därigenom tyst skyddar genomets stabilitet — och till och med påverkar hur vissa cancerformer interagerar med immunsystemet.
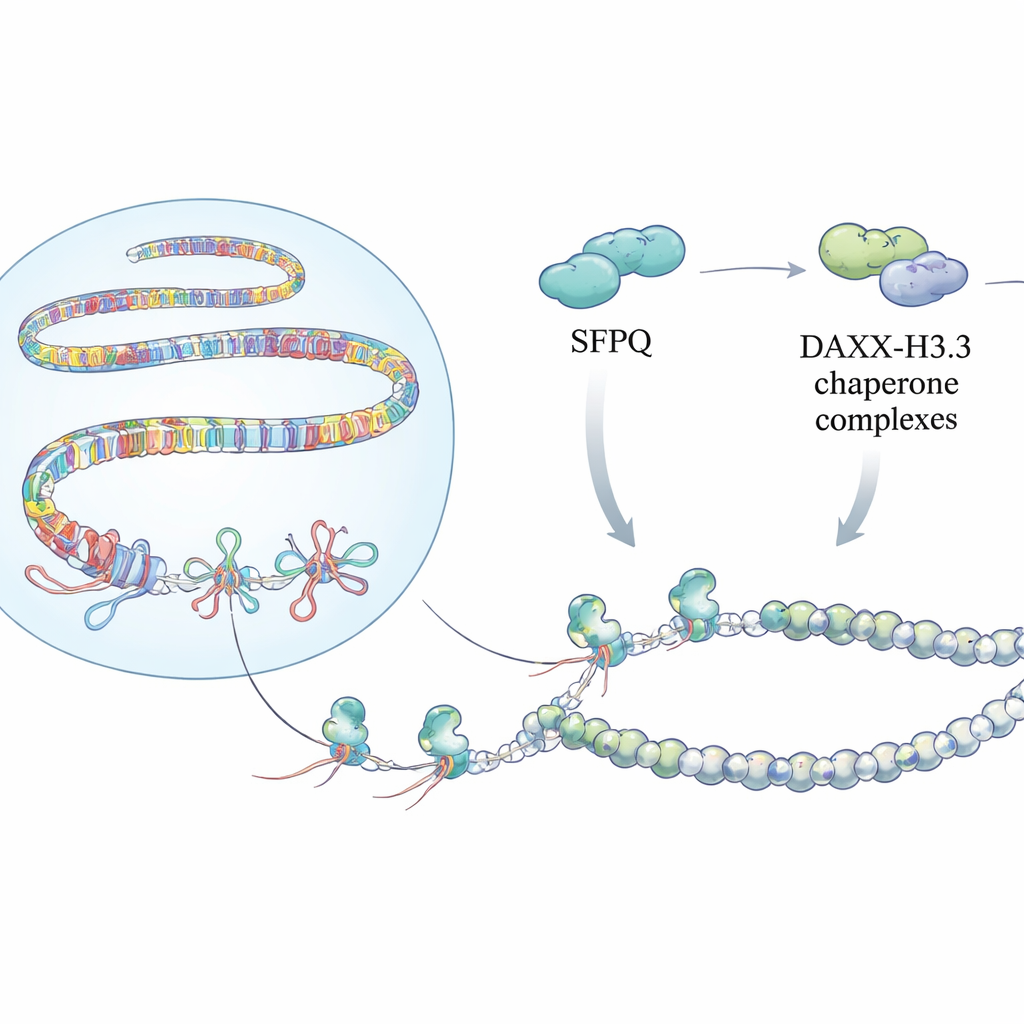
Dolda knutar i genomet
När en gen avläses bildas en temporär RNA-kopia av DNA. På vissa ställen, särskilt i repetitivt DNA som telomerer i kromosomändarna, centromerer nära mitten och mobila element som LINEs och SINEs, kan den nysyntetiserade RNA-tråden vika tillbaka och hybridisera med DNA. Det skapar en R-loop: ett kort RNA–DNA-hybridpar med en förskjuten enkelsträngad DNA-tråd. Medan R-loopar kan vara nyttiga i små, kontrollerade mängder, fungerar ihärdiga R-loopar som vägspärrar för replikeringsmaskineriet, vilket leder till brutna kromosomer, felaktig celldelning och genomisk instabilitet — centrala kännetecken vid cancer och genetiska sjukdomar.
R-loop-patrullproteinet
Forskarna visar att SFPQ, länge känt som ett RNA-bindande och splitsningsfaktor, också är en dedikerad sensor av R-loopar i repetitiva regioner. I celler där SFPQ minskats upptäckte teamet fler R-loopar över telomerer, peri-centromeriska satelliter och retroelement med hjälp av hybrid-specifika antikroppar och sekvenseringsbaserad kartläggning. Dessa hotspots sammanföll med starka signaler för replikationsstress och DNA-skada. Biokemiska experiment med renat SFPQ förklarade varför: SFPQ binder inte vanligt dubbelsträngat DNA eller RNA–DNA-duplex särskilt väl, men har stark preferens för tresträngade strukturer, framför allt R-loopar som bär blottade RNA-svansar liknande naturliga repeat-RNA. Denna selektivitet placerar SFPQ som en första insatsgrupp som känner igen problematiska R-loopar just där genomet är mest repetitivt.
Bygga ett skyddande kromatinpansar
Att upptäcka dessa knutar är bara en del av historien. Teamet upptäckte att SFPQ fysiskt interagerar med DAXX, ett protein som levererar en speciell histonavariant kallad H3.3 till kromatinet. H3.3 hjälper till att bilda stabila nukleosomer som tystar repetitivt DNA och förhindrar okontrollerad rekombination. Kartläggning över genomet visade att SFPQ och DAXX ofta delar bindningsställen i intergeniska och introniska repetitioner, snarare än vid klassiska genpromotorer. När SFPQ förlorades försköts DAXX bort från repetitioner mot regulatoriska regioner, och H3.3 avsattes inte längre effektivt vid repeat‑rika partier, trots att de totala H3.3-proteinnivåerna var oförändrade. Som ett resultat blev kromatinmallen i dessa repetitioner dåligt organiserad, vilket tillät att R-loopar och replikationsstress byggdes upp.
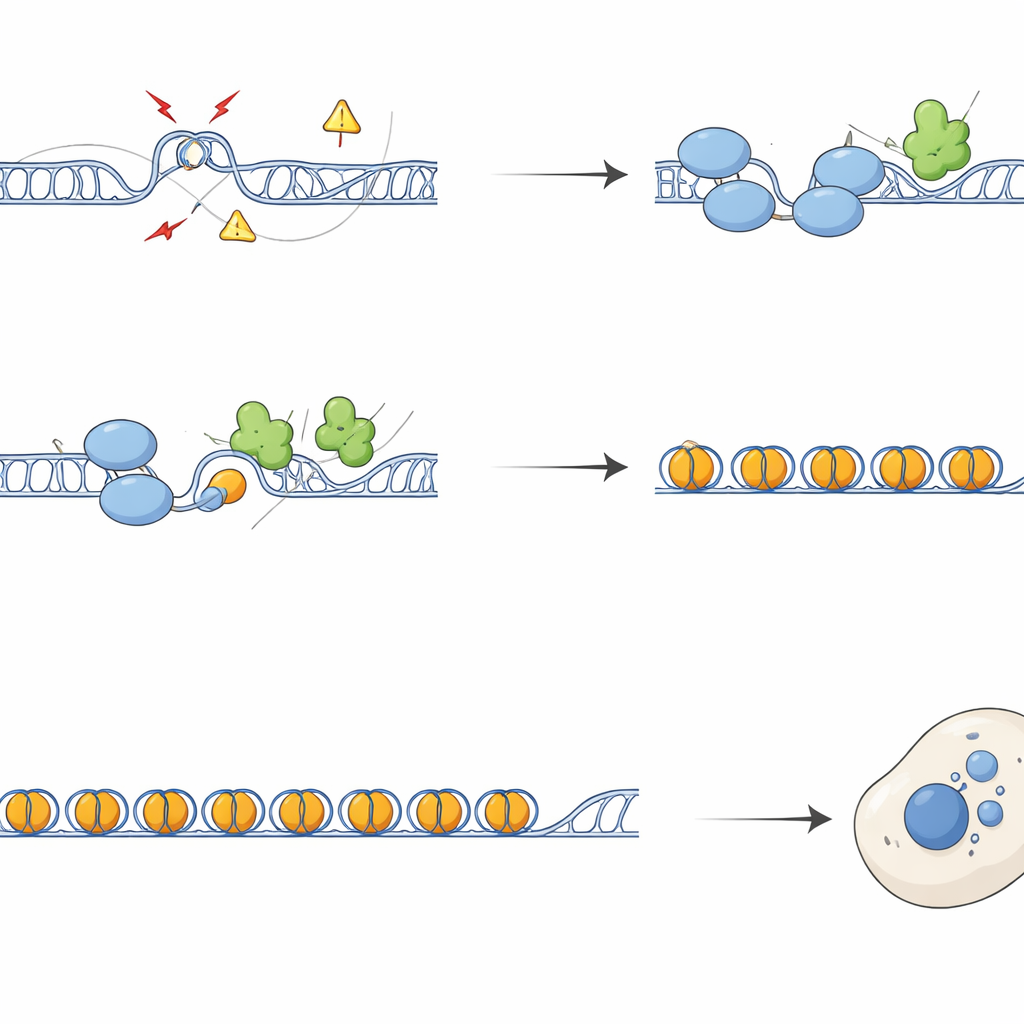
Från brutna kromosomer till ett larmat immunsystem
Utan SFPQ ackumulerade repetitiva regioner DNA-skademarkörer och reparationsfaktorer, och kromosomer visade fler brott och utbyten mellan systersträngar. Under celldelning gav detta upphov till defekt segregation och bildning av kromatinbroar och mikronuklei — små extra DNA-innehållande kroppar utanför huvudkärnan. Dessa mikronuklei bar ofta telomeriska och centromeriska sekvenser och var bestrukna med cGAS, en sensor av felplacerat DNA som aktiverar den medfödda cGAS–STING‑vägen. Celler som saknade SFPQ eller DAXX aktiverade interferon- och inflammatoriska gener, en effekt som till stor del kunde återställas genom överuttryck av RNaseH1, ett enzym som tar bort R-loopar, eller genom blockad av STING. Således föder överskott av R-loopar i repetitioner direkt immunaktivering via produktion av cytoplasmatiskt DNA-avfall.
Konsekvenser för cancer och patientutfall
I data från sarkompatienter korrelerade hög SFPQ‑uttryck med sämre överlevnad, medan en gensekvens som speglar stark aktivering av medfödd immunitet — liknande den som ses vid förlust av SFPQ — var kopplad till bättre utfall. Patienter med låg SFPQ men hög immun-signatur hade bäst prognos, vilket antyder att tumörer som inaktiverar denna skyddande axel i repetitioner av misstag kan blottlägga cancerceller för immunsystemet. Arbetet beskriver en mekanistisk kedja från R-loop‑sensing av SFPQ, till DAXX–H3.3‑medierat kromatinskydd, till förebyggande av genominstabilitet och dämpning av medfödd immunitet. För en allmän publik är kärnbudskapet att SFPQ fungerar som ett underhållsteam för repetitivt DNA: det upptäcker farliga RNA–DNA‑knutar, kallar in paketeringshjälpare för att jämna ut och pansra dessa regioner, och håller därigenom kromosomer intakta och immunsignaler tysta — en balans som cancer kan utnyttja men som framtida terapier potentiellt kan återställa till patientens fördel.
Citering: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Nyckelord: R-loopar, genomstabilitet, histon H3.3, medfödd immunitet, sarkom