Clear Sky Science · it
SFPQ indirizza il deposito dell’istone H3.3 sugli R-loop nei ripetuti del DNA per proteggere la stabilità del genoma
Guardiani dei nostri ripetuti del DNA
Gran parte del nostro DNA è costituita da lunghe sequenze ripetute un tempo bollate come “spazzatura”. Oggi sappiamo che queste regioni possono comportarsi in modo anomalo, formando nodi insoliti a tre filamenti chiamati R-loop che ostacolano la replicazione del DNA e scatenano danni. Questo studio rivela come una proteina chiamata SFPQ pattugli questi tratti ripetitivi, organizzi il loro impacchettamento e, così facendo, protegga silenziosamente la stabilità del genoma e persino moduli il modo in cui alcuni tumori interagiscono con il sistema immunitario.
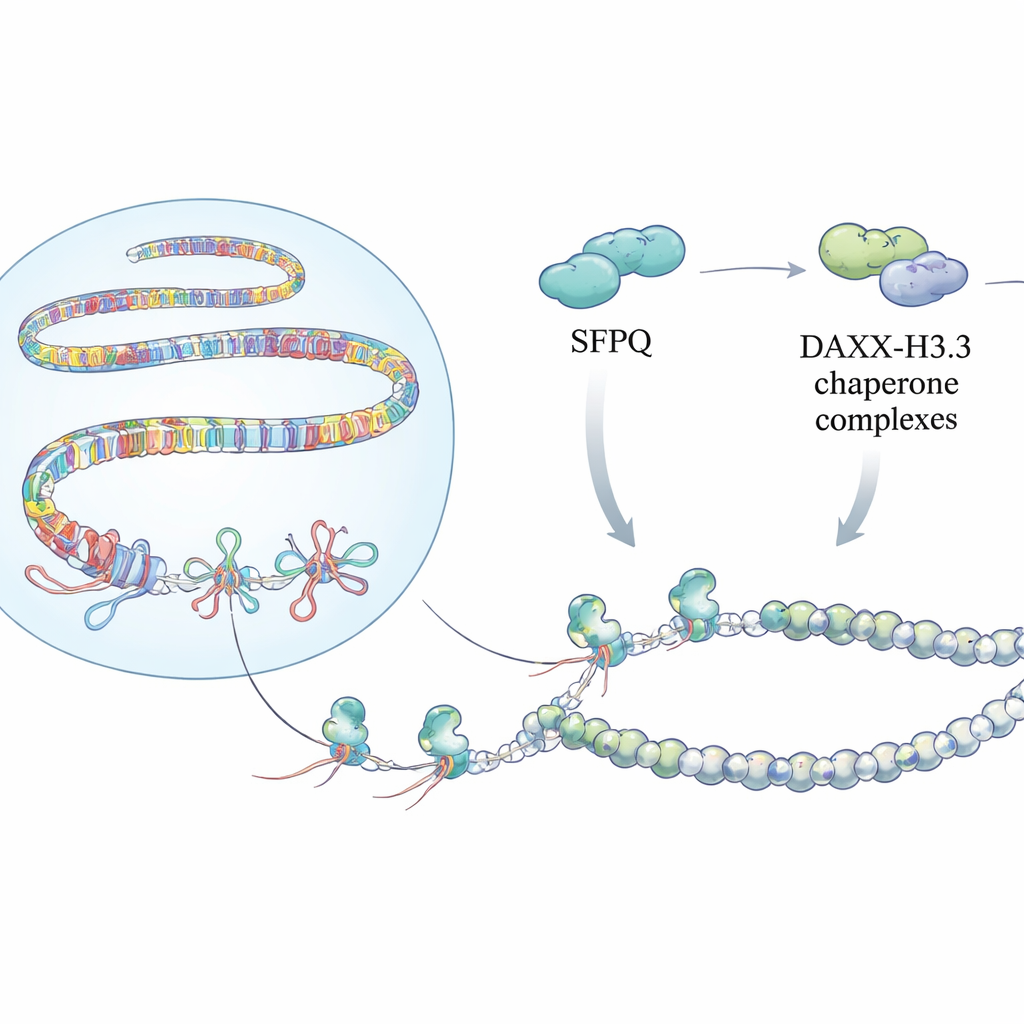
Nodi nascosti nel genoma
Quando un gene viene letto, dal DNA viene prodotto una copia temporanea di RNA. In alcuni punti, specialmente nel DNA ripetuto come i telomeri alle estremità dei cromosomi, i centromeri vicino al centro e gli elementi mobili come LINE e SINE, il nuovo RNA può ripiegarsi e ibridare il DNA. Si crea così un R-loop: un breve ibrido RNA–DNA affiancato da un filamento di DNA singolo spostato. Sebbene gli R-loop possano essere utili a dosi piccole e controllate, quelli persistenti agiscono come blocchi per la macchina che copia il DNA, portando a cromosomi rotti, divisione cellulare defectuosa e instabilità del genoma—caratteristiche chiave del cancro e delle malattie genetiche.
La proteina pattuglia degli R-loop
I ricercatori mostrano che SFPQ, nota da tempo come proteina legante RNA e fattore di splicing, è anche un sensore dedicato degli R-loop nelle regioni ripetute. Nelle cellule in cui SFPQ era ridotta, il gruppo ha rilevato più R-loop su telomeri, satelliti peri-centromerici e retroelementi usando anticorpi specifici per gli ibridi e mappature basate sul sequenziamento. Questi punti caldi coincidevano con forti segnali di stress di replicazione e danno al DNA. Esperimenti biochimici con SFPQ purificata hanno spiegato il motivo: SFPQ non lega bene il normale DNA a doppio filamento né i duplex RNA–DNA, ma preferisce fortemente strutture a tre filamenti, in particolare R-loop che presentano code di RNA esposte simili agli RNA naturali dei ripetuti. Questa selettività pone SFPQ come primo intervento che riconosce gli R-loop problematici proprio dove il genoma è più ripetitivo.
Costruire un’armatura cromatina protettiva
Rilevare questi nodi è solo una parte della storia. Il team ha scoperto che SFPQ interagisce fisicamente con DAXX, una proteina che consegna una variante speciale dell’istone chiamata H3.3 nella cromatina. H3.3 contribuisce a formare nucleosomi stabili che silenziano il DNA ripetuto e prevengono ricombinazioni incontrollate. Esperimenti di mappatura sul genoma hanno mostrato che SFPQ e DAXX condividono frequentemente siti di legame in ripetuti intergenici e intronici, piuttosto che nei classici promotori genici. Quando SFPQ veniva perso, DAXX si spostava lontano dai ripetuti verso regioni regolatorie, e H3.3 non veniva più depositata efficacemente sugli allunghi ricchi di ripetizioni, nonostante i livelli complessivi di proteina H3.3 restassero invariati. Di conseguenza, il modello cromatinico in queste regioni diventava disorganizzato, permettendo l’accumulo di R-loop e stress di replicazione.
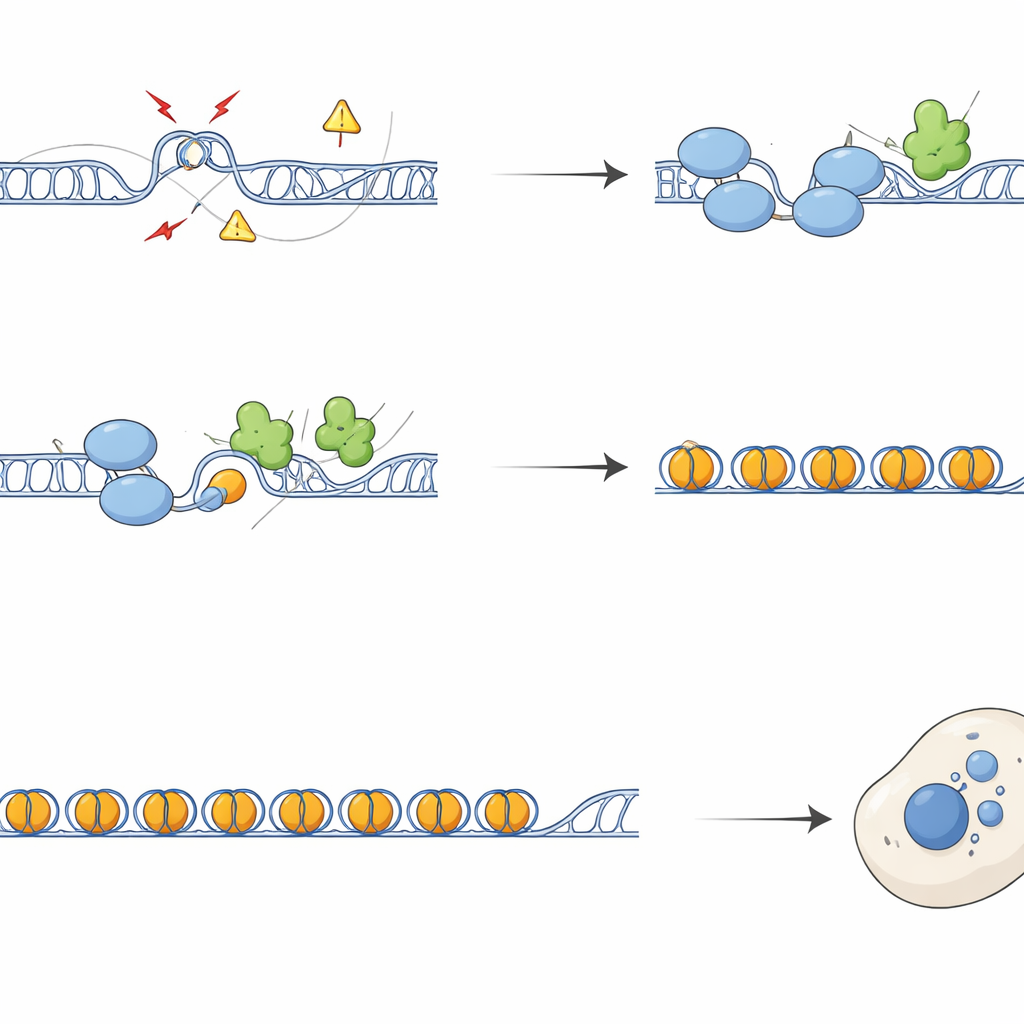
Da cromosomi rotti a immunità allertata
Senza SFPQ, le regioni ripetute accumulavano marcatori di danno al DNA e fattori di riparazione, e i cromosomi mostravano più rotture e scambi tra filamenti sorelle. Durante la divisione cellulare, questo danno si traduceva in segregazione difettosa, formando ponti di cromatina e micronuclei—minuscoli corpi extra contenenti DNA al di fuori del nucleo principale. Questi micronuclei spesso contenevano sequenze telomeriche e centromeriche e risultavano rivestiti da cGAS, un sensore del DNA spostato che attiva la via immunitaria innata cGAS–STING. Le cellule prive di SFPQ o DAXX attivavano geni interferonici e infiammatori, un effetto che poteva essere in larga misura invertito sovraesprimendo RNaseH1, un enzima che rimuove gli R-loop, o bloccando STING. Dunque, l’eccesso di R-loop nei ripetuti alimenta direttamente la segnalazione immunitaria tramite la produzione di detriti di DNA citoplasmatico.
Implicazioni per il cancro e gli esiti nei pazienti
Nei dati di pazienti con sarcoma, l’elevata espressione di SFPQ si associava a una sopravvivenza peggiore, mentre una firma genica che rifletteva una forte attivazione dell’immunità innata—simile a quella osservata quando SFPQ è assente—era legata a risultati migliori. I pazienti con bassa espressione di SFPQ ma alta espressione della firma immunitaria ottenevano i risultati migliori, suggerendo che, nei tumori, disattivare quest’asse protettivo sui ripetuti può involontariamente esporre le cellule cancerose al sistema immunitario. Il lavoro delinea una catena meccanicistica dal riconoscimento degli R-loop da parte di SFPQ, alla protezione della cromatina mediata da DAXX–H3.3, alla prevenzione dell’instabilità genomica e all’attenuazione dell’immunità innata. Per un pubblico non specialistico, il messaggio centrale è che SFPQ agisce come una squadra di manutenzione per il DNA ripetuto: rileva pericolosi nodi RNA–DNA, richiama aiutanti per l’impacchettamento per lisciare e proteggere queste regioni e, così facendo, mantiene i cromosomi integri e gli allarmi immunitari silenziati—un equilibrio che i tumori possono sfruttare ma che terapie future potrebbero ribaltare a vantaggio del paziente.
Citazione: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Parole chiave: R-loop, stabilità del genoma, istone H3.3, immunità innata, sarcoma