Clear Sky Science · nl
SFPQ dirigeert depositie van histon H3.3 naar R-lussen in DNA-repeats om de genomische stabiliteit te beschermen
Bewakers van onze DNA-repeats
Een groot deel van ons DNA bestaat uit lange, herhaalde sequenties die ooit als “junk” werden bestempeld. We weten nu dat deze regio’s zich kunnen misdragen en ongebruikelijke driedubbele knopen vormen, R-lussen genoemd, die het kopiëren van DNA kunnen doen vastlopen en schade veroorzaken. Deze studie onthult hoe een eiwit genaamd SFPQ deze repetitieve stukken patrouilleert, hun verpakking regelt en daarmee stilletjes de genomische stabiliteit beschermt en zelfs beïnvloedt hoe bepaalde kankers met het immuunsysteem omgaan.
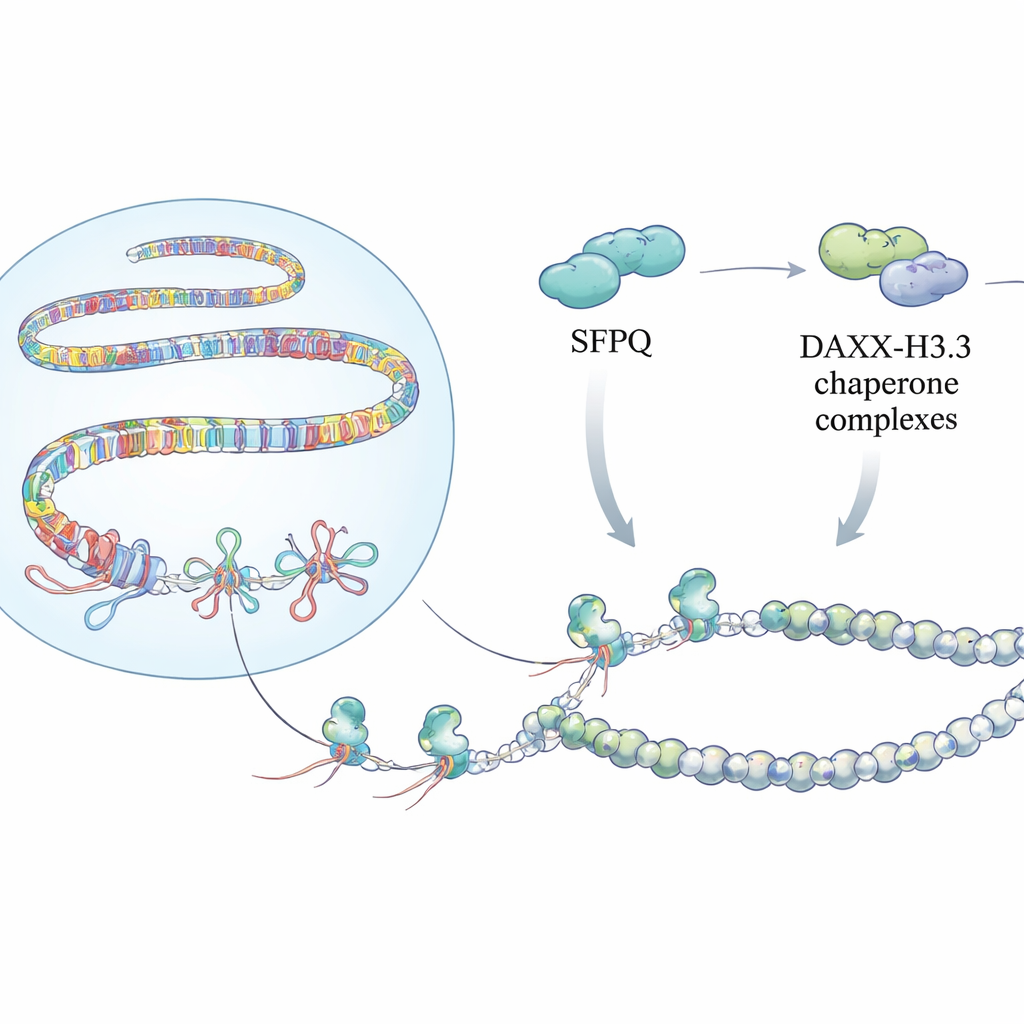
Verborgen knopen in het genoom
Als een gen wordt afgelezen, wordt tijdelijk een RNA-kopie van het DNA gemaakt. Op sommige plaatsen, vooral in repetitief DNA zoals telomeren aan chromosoomuiteinden, centromeren nabij het midden en mobiele elementen zoals LINEs en SINEs, kan het nieuwe RNA terugvouwen en hybridiseren met het DNA. Dit creëert een R-lus: een kort RNA–DNA-hybride gekoppeld aan een verplaatste streng enkelstrengs DNA. Hoewel R-lussen in kleine, gecontroleerde hoeveelheden nuttig kunnen zijn, werken aanhoudende R-lussen als wegversperringen voor het machinerie dat DNA kopieert, wat leidt tot gebroken chromosomen, foutieve celdeling en genoominstabiliteit — kernmerken van kanker en genetische aandoeningen.
Het R-lus patrouille-eiwit
De onderzoekers tonen aan dat SFPQ, lang bekend als een RNA-bindend en spliceerfactor, ook een toegewijde sensor van R-lussen in repetitieve regio’s is. In cellen waarin SFPQ verminderd was, detecteerde het team meer R-lussen over telomeren, peri-centromerische satellieten en retro-elementen met behulp van hybride-specifieke antilichamen en sequencing-gebaseerde mapping. Deze hotspots vielen samen met sterke signalen van replicatiestress en DNA-schade. Biochemische experimenten met gezuiverd SFPQ onthulden waarom: SFPQ bindt niet goed aan gewoon dubbelstrengs DNA of aan RNA–DNA-duplexen, maar geeft een sterke voorkeur aan driedubbele structuren, vooral R-lussen die blootliggende RNA-staartjes dragen die lijken op natuurlijke repeat-RNA’s. Deze selectiviteit plaatst SFPQ als een eerstehulpverlener die problematische R-lussen herkent precies daar waar het genoom het meest repetitief is.
Opbouwen van beschermend chromatine-harnas
Het detecteren van deze knopen is slechts een deel van het verhaal. Het team ontdekte dat SFPQ fysiek interageert met DAXX, een eiwit dat een speciaal histonvariant, H3.3, in chromatine levert. H3.3 helpt bij het vormen van stabiele nucleosomen die repetitief DNA stilleggen en ongecontroleerde recombinatie voorkomen. Mapping-experimenten over het genoom lieten zien dat SFPQ en DAXX vaak gedeelde bindingsplaatsen hebben in intergene en intronische repeats, eerder dan bij klassieke genpromoters. Wanneer SFPQ verloren ging, verschoof DAXX weg van repeats richting regulerende regio’s, en werd H3.3 niet langer efficiënt gedeponeerd op repeat-rijke stukken, hoewel de totale H3.3-eiwitniveaus onveranderd bleven. Daardoor raakte het chromatine bij deze repeats slecht georganiseerd, wat R-lussen en replicatiestress liet ophopen.
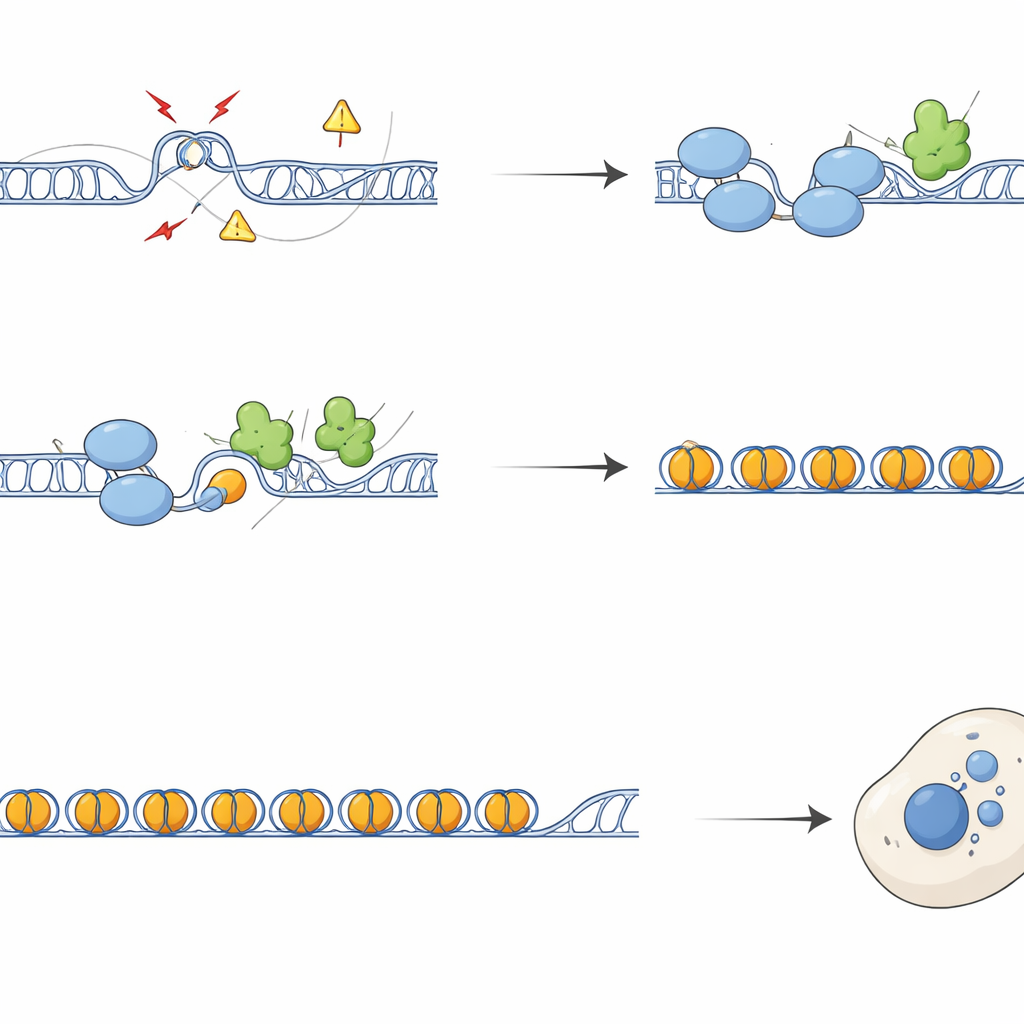
Van gebroken chromosomen naar gealarmeerde immuniteit
Zonder SFPQ stapelden repetitieve regio’s DNA-schadekenmerken en reparatiefactoren op, en vertoonden chromosomen meer breuken en uitwisselingen tussen zusterstrengen. Tijdens celdeling vertaalde deze schade zich in defecte segregatie, waarbij chromatinebruggen en micronuclei ontstonden — kleine extra DNA-bevattende lichaampjes buiten de hoofdcelkern. Deze micronuclei bevatten vaak telomerische en centromerische sequenties en waren bedekt met cGAS, een sensor van verkeerd geplaatsto DNA die de cGAS–STING-route van de aangeboren immuniteit activeert. Cellen zonder SFPQ of DAXX activeerden interferon- en ontstekingsgenen, een effect dat grotendeels kon worden teruggedraaid door overexpressie van RNaseH1, een enzym dat R-lussen verwijdert, of door STING te blokkeren. Zo voeden overtollige R-lussen bij repeats rechtstreeks immuunsignalen via de productie van cytoplasmatisch DNA-afval.
Implicaties voor kanker en patiëntuitkomsten
In gegevens van sarcoompatiënten correleerde hoge SFPQ-expressie met slechtere overleving, terwijl een genhandtekening die sterke activatie van de aangeboren immuniteit weerspiegelt — vergelijkbaar met wat wordt gezien bij verlies van SFPQ — werd verbonden met betere uitkomsten. Patiënten met lage SFPQ maar hoge immuunhandtekening scoorden het beste, wat suggereert dat het uitschakelen van deze beschermende as bij repeats in tumoren onbedoeld kankercellen aan het immuunsysteem kan blootstellen. Het werk schetst een mechanistische keten van R-lusdetectie door SFPQ, naar DAXX–H3.3-gemedieerde chromatinebescherming, naar het voorkomen van genoominstabiliteit en het dempen van aangeboren immuniteit. Voor leken is de kernboodschap dat SFPQ fungeert als een onderhoudsteam voor repetitief DNA: het detecteert gevaarlijke RNA–DNA-knopen, roept verpakkingshulpen op om deze regio’s glad te strijken en te bepantseren, en houdt daarmee chromosomen intact en immuunalarmen gedempt — een evenwicht dat kankers kunnen uitbuiten maar dat toekomstige therapieën mogelijk weer in het voordeel van de patiënt kunnen kantelen.
Bronvermelding: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Trefwoorden: R-lussen, genoomstabiliteit, histon H3.3, aangeboren immuniteit, sarcoom