Clear Sky Science · de
SFPQ lenkt die Einlagerung von Histon H3.3 zu R-Schlaufen in DNA-Wiederholungen, um die Genomstabilität zu schützen
Wächter unserer DNA‑Wiederholungen
Ein großer Teil unserer DNA besteht aus langen, wiederholten Sequenzen, die früher als „Junk“ abgetan wurden. Heute wissen wir, dass diese Regionen fehlgehen können und ungewöhnliche, dreisträngige Knoten bilden — sogenannte R‑Schlaufen — die die DNA‑Replikation blockieren und Schäden auslösen. Diese Studie zeigt, wie ein Protein namens SFPQ diese repetitiven Abschnitte überwacht, ihre Verpackung organisiert und so stillschweigend die Genomstabilität schützt und sogar beeinflusst, wie bestimmte Krebsarten mit dem Immunsystem interagieren.
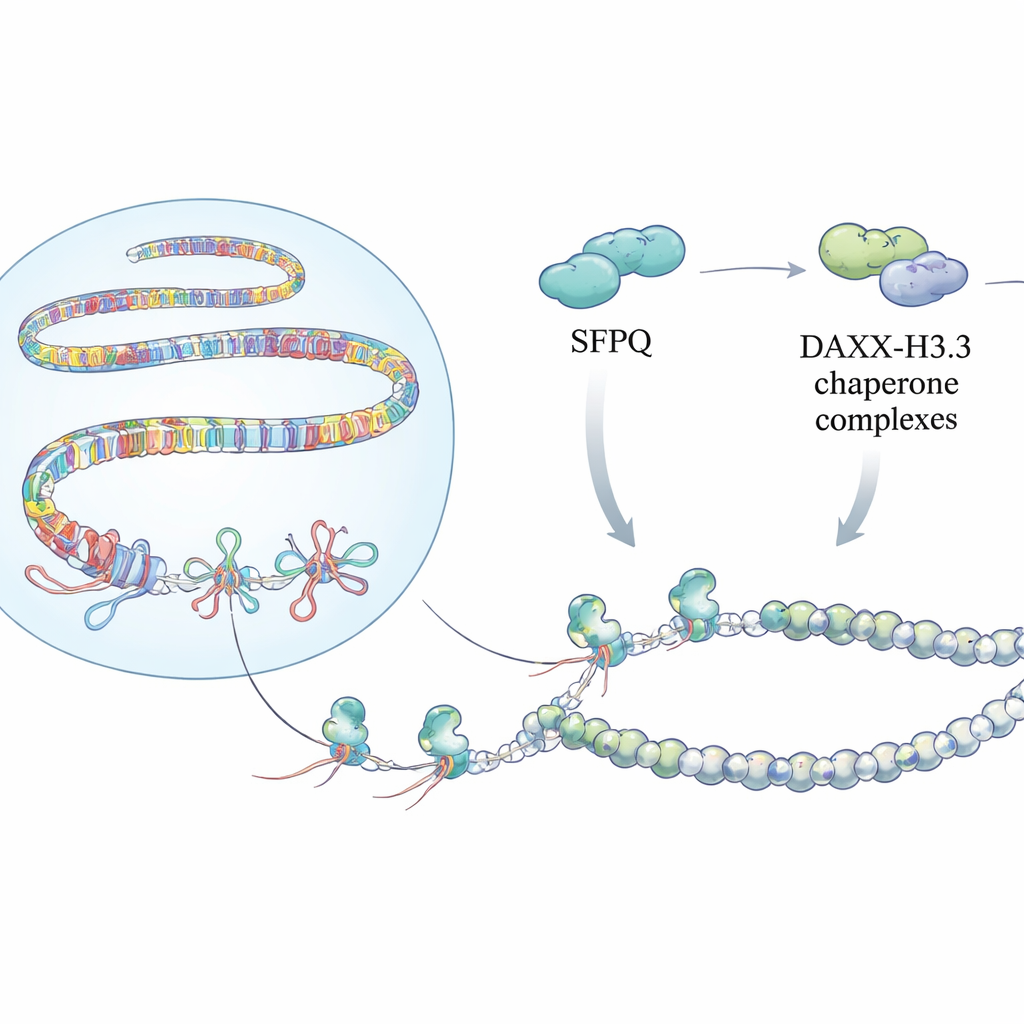
Versteckte Knoten im Genom
Beim Ablesen eines Gens wird eine vorübergehende RNA‑Kopie aus der DNA erzeugt. An manchen Stellen, besonders in repetitiver DNA wie Telomeren an Chromosomenenden, Zentromeren in der Chromosomenmitte und mobilen Elementen wie LINEs und SINEs, kann die neu entstehende RNA zurückfalten und sich an die DNA hybridisieren. Das ergibt eine R‑Schlaufe: ein kurzes RNA–DNA‑Hybrid mit einem verdrängten einzelsträngigen DNA‑Strang. Während R‑Schlaufen in kleinen, kontrollierten Mengen nützlich sein können, wirken persistente R‑Schlaufen wie Blockaden für die Replikationsmaschinerie und führen zu Chromosomenbrüchen, fehlerhafter Zellteilung und Genominstabilität — Kernmerkmale von Krebs und genetischen Erkrankungen.
Das R‑Schlaufen‑Patrouillenprotein
Die Forschenden zeigen, dass SFPQ, lange bekannt als RNA‑bindender und Spleißfaktor, auch als spezialisierter Sensor für R‑Schlaufen in repetitiven Regionen fungiert. In Zellen mit reduziertem SFPQ fanden die Autorinnen und Autoren mehr R‑Schlaufen an Telomeren, peri‑zentromerischen Satelliten und Retroelementen, gemessen mit hybrid‑spezifischen Antikörpern und sequencing‑basierten Karten. Diese Hotspots fielen mit starken Signalen von Replikationsstress und DNA‑Schäden zusammen. Biochemische Experimente mit gereinigtem SFPQ erklärten das: SFPQ bindet weder gewöhnliche doppelsträngige DNA noch RNA–DNA‑Duplexe gut, sondern bevorzugt deutlich dreisträngige Strukturen, insbesondere R‑Schlaufen mit exponierten RNA‑Enden, die natürlichen Repeat‑RNAs ähneln. Diese Selektivität positioniert SFPQ als Ersthelfer, der problematische R‑Schlaufen genau dort erkennt, wo das Genom am repetitivsten ist.
Aufbau einer schützenden Chromatin‑Hülle
Das Erkennen dieser Knoten ist nur ein Teil der Geschichte. Das Team entdeckte, dass SFPQ physisch mit DAXX interagiert, einem Protein, das eine spezielle Histonvariante namens H3.3 in das Chromatin einbringt. H3.3 hilft, stabile Nukleosomen zu bilden, die repetitive DNA stilllegen und unkontrollierte Rekombination verhindern. Genomweite Kartierungen zeigten, dass SFPQ und DAXX häufig Bindungsstellen in intergenen und intronischen Repeats teilen, eher als an klassischen Promotoren von Genen. Beim Verlust von SFPQ verlagerte sich DAXX weg von Repeats hin zu regulatorischen Regionen, und H3.3 wurde an repeat‑reichen Abschnitten nicht mehr effizient eingebracht, obwohl die Gesamtmenge an H3.3‑Protein unverändert blieb. Infolgedessen wurde das Chromatin‑Gerüst an diesen Repeats schlecht organisiert, sodass R‑Schlaufen und Replikationsstress zunahmen.
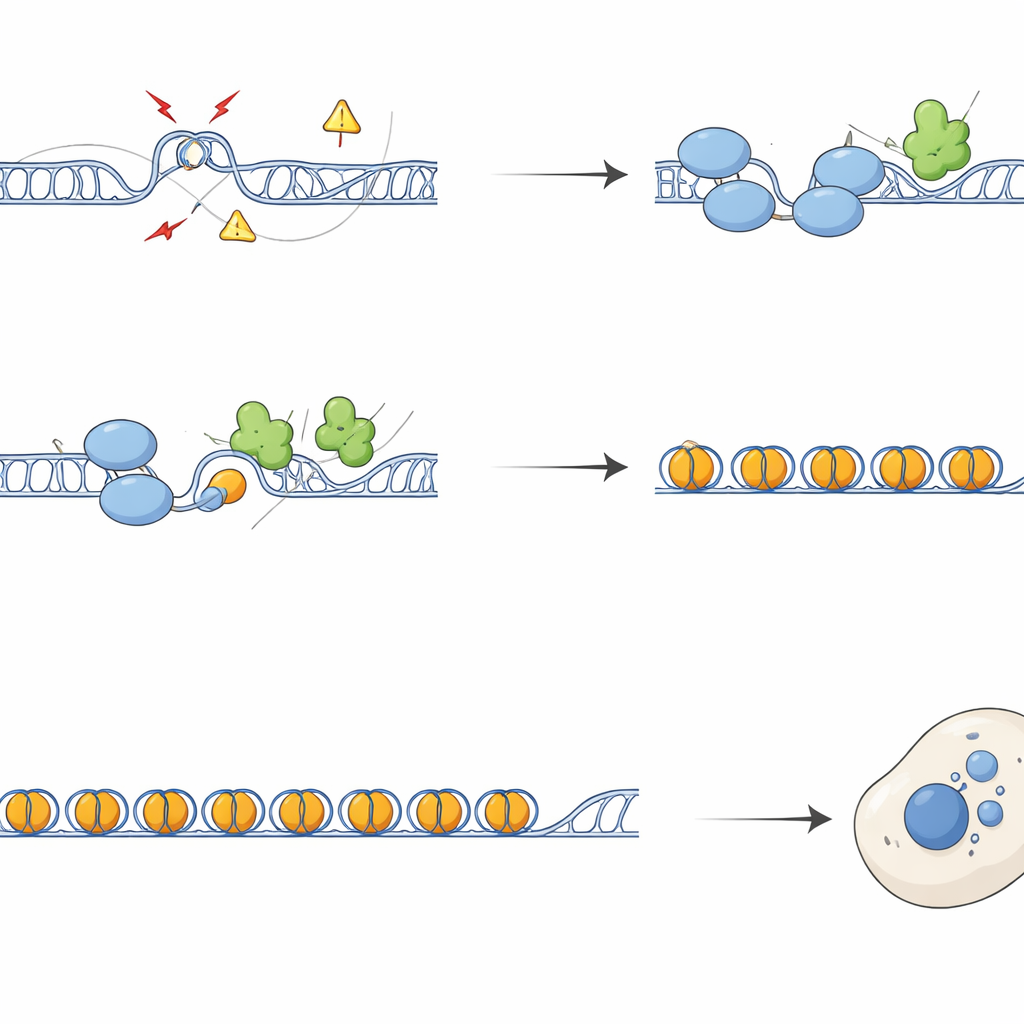
Von gebrochenen Chromosomen zu alarmierter Immunität
Ohne SFPQ häuften sich in repetitiven Regionen DNA‑Schadensmarker und Reparaturfaktoren, und Chromosomen zeigten mehr Brüche und Austauschereignisse zwischen Schwesterchromatiden. Während der Zellteilung führte dieser Schaden zu fehlerhafter Segregation, der Bildung von Chromatinbrücken und Mikrokernen — winzigen zusätzlichen DNA‑haltigen Körpern außerhalb des Hauptkerns. Diese Mikrokerne trugen häufig telomerische und zentromerische Sequenzen und waren mit cGAS überzogen, einem Sensor fehlplatzierter DNA, der den cGAS–STING‑Weg der angeborenen Immunität aktiviert. Zellen ohne SFPQ oder DAXX schalteten Interferon‑ und Entzündungs‑Gene ein; dieser Effekt ließ sich weitgehend rückgängig machen durch Überexpression von RNaseH1, einem Enzym, das R‑Schlaufen entfernt, oder durch Blockade von STING. Überschüssige R‑Schlaufen an Repeats führen demnach direkt zu Immun‑Signalen durch die Entstehung zytoplasmatischer DNA‑Trümmer.
Folgen für Krebs und Patientenverläufe
In Daten von Sarkom‑Patienten korrelierte hohe SFPQ‑Expression mit schlechterem Überleben, während eine Gen‑Signatur, die starke Aktivierung der angeborenen Immunität widerspiegelt — ähnlich der bei SFPQ‑Verlust beobachteten — mit besseren Ergebnissen verbunden war. Am besten schnitten Patientinnen und Patienten mit niedrigem SFPQ, aber hoher Immun‑Signatur ab, was nahelegt, dass das Ausschalten dieser Schutzachse an Repeats Tumorzellen unbeabsichtigt dem Immunsystem aussetzen kann. Die Arbeit skizziert eine mechanistische Kette: R‑Schlaufen‑Erkennung durch SFPQ, DAXX–H3.3‑vermittelte Chromatin‑Schutzmaßnahmen, Verhinderung von Genominstabilität und Dämpfung der angeborenen Immunität. Für ein allgemeines Publikum lautet die Kernbotschaft: SFPQ wirkt wie eine Wartungsmannschaft für repetitive DNA — es erkennt gefährliche RNA–DNA‑Knoten, ruft Verpackungshilfen, um diese Regionen zu glätten und zu schützen, und erhält so Chromosomenintegrität und stille Immunalarme — ein Gleichgewicht, das Krebsarten ausnutzen können, das aber durch zukünftige Therapien zugunsten der Patientinnen und Patienten verschoben werden könnte.
Zitation: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Schlüsselwörter: R‑Schlaufen, Genomstabilität, Histon H3.3, angeborene Immunität, Sarkom