Clear Sky Science · ru
SFPQ направляет отложение гистона H3.3 на R-петли в повторах ДНК для защиты стабильности генома
Стражи наших повторяющихся участков ДНК
Большая часть нашей ДНК состоит из длинных повторяющихся последовательностей, которые когда‑то считались «мусором». Сейчас известно, что эти участки могут вести себя проблемно, образуя необычные трёхцепочные узлы, называемые R‑петлями, — они тормозят копирование ДНК и вызывают повреждения. В этом исследовании показано, как белок SFPQ патрулирует эти повторяющиеся участки, организует их упаковку и тем самым защищает стабильность генома и даже влияет на то, как некоторые опухоли взаимодействуют с иммунной системой.
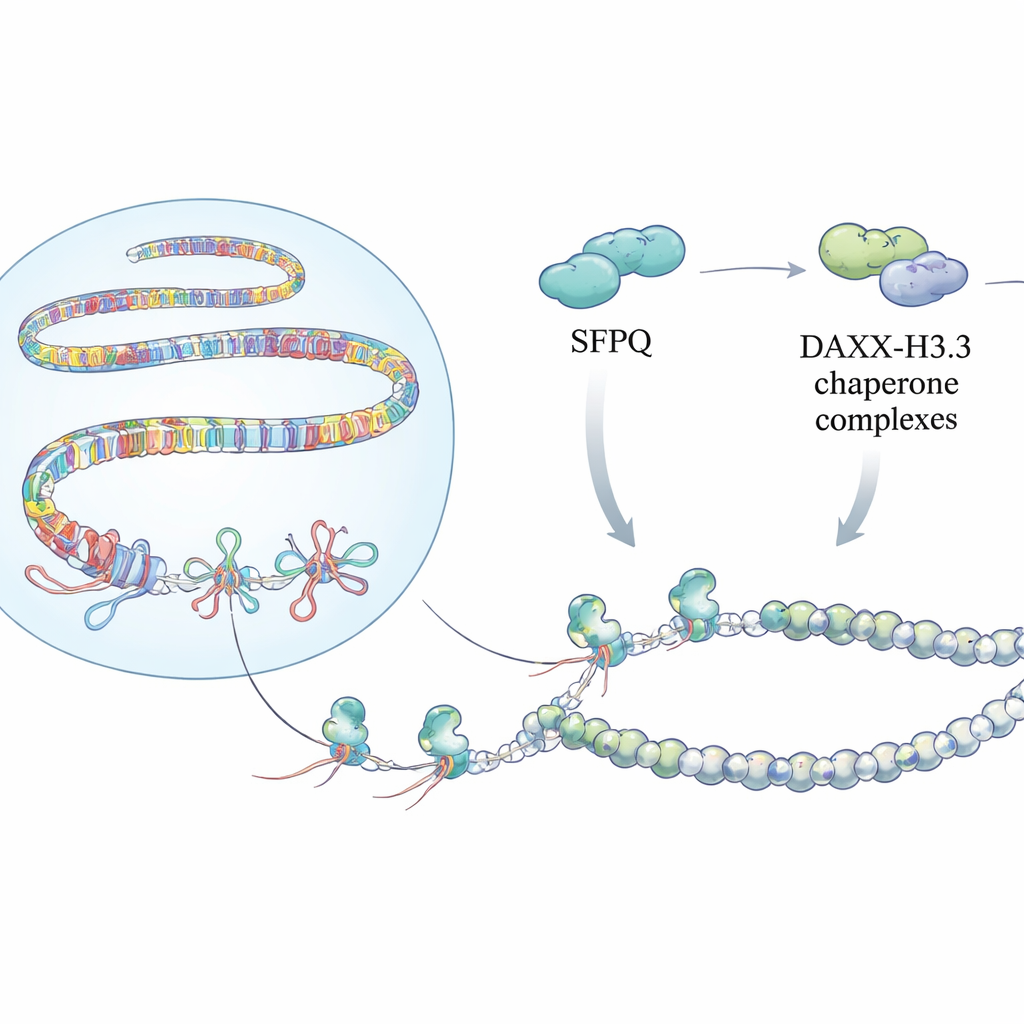
Скрытые узлы в геноме
При считывании гена временная копия РНК синтезируется с ДНК. В некоторых местах, особенно в повторяющейся ДНК, например в теломерах на концах хромосом, центромерах возле середины и в подвижных элементах типа LINE и SINE, новая РНК может складываться назад и гибридизоваться с ДНК. Это создаёт R‑петлю: короткий РНК–ДНК гибрид вместе с вытесненной однонитевой ДНК. Хотя R‑петли бывают полезны в малых, контролируемых количествах, стойкие петли действуют как препятствия для аппарата репликации ДНК, приводя к разрывам хромосом, ошибкам при делении клеток и нестабильности генома — ключевым признакам рака и генетических заболеваний.
Белок‑патруль R‑петель
Авторы показывают, что SFPQ, давно известный как РНК‑связывающий и сплайсинговый фактор, также выполняет роль датчика R‑петель в повторяющихся регионах. В клетках с уменьшенным уровнем SFPQ команда обнаружила больше R‑петель на теломерах, перицентромерных сателлитах и ретроэлементах с помощью антител, специфичных к гибридам, и картирования на основе секвенирования. Эти «горячие точки» совпадали с сильными признаками репликационного стресса и повреждений ДНК. Биохимические эксперименты с очищенным SFPQ объяснили причину: SFPQ слабо связывается с обычной двуцепочечной ДНК или с двойными РНК–ДНК дуплексами, но сильно предпочитает трёхцепочные структуры, особенно R‑петли с открытыми хвостами РНК, похожими на природные повторяющиеся РНК. Такая селективность делает SFPQ первым реагирующим фактором, распознающим проблемные R‑петли именно там, где геном наиболее повторяющийся.
Формирование защитной хроматиновой брони
Обнаружение этих узлов — лишь часть истории. Команда выяснила, что SFPQ физически взаимодействует с DAXX, белком, который доставляет в хроматин особый вариант гистона, называемый H3.3. H3.3 способствует формированию стабильных нуклеосом, которые подавляют активность повторяющейся ДНК и предотвращают неконтролируемую рекомбинацию. Картирование по всему геному показало, что SFPQ и DAXX часто разделяют сайты связывания в интергенных и интронных повторах, а не на классических промоторах генов. При потере SFPQ DAXX смещался с повторов к регуляторным областям, и H3.3 уже не депонировался эффективно в участках, богатых повторами, хотя общий уровень белка H3.3 оставался неизменным. В результате хроматиновый ландшафт этих повторов становился плохо организованным, что позволяло накапливаться R‑петлям и репликационному стрессу.
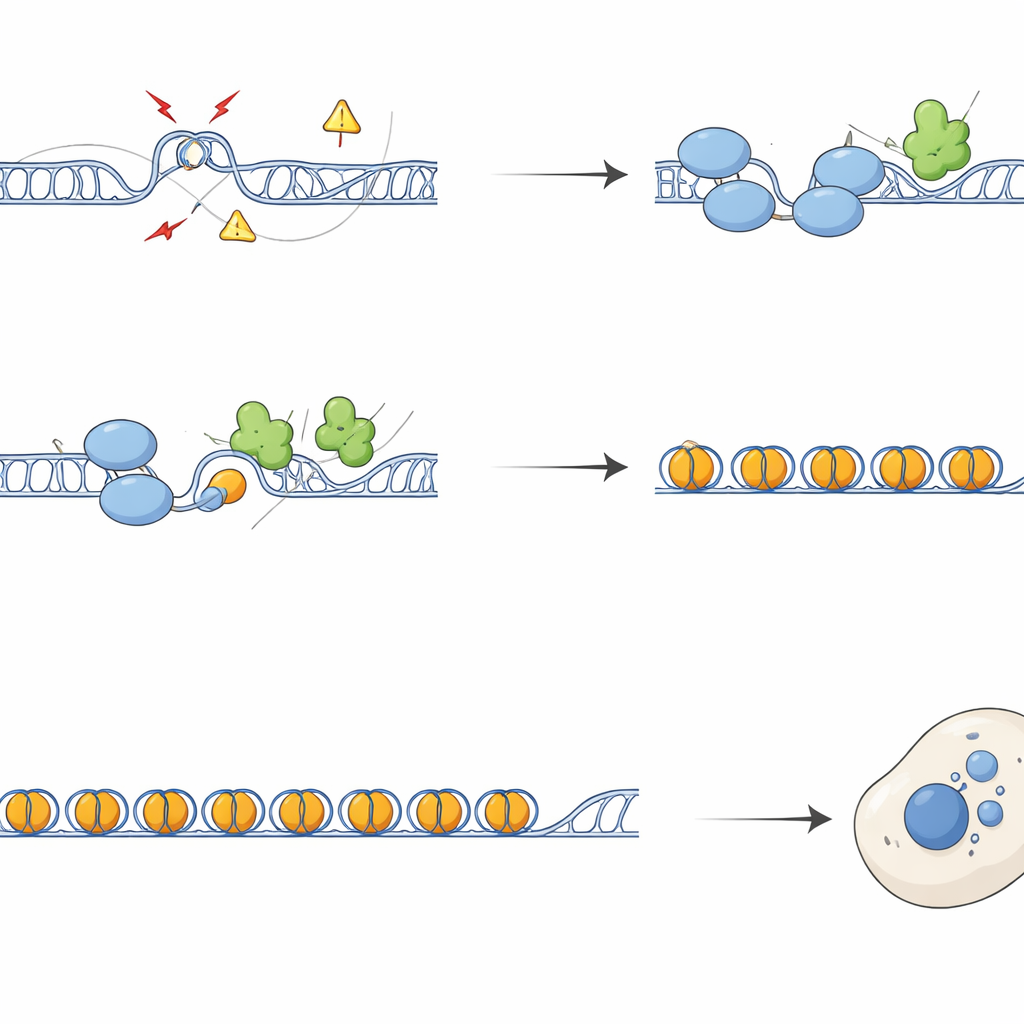
От разорванных хромосом до сигналов тревоги иммунной системы
Без SFPQ повторяющиеся регионы накапливали маркеры повреждений ДНК и факторы репарации, хромосомы демонстрировали больше разрывов и обменов между сестринскими нитями. В процессе деления клеток это выливалось в дефекты сегрегации — образование хроматиновых мостов и микронуклеев — крошечных дополнительных телец с ДНК вне основного ядра. Эти микронуклеи часто содержали теломерные и центромерные последовательности и были покрыты cGAS, сенсором смещённой ДНК, который активирует врождённый путь cGAS–STING. Клетки, лишённые SFPQ или DAXX, активировали интерферонные и провоспалительные гены — эффект, который в значительной мере можно было обратить, переэкспрессируя RNaseH1, фермент, удаляющий R‑петли, или блокируя STING. Таким образом, избыточные R‑петли в повторах напрямую запускают иммунную сигнализацию через образование цитоплазматических фрагментов ДНК.
Последствия для рака и прогноза пациентов
В данных по пациентам с саркомой высокий уровень экспрессии SFPQ кореллировал с более худшей выживаемостью, тогда как сигнатура генов, отражающая сильную активацию врождённого иммунитета — похожая на ту, что наблюдается при потере SFPQ — ассоциировалась с лучшими исходами. Пациенты с низким SFPQ и высокой иммунной сигнатурой имели наилучшие результаты, что указывает на то, что в опухолях нарушение этой защитной оси на повторах может непреднамеренно сделать раковые клетки более заметными для иммунной системы. Работа описывает механистическую цепочку от распознавания R‑петель SFPQ до DAXX–H3.3‑опосредованной хроматиновой защиты, предотвращения нестабильности генома и ослабления врождённого иммунитета. Для широкой аудитории главный вывод таков: SFPQ действует как служба технического обслуживания повторяющейся ДНК — он обнаруживает опасные РНК–ДНК узлы, привлекает помощников по упаковке, чтобы сгладить и оградить эти участки, и тем самым сохраняет целостность хромосом и подавляет ложные иммунные тревоги — равновесие, которым опухоли могут воспользоваться, но которое потенциально можно переориентировать в пользу пациента при будущих терапиях.
Цитирование: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Ключевые слова: R-петли, стабильность генома, гистон H3.3, врождённый иммунитет, саркома