Clear Sky Science · es
SFPQ dirige la deposición de la histona H3.3 hacia los R-loops en repeticiones de ADN para proteger la estabilidad del genoma
Guardianes de nuestras repeticiones de ADN
Gran parte de nuestro ADN está compuesto por secuencias largas y repetidas que antes se consideraban “basura”. Ahora sabemos que estas regiones pueden comportarse mal, formando nudos inusuales de tres hebras llamados R-loops que detienen la copia del ADN y provocan daños. Este estudio revela cómo una proteína llamada SFPQ patrulla estos tramos repetitivos, organiza su empaquetamiento y, al hacerlo, protege silenciosamente la estabilidad del genoma e incluso condiciona cómo ciertos cánceres interactúan con el sistema inmune.
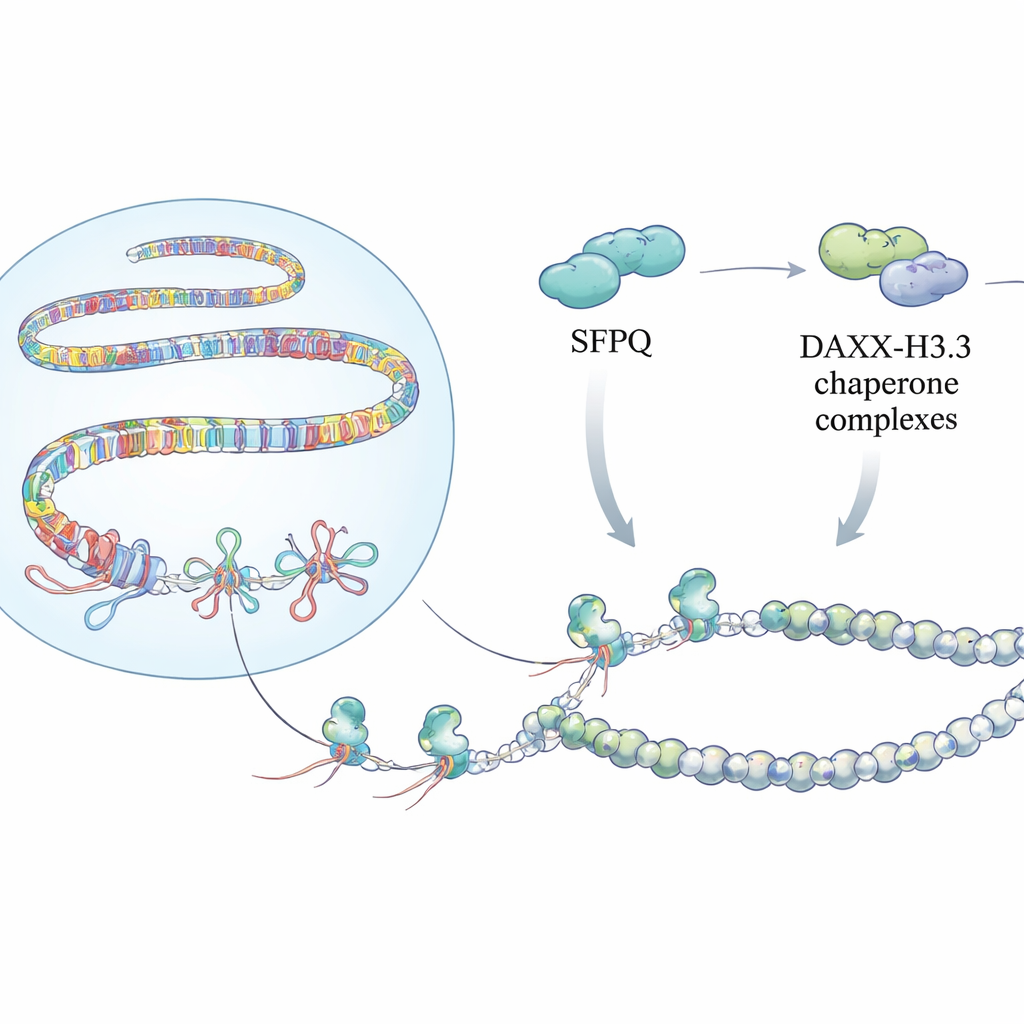
Nudos ocultos en el genoma
Cuando se lee un gen, se produce una copia temporal de ARN desde el ADN. En algunos lugares, sobre todo en ADN repetitivo como los telómeros en los extremos cromosómicos, los centrómeros cerca del centro y elementos móviles como LINEs y SINEs, el ARN nuevo puede plegarse y hibridarse con el ADN. Esto crea un R-loop: un híbrido ARN–ADN corto emparejado con una hebra de ADN sencilla desplazada. Aunque los R-loops pueden ser útiles en dosis pequeñas y controladas, los persistentes actúan como obstáculos para la maquinaria que replica el ADN, provocando roturas cromosómicas, división celular defectuosa e inestabilidad genómica, rasgos clave del cáncer y las enfermedades genéticas.
La proteína patrulla de los R-loops
Los investigadores muestran que SFPQ, conocida desde hace tiempo como una proteína de unión al ARN y factor del empalme, es también un sensor dedicado de R-loops en regiones repetitivas. En células con niveles reducidos de SFPQ, el equipo detectó más R-loops a lo largo de telómeros, satélites pericentroméricos y retroelementos mediante anticuerpos específicos para híbridos y mapeo por secuenciación. Estos puntos calientes coincidían con señales intensas de estrés replicativo y daño en el ADN. Experimentos bioquímicos con SFPQ purificada explicaron por qué: SFPQ no se une bien al ADN de doble cadena ordinario ni a los dúplex ARN–ADN, pero prefiere con fuerza las estructuras de tres hebras, especialmente los R-loops que presentan colas de ARN expuestas similares a los ARNs de repeticiones naturales. Esta selectividad sitúa a SFPQ como un primer respondedor que reconoce R-loops problemáticos precisamente donde el genoma es más repetitivo.
Construyendo una armadura protectora de cromatina
Detectar estos nudos es solo parte de la historia. El equipo descubrió que SFPQ interactúa físicamente con DAXX, una proteína que entrega una variante especial de histona llamada H3.3 a la cromatina. H3.3 ayuda a formar nucleosomas estables que silencian el ADN repetitivo y previenen la recombinación descontrolada. Experimentos de mapeo en todo el genoma mostraron que SFPQ y DAXX comparten con frecuencia sitios de unión en repeticiones intergénicas e intrónicas, más que en promotores clásicos de genes. Cuando se perdió SFPQ, DAXX se desplazó desde las repeticiones hacia regiones regulatorias, y H3.3 dejó de depositarse eficazmente en tramos ricos en repeticiones, aun cuando los niveles totales de proteína H3.3 no cambiaron. Como resultado, la plantilla de cromatina en estas repeticiones quedó desorganizada, permitiendo la acumulación de R-loops y estrés replicativo.
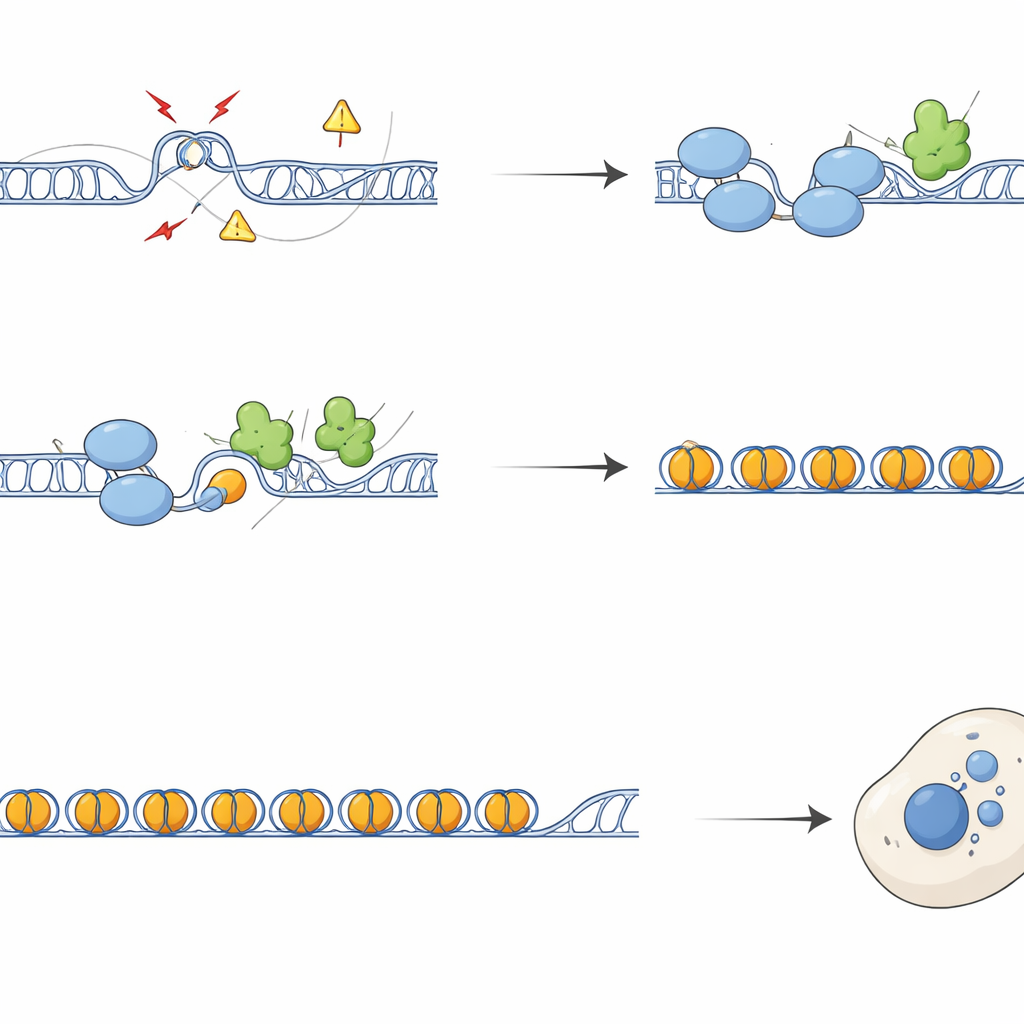
Desde cromosomas rotos hasta una inmunidad alarmada
Sin SFPQ, las regiones repetitivas acumularon marcadores de daño en el ADN y factores de reparación, y los cromosomas mostraron más roturas e intercambios entre cromátidas hermanas. Durante la división celular, este daño se tradujo en una segregación defectuosa, formando puentes de cromatina y micronúcleos: pequeños cuerpos extra con ADN fuera del núcleo principal. Estos micronúcleos con frecuencia contenían secuencias teloméricas y centroméricas y estaban recubiertos por cGAS, un sensor de ADN en lugar equivocado que activa la vía inmune innata cGAS–STING. Las células carentes de SFPQ o DAXX activaron genes de interferón e inflamatorios, un efecto que pudo revertirse en gran medida al sobreexpresar RNaseH1, una enzima que elimina R-loops, o al bloquear STING. Así, el exceso de R-loops en repeticiones alimenta directamente la señalización inmune mediante la producción de desechos de ADN citoplasmático.
Implicaciones para el cáncer y el pronóstico de los pacientes
En datos de pacientes con sarcoma, una alta expresión de SFPQ se correlacionó con peor supervivencia, mientras que una firma génica que refleja una fuerte activación de la inmunidad innata—similar a la observada cuando SFPQ se pierde—se asoció con mejores resultados. Los pacientes con baja expresión de SFPQ pero alta expresión de la firma inmune tuvieron el mejor pronóstico, lo que sugiere que, en tumores, desactivar este eje protector en las repeticiones puede exponer inadvertidamente a las células cancerosas al sistema inmune. El trabajo describe una cadena mecanicista desde la detección de R-loops por SFPQ, pasando por la protección de la cromatina mediada por DAXX–H3.3, hasta la prevención de la inestabilidad genómica y el apagado de la inmunidad innata. Para un público general, el mensaje principal es que SFPQ actúa como un equipo de mantenimiento del ADN repetitivo: detecta nudos peligrosos ARN–ADN, recluta ayudantes de empaquetamiento para alisar y blindar estas regiones y, al hacerlo, mantiene los cromosomas intactos y las alarmas inmunitarias en silencio—un equilibrio que los cánceres pueden explotar, pero que las terapias futuras podrían inclinar a favor del paciente.
Cita: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Palabras clave: R-loops, estabilidad genómica, histona H3.3, inmunidad innata, sarcoma