Clear Sky Science · pl
SFPQ kieruje osadzaniem histonu H3.3 w pętlach R w powtórzeniach DNA, aby chronić stabilność genomu
Strażnicy naszych powtórzeń DNA
Znaczna część naszego DNA składa się z długich sekwencji powtarzalnych kiedyś lekceważonych jako „śmieciowe”. Dziś wiadomo, że te regiony mogą źle się zachowywać, tworząc nietypowe, trójłącznikowe supły zwane pętlami R, które zatrzymują kopiowanie DNA i wywołują uszkodzenia. Badanie to ujawnia, jak białko o nazwie SFPQ patroluje te powtarzalne odcinki, organizuje ich upakowanie i w ten sposób dyskretnie chroni stabilność genomu, a nawet wpływa na to, jak niektóre nowotwory oddziałują z układem odpornościowym.
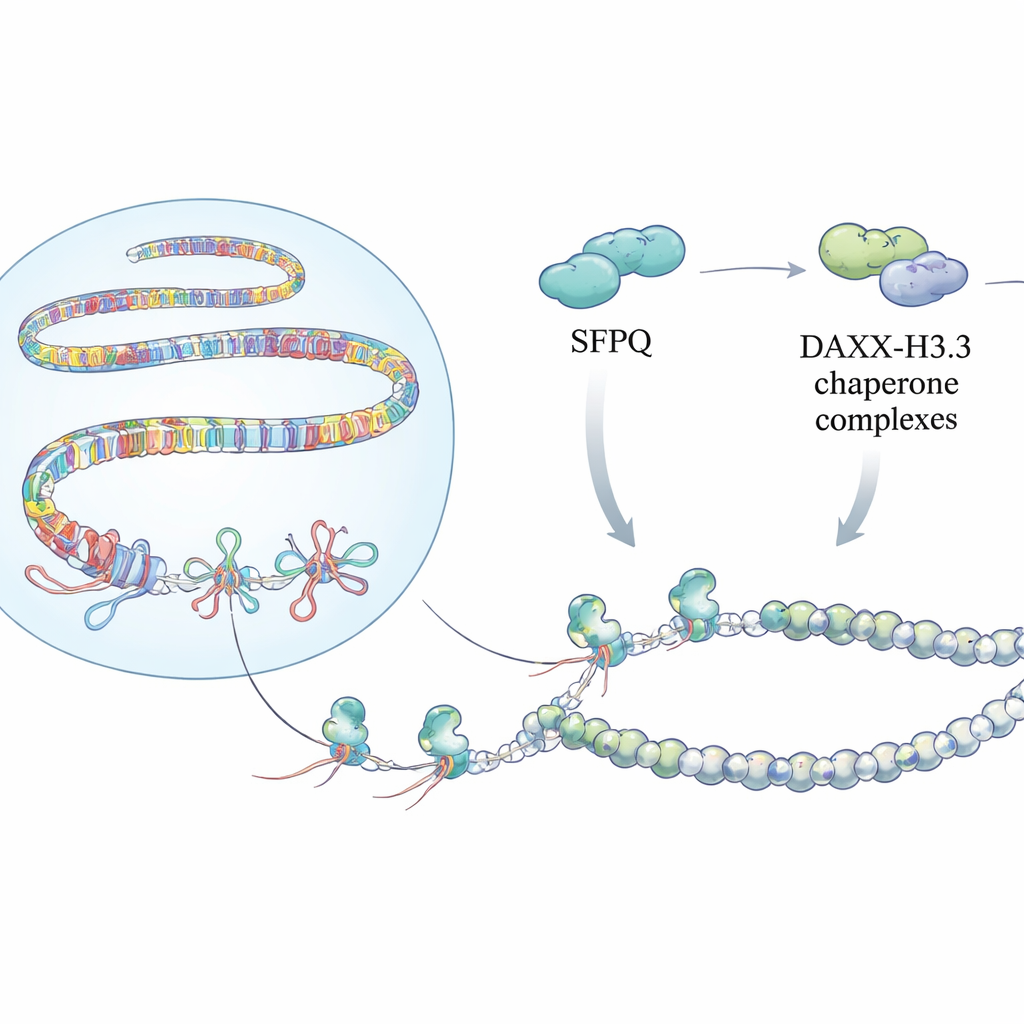
Ukryte supły w genomie
Gdy gen jest odczytywany, z DNA powstaje tymczasowa kopia RNA. W niektórych miejscach, zwłaszcza w DNA powtarzalnym, takim jak telomery na końcach chromosomów, centromery w pobliżu środka oraz elementy mobilne jak LINE i SINE, nowy RNA może zawijać się i hybrydyzować z DNA. Powstaje wtedy pętla R: krótki hybryd RNA–DNA sparowany z odsuniętym pojedynczym nicią DNA. Chociaż pętle R mogą być użyteczne w niewielkich, kontrolowanych ilościach, te przewlekłe działają jak przeszkody dla maszynerii kopiującej DNA, prowadząc do złamań chromosomów, wadliwego podziału komórki i niestabilności genomu — kluczowych cech nowotworów i chorób genetycznych.
Białko patrolujące pętle R
Naukowcy wykazali, że SFPQ, znane dotąd jako czynnik wiążący RNA i biorący udział w składaniu transkryptów, jest także wyspecjalizowanym sensorem pętli R w regionach powtarzalnych. W komórkach z obniżonym poziomem SFPQ zespół wykrył więcej pętli R w telomerach, przycentromerowych satelitach i elementach retrowirusopodobnych za pomocą przeciwciał specyficznych dla hybryd oraz mapowania opartego na sekwencjonowaniu. Te miejsca pokrywały się z silnymi sygnałami stresu replikacyjnego i uszkodzeń DNA. Doświadczenia biochemiczne z oczyszczonym SFPQ wyjaśniły dlaczego: SFPQ słabo wiąże zwykłe dwuniciowe DNA lub duplexy RNA–DNA, ale wyraźnie preferuje struktury trójwiązkowe, zwłaszcza pętle R z odsłoniętymi ogonami RNA podobnymi do naturalnych RNA z powtórzeń. Ta selektywność stawia SFPQ w roli pierwszego reagenta, który rozpoznaje problematyczne pętle R dokładnie tam, gdzie genom jest najbardziej powtarzalny.
Budowanie ochronnej zbroi chromatyny
Rozpoznanie tych supełków to tylko część historii. Zespół odkrył, że SFPQ fizycznie współdziała z DAXX, białkiem dostarczającym specjalny wariant histonu H3.3 do chromatyny. H3.3 pomaga tworzyć stabilne nukleosomy, które wyciszają DNA powtarzalne i zapobiegają niekontrolowanej rekombinacji. Mapowania w skali genomu wykazały, że SFPQ i DAXX często dzielą miejsca wiązania w powtórzeniach międzygenowych i intronowych, zamiast klasycznych promotorów genów. Gdy SFPQ zniknęło, DAXX przesunął się z powtórzeń w kierunku regionów regulacyjnych, a H3.3 przestał być efektywnie osadzany w fragmentach bogatych w powtórzenia, mimo że ogólne poziomy białka H3.3 pozostały niezmienione. W rezultacie szablon chromatynowy w tych powtórzeniach stał się słabo zorganizowany, co umożliwiło narastanie pętli R i stresu replikacyjnego.
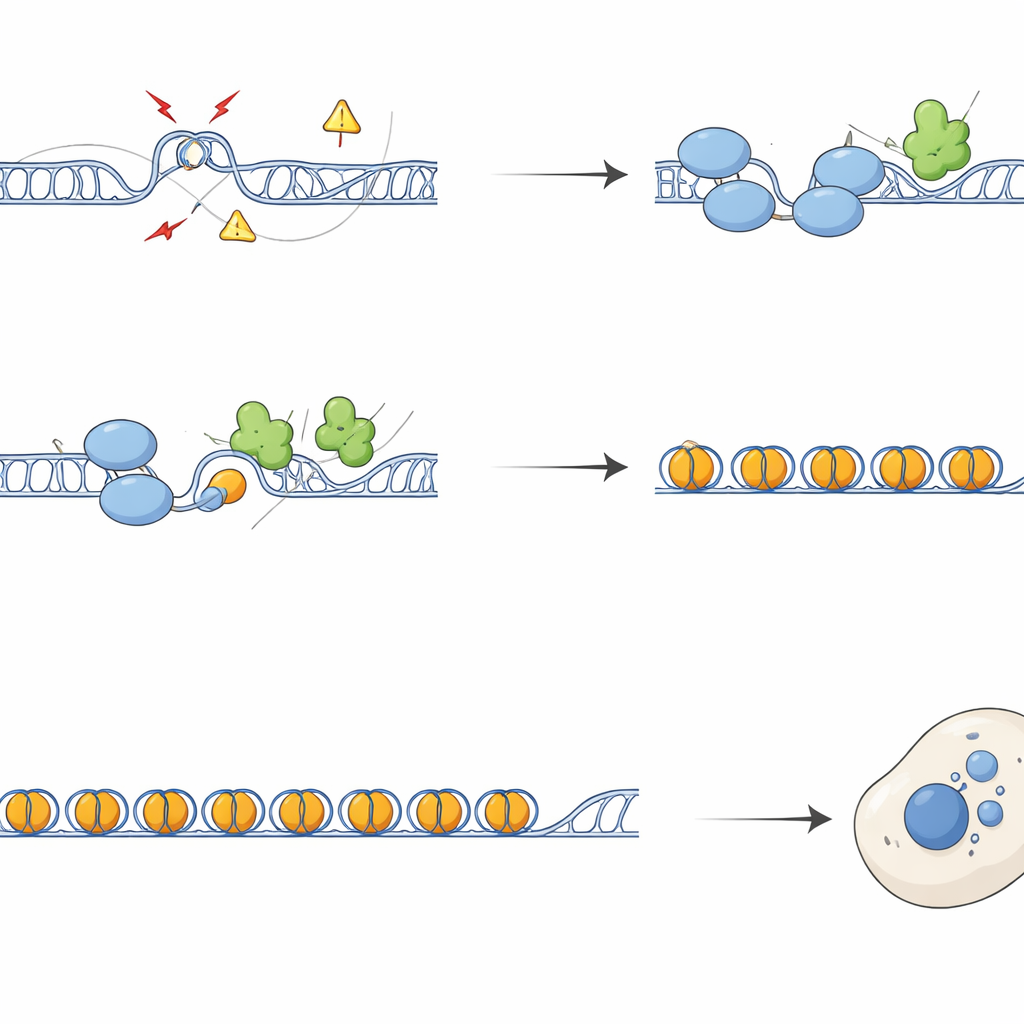
Od złamanych chromosomów do zaalarmowanej odpornosti
Bez SFPQ regiony powtarzalne gromadziły markery uszkodzeń DNA i czynniki naprawcze, a chromosomy wykazywały więcej złamań i wymian między chromatydami siostrzanymi. Podczas podziału komórki te uszkodzenia przekładały się na wadliwe segregowanie, tworząc mostki chromatynowe i mikrojądra — małe dodatkowe ciała zawierające DNA poza głównym jądrem. Te mikrojądra często zawierały sekwencje telomerowe i centromerowe i były pokryte cGAS, sensorem przemieszonego DNA uruchamiającym ścieżkę odporności wrodzonej cGAS–STING. Komórki pozbawione SFPQ lub DAXX aktywowały geny interferonowe i zapalne, efekt który można było w dużej mierze odwrócić przez nadekspresję RNaseH1, enzymu usuwającego pętle R, lub przez zablokowanie STING. Tak więc nadmiar pętli R w powtórzeniach bezpośrednio napędza sygnalizację immunologiczną poprzez powstawanie cytoplazmatycznych fragmentów DNA.
Implikacje dla nowotworów i rokowań pacjentów
W danych pacjentów z mięsakiem wysoka ekspresja SFPQ korelowała z gorszym przeżyciem, podczas gdy sygnatura genowa odzwierciedlająca silną aktywację odporności wrodzonej — podobna do tej obserwowanej przy utracie SFPQ — wiązała się z lepszymi wynikami. Pacjenci z niskim SFPQ, ale wysoką ekspresją sygnatury odpornościowej radzili sobie najlepiej, co sugeruje, że w guzie wyłączenie tej ochronnej osi w powtórzeniach może mimowolnie odsłonić komórki nowotworowe przed układem odpornościowym. Praca ta przedstawia mechaniczny łańcuch: od wykrywania pętli R przez SFPQ, przez ochronę chromatyny mediowaną przez DAXX–H3.3, po zapobieganie niestabilności genomu i tłumienie odporności wrodzonej. Dla szerokiej publiczności główny przekaz brzmi: SFPQ działa jak ekipa konserwacyjna dla DNA powtarzalnego — wykrywa niebezpieczne supły RNA–DNA, przywołuje pomoc przy upakowaniu, aby wygładzić i wzmocnić te regiony, i w ten sposób utrzymuje chromosomy w całości oraz tłumi alarmy odpornościowe — równowaga, którą nowotwory mogą wykorzystywać, ale którą przyszłe terapie mogłyby potencjalnie przywrócić na korzyść pacjenta.
Cytowanie: Ferrando, A., Giaquinto, M., Napolitano, L.M.R. et al. SFPQ directs histone H3.3 deposition to R-loops in DNA repeats to protect genome stability. Nat Commun 17, 3151 (2026). https://doi.org/10.1038/s41467-026-69479-w
Słowa kluczowe: pętle R, stabilność genomu, histon H3.3, odporność wrodzona, mięsak