Clear Sky Science · tr
Çeşitli popülasyonlardan xQTL ve tüm genom ilişki çalışmalarını birleştirmek ilaç hedefli gen keşfini geliştiriyor
Neden genler geleceğin ilaçları için önemli
Modern genetik, yaygın hastalıklarla ilişkili binlerce DNA işaretleyicisi ortaya çıkardı, ancak bu ipuçlarını gerçek ilaç hedeflerine dönüştürmek hayal kırıcı derecede yavaş ilerliyor. Bu çalışma merkezi bir darboğaza odaklanıyor: büyük genetik çalışmaların standart okunma biçimleri genellikle ilaçların gerçekten etkileyebileceği genleri kaçırıyor. Farklı popülasyonlar ve biyolojinin farklı katmanları arasındaki genetik verileri yeniden düşünerek, yazarlar Alzheimer, depresyon, şizofreni ve tip 2 diyabet gibi hastalıklarda gizli ama ilaçlanabilir zayıf noktaları ortaya çıkarmayı amaçlıyorlar.
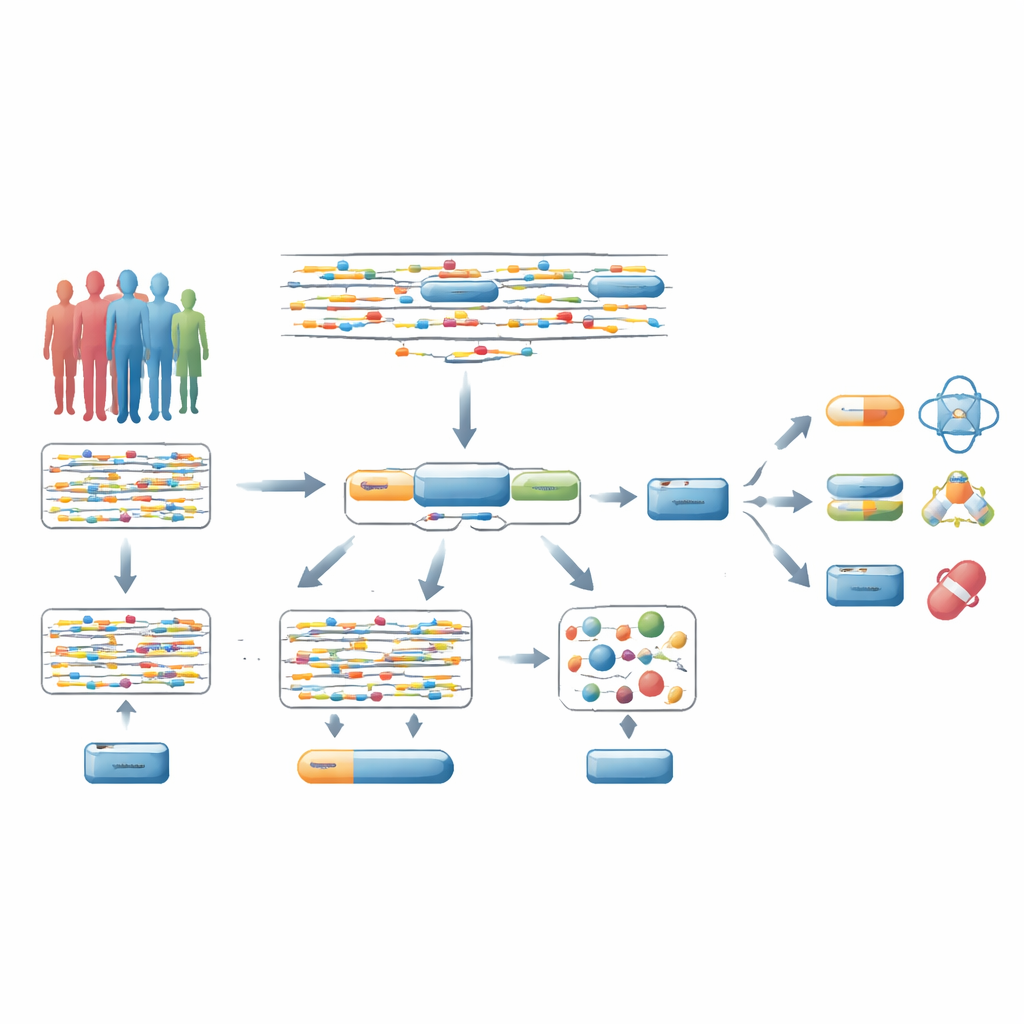
Dağınık DNA sinyallerinden tamamı bir gene
Çoğu tüm genom ilişki çalışması (GWAS) milyonlarca tek DNA değişikliğini teker teker inceler ve her birinin bir hastalıkla ilişkili olup olmadığını sorar. Genellikle araştırmacılar, bir genin yakınındaki en güçlü ilişkili DNA değişikliğinin o gene işaret ettiğini varsayar. Ancak bu kestirme sıklıkla yanlıştır: bu “önde gelen” varyantların yalnızca küçük bir kısmı gerçekten hastalığa neden olur ve uzak genleri etkileyebilir. Bu yüzden milyonlarca teste uygulanan katı istatistiksel düzeltmeler gerçek hastalık genlerini bulmayı zorlaştırır; özellikle mevcut veya potansiyel ilaçların hedefleyebileceği genleri bulmak daha zor hale gelir.
Genetik haritayı okumak için yeni bir araç seti
Yazarlar “gen-temelli” testler ailesini tanıtıyor; önder yöntemin adı GenT. Tek tek DNA değişikliklerini izole şekilde değerlendirmek yerine GenT, her gen çevresindeki ilgili tüm varyantları grupluyor ve birlikte test ediyor. Kritik olarak, ekip GenT gerçekte sinyal olmadığında nasıl davranması gerektiğini matematiksel olarak ortaya koydu; böylece önceki gen-temelli yaklaşımları rahatsız eden sahte alarmlardan kaçınılıyor. Bu çerçevenin MuGenT (çok kökenli veya çok özellikli veriler için) ve xGenT (gen ifade düzeyi veya protein miktarı gibi moleküler ölçümleri entegre eden) gibi uzantıları, araştırmacıların farklı popülasyonlar ve biyolojik katmanlar arasında bilgiyi özet istatistiklerden hareketle birleştirmesine olanak veriyor; bu özet istatistikler yaygın şekilde erişilebiliyor.
Beyinde ve vücutta gizli ilaç hedeflerini bulmak
GenT’yi Alzheimer hastalığı, amiyotrofik lateral skleroz, majör depresyon ve şizofreni üzerine yapılan büyük genetik çalışmalara uygulayan yazarlar 18.000’den fazla geni analiz etti. Mevcut veya deneysel bileşiklerle hedeflenebilen 415 protein üreten geni ortaya çıkardılar; bunların çoğunu standart GWAS yöntemleri kaçırmıştı. Bu ilaçlanabilir genlerin onlarcası, güçlü tek varyant sinyali göstermeyen bölgelere yerleşmiş; bu da riski ancak gen düzeyinde bakıldığında görünür hale gelen birçok ılımlı etkinin yaydığına işaret ediyor. Dikkate değer örnekler arasında Alzheimer için SYK ve şizofreni için THRB var; her ikisi de önceki biyolojik çalışmalarla desteklenmiş, fakat geleneksel analizlerin radarının altında kalmıştı.
Çeşitlilik ve moleküler katmanların gücü
MuGenT bu stratejiyi Avrupa, Afrika, Doğu Asya, Güney Asya ve Hispano kökenli kişilerden gelen genetik verilerle tip 2 diyabet için birleştiriyor. Birçok risk varyantı paylaşılsa da, sıklık ve etki büyüklüğü gruplar arasında değiştiğinden, bunları gen düzeyinde birleştirmek istatistiksel gücü büyük ölçüde artırıyor. MuGenT, bireysel olarak anlamlı hiçbir DNA varyantı içermeyen 269 diyabet ilişkili gen belirledi; bunların 45’i daha önce fark edilmemiş bölgelerde ilaçlanabilir proteinleri kodluyordu. Genleri gerçek biyolojiyle bağlamak için xGenT yöntemi, hastalık genetiğini varyantların gen aktivitesi ve beyin dokusundaki protein bolluğu üzerindeki etkileriyle üst üste koyuyor. Alzheimer hastalığında xGenT, NTRK1 ve RIPK2 dahil olmak üzere bilinen risk bölgelerinin dışında 26 ilaçlanabilir gene dikkat çekti ve bu genlerin hangi beyin bölgelerinde ve hücre tiplerinde aktif olduğuna işaret etti.
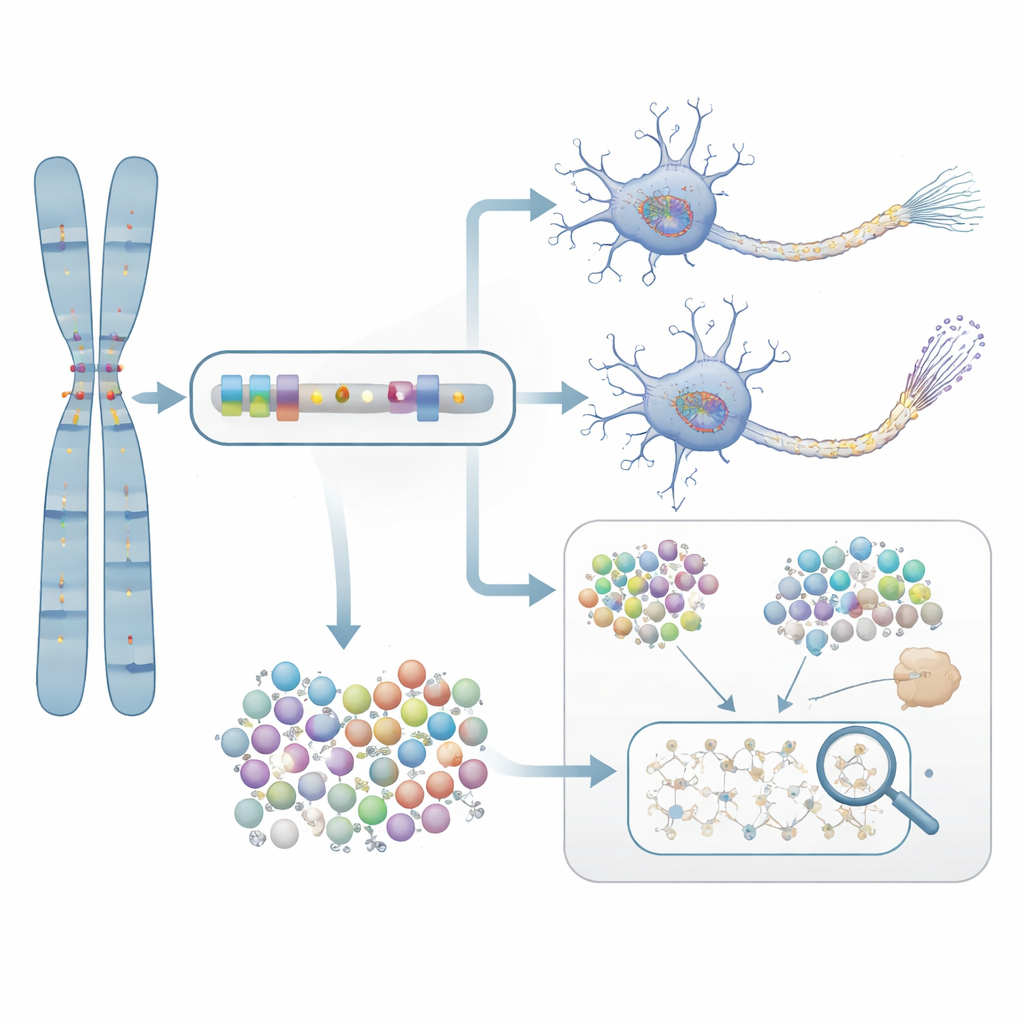
Tahminden laboratuvar kanıtına
İstatistiksel olarak işaretlenen bu genlerin gerçekten hastalık için önemli olup olmadığını sınamak üzere araştırmacılar NTRK1 üzerinde yakından çalıştı; bu gen sinir hücresi hayatta kalmasında rol oynuyor. Alzheimer hastalarından türetilen hücrelerden yetiştirilen nöronlara seçici NTRK1 engelleyici bir bileşik uyguladılar. Laboratuvarda yetiştirilen bu nöronlarda NTRK1’in inhibisyonu, Alzheimer beyinlerinde görülen düğümlenmiş protein kümeleriyle yakından ilişkili olan tau proteini üzerindeki anormal kimyasal işaretleri azalttı. Bu deney, gen-temelli istatistiklerden ilaçla hedeflenebilir bir biyolojik sürece uzanan mekanistik bir köprü sağlıyor.
Gelecekteki tedaviler için anlamı
Bir arada değerlendirildiğinde, çalışma tek tek DNA işaretleyicilerinden tüm gene kaymanın ve çeşitli popülasyonlardan ve çoklu moleküler katmanlardan yararlanmanın karmaşık hastalıklar için çok daha fazla makul ilaç hedefi ortaya çıkarabileceğini gösteriyor. Yazarlar, gerçekten önemli birçok genin hastalığı geleneksel GWAS taramalarıyla zayıf yakalanan ılımlı, dağılmış etkiler ağları aracılığıyla etkilediğini savunuyor. GenT çerçevesi ve onun çok kökenli ve moleküler uzantıları, bu gizli sinyalleri açığa çıkarmak ve daha derin deneysel testler için genleri önceliklendirmek amacıyla istatistiksel olarak sağlam bir yol sunuyor. Herhangi bir terapinin hastalara ulaşmasından önce daha fazla laboratuvar ve klinik çalışmaya ihtiyaç duyulacak olsa da, bu yaklaşım tedaviye acil ihtiyaç duyulan hastalıklarda ilaç keşfi için genetik başlangıç noktalarını önemli ölçüde genişletiyor.
Atıf: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Anahtar kelimeler: gen-temelli ilişki, Alzheimer hastalığı, tip 2 diyabet, ilaçlanabilir hedefler, çok kökenli genetik