Clear Sky Science · ar
دمج اختبارات xQTL ودراسات الترابط في جميع أنحاء الجينوم من مجموعات سكانية متنوعة يحسّن اكتشاف الجينات القابلة للعلاج
لماذا تهم الجينات للأدوية المستقبلية
كشفت علم الوراثة الحديث عن آلاف العلامات في الحمض النووي المرتبطة بالأمراض الشائعة، لكن تحويل هذه المؤشرات إلى أهداف دوائية عملية ظلّ بطيئًا ومحبِطًا. تتناول هذه الدراسة عائقًا مركزيًا: طرقنا التقليدية لقراءة الدراسات الوراثية الكبيرة غالبًا ما تفوّت الجينات التي يمكن أن تعمل عليها الأدوية فعليًا. من خلال إعادة التفكير في كيفية تحليل البيانات الوراثية عبر مجموعات سكانية متنوعة وطبقات بيولوجية متعددة، يسعى المؤلفون إلى كشف ثغرات خفية قابلة للعلاج في أمراض مثل الزهايمر والاكتئاب والفصام والسكري من النوع الثاني.
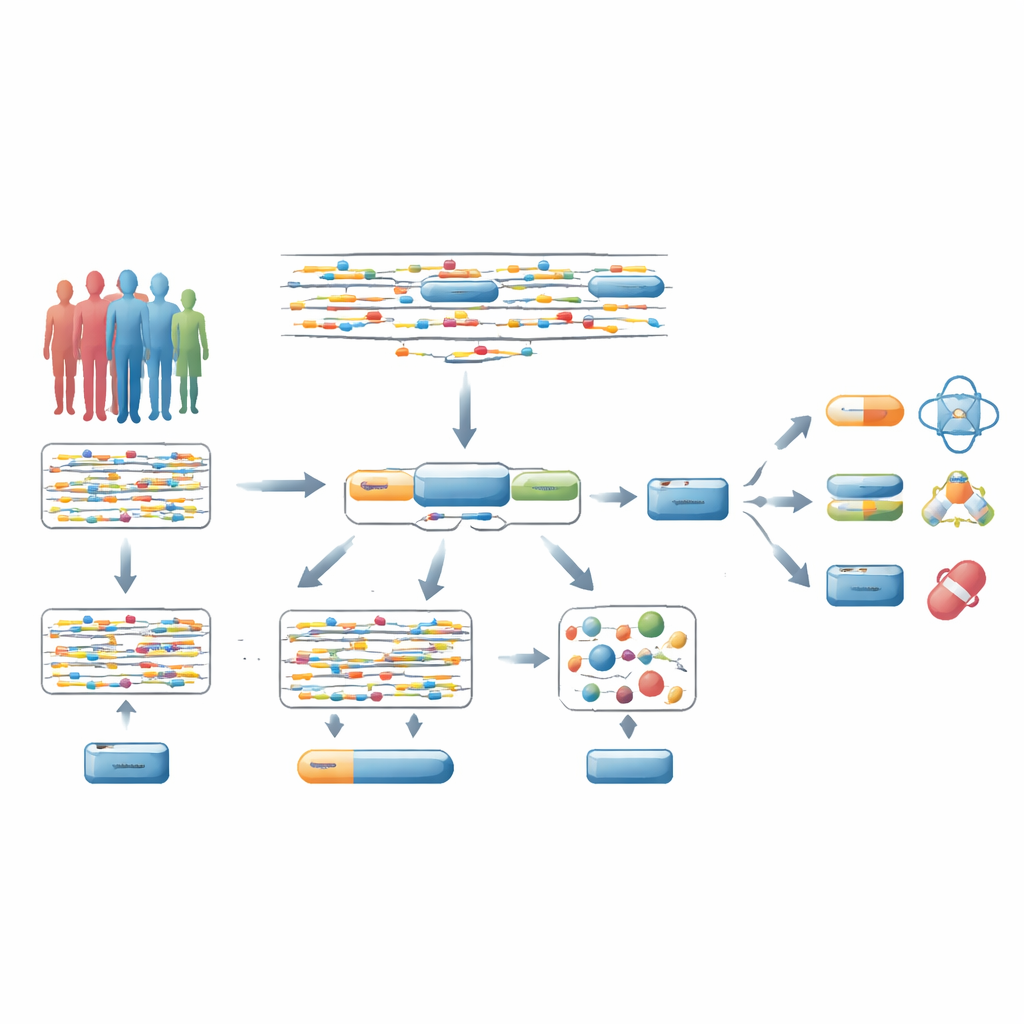
من إشارات DNA المتناثرة إلى جينات كاملة
تركّز معظم دراسات الترابط عبر الجينوم (GWAS) على ملايين التغيرات المفردة في الـDNA واحدًا تلو الآخر وتسأل ما إذا كانت كل منها مرتبطة بمرض معين. عادةً ما يفترض الباحثون بعد ذلك أن التغير الأشد ارتباطًا القريب من جين ما يشير إلى ذلك الجين. لكن هذا الاختصار غالبًا ما يكون خاطئًا: نسبة صغيرة فقط من هذه "المتغيرات القيادية" سببًا حقيقيًا للمرض، وقد تؤثر على جينات بعيدة. وبسبب ذلك، تؤدي التصحيحات الإحصائية الصارمة عبر ملايين الاختبارات إلى صعوبة كشف الجينات المسببة فعليًا للأمراض، خصوصًا تلك التي يمكن للأدوية الحالية أو المحتملة استهدافها.
مجموعة جديدة من الأدوات لقراءة الخريطة الوراثية
يقدّم المؤلفون عائلة من الاختبارات "المستندة إلى الجين"، يقودها أسلوب يسمى GenT. بدلًا من تقييم تغيرات DNA مفردة بمعزل عن غيرها، يجمع GenT كل المتغيرات ذات الصلة حول كل جين ويختبرها مجتمعة. والأهم أن الفريق وضع الأساس الرياضي لهذه الطريقة بحيث يعرفون تمامًا كيف ينبغي أن يتصرف GenT عندما لا يوجد إشارة حقيقية، متجنبين التنبيهات الكاذبة التي قد تبتلي الأساليب السابقة. وتمتد هذه الإطارية عبر امتدادات—MuGenT للبيانات متعددة الأنساب أو متعددة السمات، وxGenT لدمج مقاييس جزيئية مثل تعبير الجينات أو مستويات البروتين—مما يسمح للباحثين بدمج المعلومات عبر السكان وطبقات البيولوجيا بينما لا يزالون يعملون من ملخّصات إحصائية متاحة على نطاق واسع.
اكتشاف أهداف دوائية خفية في الدماغ والجسم
بتطبيق GenT على دراسات وراثية كبيرة لمرض الزهايمر، والتصلب الجانبي الضموري، والاكتئاب الشديد، والفصام، حلّل المؤلفون أكثر من 18,000 جين. كشفوا عن 415 جينًا تنتج بروتينات يمكن استهدافها بمركبات موجودة أو تجريبية، الكثير منها كان قد فاته طرق GWAS التقليدية. وتقع عشرات من هذه الجينات القابلة للعلاج في مناطق من الجينوم لم تظهر فيها إشارة قوية لمتغير واحد، مما يوحي بأن الخطر موزع عبر تأثيرات متواضعة متعددة تصبح مرئية فقط عند النظر إليها على مستوى الجين. ومن أمثلة بارزة SYK في مرض الزهايمر وTHRB في الفصام، وكلاهما يحظى بدعم من أعمال بيولوجية سابقة لكنه كان سابقًا دون رادار التحليلات التقليدية.
قوة التنوع والطبقات الجزيئية
يمد MuGenT هذه الاستراتيجية لدمج البيانات الوراثية من أشخاص ينحدرون من أصول أوروبية وإفريقية وشرق آسيوية وجنوب آسيوية وهِسبانية في دراسة داء السكري من النوع 2. وبما أن العديد من متغيرات الخطر مشتركة ولكنها تختلف في التواتر والقوة عبر المجموعات، فإن تجميعها على مستوى الجين يعزز القدرة الإحصائية بشكل كبير. حدّد MuGenT 269 جينًا مرتبطًا بالسكري تفتقر لأي متغيرات DNA فردية ذات دلالة، 45 منها تشفر بروتينات قابلة للعلاج في مناطق لم تكن متوقعة سابقًا. ولربط الجينات بالبيولوجيا الفعلية، تراكب أسلوب xGenT جينات المرض مع قياسات لكيفية تأثير المتغيرات على نشاط الجينات ووفرة البروتين في أنسجة الدماغ. في مرض الزهايمر، أبرز xGenT ستة وعشرين جينًا قابلاً للعلاج خارج مناطق المخاطر المعروفة، بما في ذلك NTRK1 وRIPK2، وأشار إلى مناطق دماغية وأنواع خلوية محددة تكون فيها هذه الجينات نشطة.
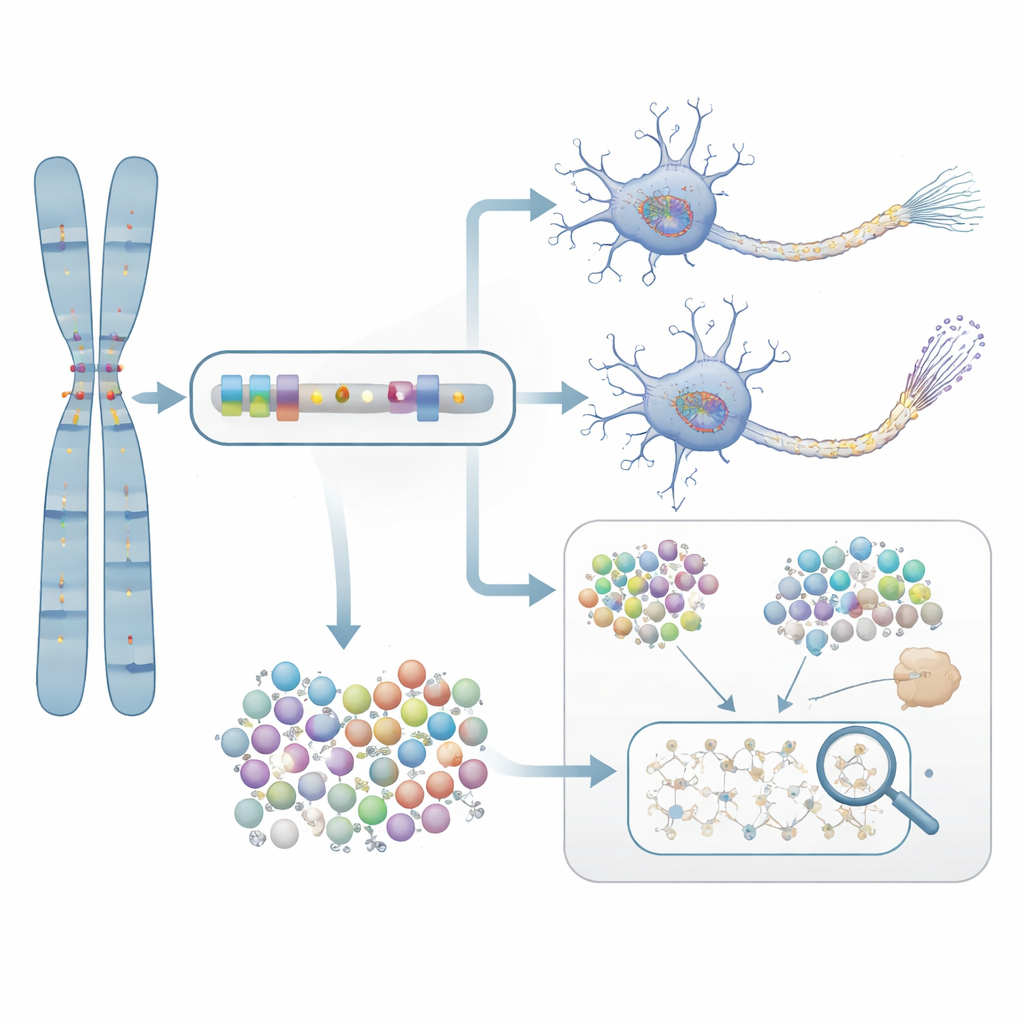
من التنبؤ إلى الدليل المخبري
لاختبار ما إذا كانت هذه الجينات التي أشارت إليها الإحصاءات مهمة فعلاً للمرض، ركّز الباحثون على NTRK1، جين يساهم في بقاء الخلايا العصبية. عالجوا الخلايا العصبية المزروعة من خلايا مرضى الزهايمر بمركب انتقائي يثبط NTRK1. في هذه الخلايا العصبية المزروعة معملًا، أدى تثبيط NTRK1 إلى تقليل الطبعات الكيميائية غير الطبيعية على بروتين تاو—تغيّرات مرتبطة ارتباطًا وثيقًا بتكتلات البروتين الملتوية الملاحظة في أدمغة مرضى الزهايمر. يوفر هذا التجربة جسرًا آليًا من الإحصاءات المستندة إلى الجينات إلى عملية بيولوجية يمكن، من الناحية النظرية، استهدافها دوائيًا.
ماذا يعني هذا للعلاجات المستقبلية
عند النظر إلى العمل مجتمعة، يظهر أن تحويل التركيز من علامات DNA المفردة إلى جينات كاملة، مع الاستفادة من بيانات مجموعات سكانية متنوعة وطبقات جزيئية متعددة، يمكن أن يكشف عن عدد أكبر بكثير من الأهداف الدوائية المحتملة للأمراض المعقدة. يجادل المؤلفون بأن العديد من الجينات الهامة حقًا تؤثر على المرض عبر شبكات من التأثيرات المتواضعة الموزعة التي لا تلتقطها فحوصات GWAS التقليدية بشكل جيد. توفّر إطارية GenT، مع امتداداتها متعددة الأنساب والجزيئية، طريقًا إحصائيًا صارمًا لكشف هذه الإشارات الخفية وترتيب أولويات الجينات للاختبارات التجريبية الأعمق. وبينما ستظل هناك حاجة لمزيد من الدراسات المخبرية والسريرية قبل أن يصل أي علاج إلى المرضى، توسع هذه المقاربة بشكل ملحوظ نقاط الانطلاق الوراثية لاكتشاف الأدوية لحالات بحاجة ملحة لعلاجات أفضل.
الاستشهاد: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
الكلمات المفتاحية: الارتباط المستند إلى الجينات, مرض الزهايمر, السكري من النمط 2, الأهداف القابلة للعلاج الدوائي, علم الوراثة عبر الأنساب المتعددة