Clear Sky Science · ja
多様な集団のxQTLとゲノムワイド関連解析を組み合わせることで薬剤標的となりうる遺伝子の発見を向上させる
医薬品のために遺伝子が重要な理由
現代の遺伝学は、一般的な疾患に関連する何千ものDNAマーカーを明らかにしてきましたが、そうした手がかりを実際の薬剤標的に結びつける作業は遅々として進んでいます。本研究は中心的なボトルネックに取り組んでいます:大規模遺伝学研究の標準的な読み取り方では、薬が実際に作用し得る遺伝子を見落とすことが多いのです。多様な集団と生物学の複数の層にまたがって遺伝データの解析法を再考することで、著者らはアルツハイマー病、うつ病、統合失調症、2型糖尿病といった疾患における、隠れたが薬剤で狙える弱点を明らかにしようとしています。
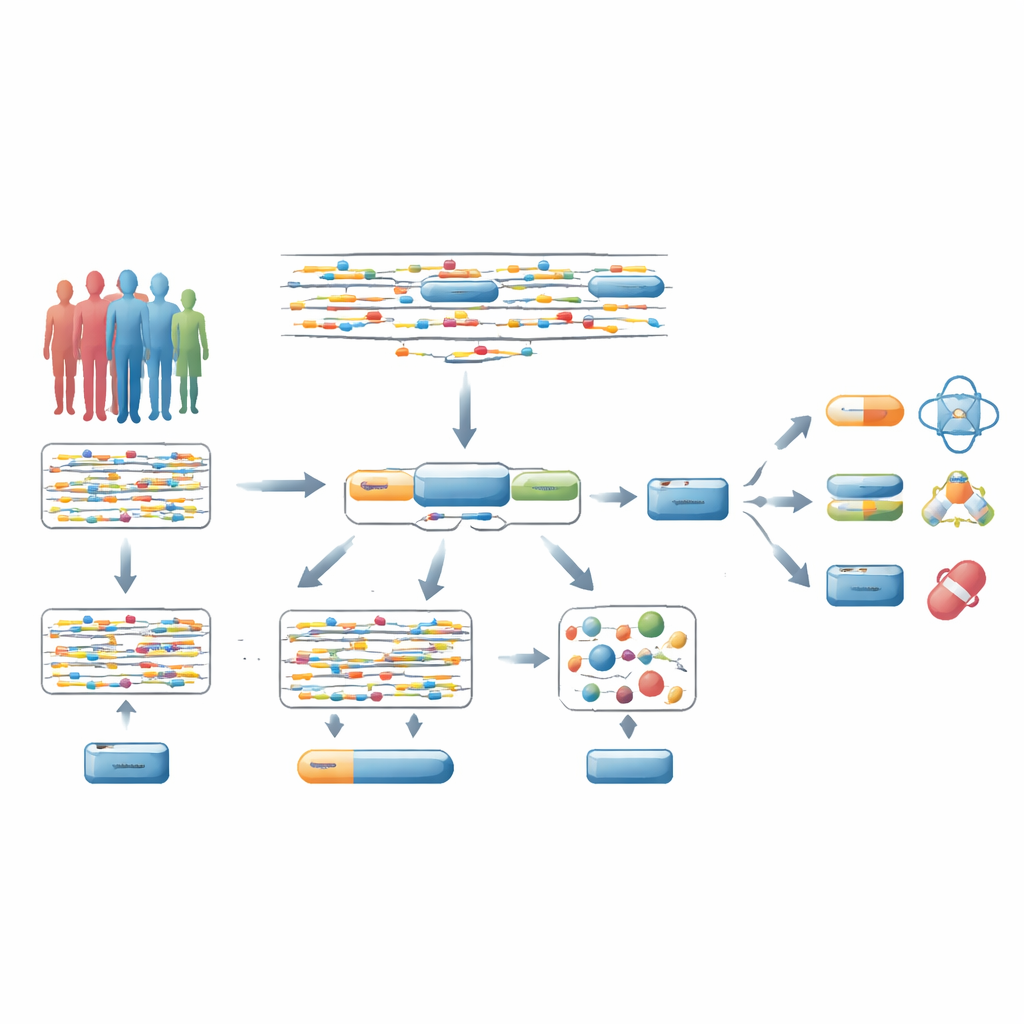
点在するDNA信号から遺伝子全体へ
ほとんどのゲノムワイド関連解析(GWAS)は、何百万もの単一のDNA変化を個別に見て、それぞれが疾患と関連するかを調べます。通常、研究者は遺伝子近傍で最も強く関連する変異がその遺伝子を指していると仮定します。しかしこの近道はしばしば誤りです:これらの「リード」変異のごく一部しか実際に疾患を引き起こすわけではなく、遠く離れた遺伝子に影響を与えることもあります。このため、何百万もの検定に対する厳しい統計的補正が必要となり、特に既存または潜在的薬剤で標的にできる実際の疾患遺伝子を見つけるのが難しくなります。
遺伝地図を読むための新しいツール群
著者らは「遺伝子ベース」の検定群を導入し、その中心にGenTという方法を据えています。単一のDNA変化を個別に評価する代わりに、GenTは各遺伝子の周辺にある関連変異をすべてまとめて一緒に検定します。重要なのは、チームが基礎となる数理を精緻化し、真のシグナルがない場合にGenTがどのように振る舞うべきかを正確に把握していることです。これにより、以前の遺伝子ベース手法で問題となった誤警報を避けられます。この枠組みの拡張であるMuGenT(多祖先または多表現型データ向け)やxGenT(遺伝子発現やタンパク質量などの分子リードアウトを統合)は、広く利用可能なサマリ統計量を用いながら、集団間や生物学の層を横断して情報を結合できるようにします。
脳と体における隠れた薬剤標的の発見
著者らはGenTをアルツハイマー病、筋萎縮性側索硬化症(ALS)、大うつ病、統合失調症の大規模遺伝学研究に適用し、18,000を超える遺伝子を解析しました。その結果、既存または実験的化合物で狙えるタンパク質をコードする415の遺伝子を発見し、その多くは標準的なGWAS手法では見逃されていました。これらの薬剤標的可能な遺伝子のうち数十は、単一の変異で強い信号を示さないゲノム領域にあり、リスクが多数の控えめな効果に分散しているため、遺伝子レベルで見たときにのみ可視化されることを示唆しています。注目すべき例としては、アルツハイマー病に対するSYKや統合失調症に対するTHRBがあり、いずれも以前の生物学的知見に支持されながら従来の解析では見過ごされていました。
多様性と分子層の力
MuGenTはこの戦略を拡張して、ヨーロッパ系、アフリカ系、東アジア系、南アジア系、ヒスパニック系の人々の遺伝データを2型糖尿病と組み合わせます。多くのリスク変異は集団間で共有されているものの頻度や効果の大きさが異なるため、遺伝子レベルでそれらをプールすることは統計的検出力を大幅に高めます。MuGenTは、個別には有意なDNA変異を欠く269の糖尿病関連遺伝子を同定し、そのうち45はこれまで注目されていなかった領域に位置する薬剤標的可能なタンパク質をコードしていました。遺伝子を実際の生物学に結びつけるために、xGenTは病気の遺伝学に変異が遺伝子活性や脳組織のタンパク質量に与える影響の測定値を重ね合わせます。アルツハイマー病では、xGenTは既知のリスク領域外にある26の薬剤標的可能な遺伝子を強調し、NTRK1やRIPK2を含め、これらが活性を示す特定の脳領域や細胞型を示しました。
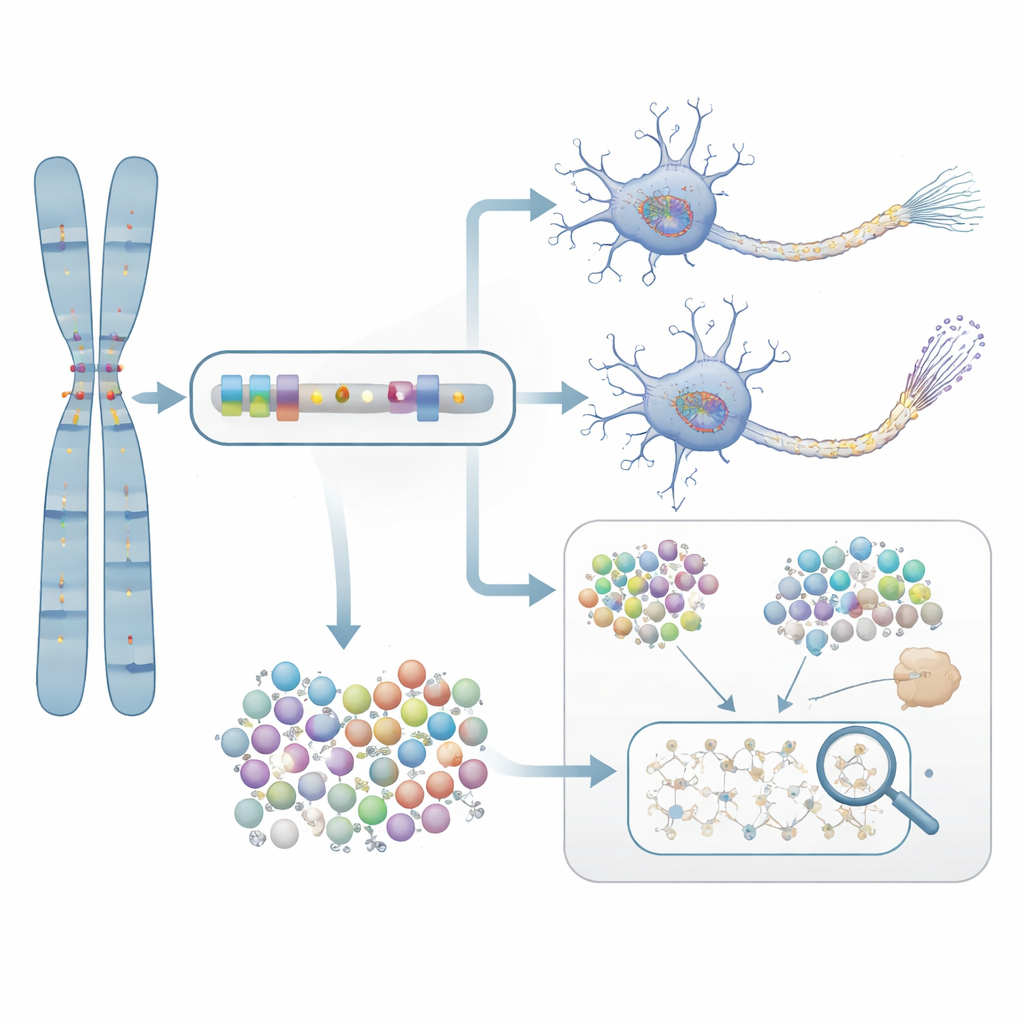
予測から実験室での証拠へ
これらの統計的に示唆された遺伝子が実際に疾患に重要かを検証するため、研究者らは神経細胞の生存に関わる遺伝子NTRK1に注目しました。彼らはアルツハイマー病患者の細胞から育てたニューロンに選択的なNTRK1阻害化合物を投与しました。これらの培養ニューロンでは、NTRK1を抑制するとタウタンパク質の異常な化学修飾が減少し、これはアルツハイマー病脳に見られる絡み合ったタンパク質塊と密接に関連する変化です。この実験は、遺伝子ベースの統計結果から薬剤で標的にし得る生物学的プロセスへの機構的な橋渡しを行うものです。
将来の治療への意義
総覧すると、本研究は単一のDNAマーカーから遺伝子全体へと注目を移し、多様な集団と複数の分子層のデータを活用することで、複雑な疾患に対するより多くの妥当な薬剤標的を明らかにできることを示しています。著者らは、多くの真に重要な遺伝子は控えめで分散した効果のネットワークを通じて疾患に影響を与え、従来のGWASスキャンでは十分に捉えられないと主張します。GenTの枠組みとその多祖先・分子拡張は、これらの隠れたシグナルを統計的に厳密な方法で露出させ、より深い実験的検証に値する遺伝子の優先順位付けを可能にします。どの治療法が患者に届けられるかはさらに実験室や臨床での検証が必要ですが、このアプローチは切実により良い治療法が求められる疾患に対する薬剤開発の出発点を大幅に広げます。
引用: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
キーワード: 遺伝子ベースの関連解析, アルツハイマー病, 2型糖尿病, 薬剤標的可能性, 多祖先遺伝学