Clear Sky Science · it
Combinare xQTL e studi di associazione genome-wide in popolazioni diverse migliora la scoperta di geni bersaglio di farmaci
Perché i geni sono importanti per i medicinali del futuro
La genetica moderna ha identificato migliaia di marcatori del DNA associati a malattie comuni, ma trasformare questi indizi in veri bersagli farmacologici è stato sorprendentemente lento. Questo studio affronta un collo di bottiglia centrale: i nostri modi standard di leggere gli ampi studi genetici spesso non riescono a individuare i geni su cui i farmaci possono realmente intervenire. Ripensando l’analisi dei dati genetici attraverso popolazioni diverse e livelli biologici multipli, gli autori mirano a scoprire punti deboli nascosti, ma farmacologicamente sfruttabili, in malattie come Alzheimer, depressione, schizofrenia e diabete di tipo 2.
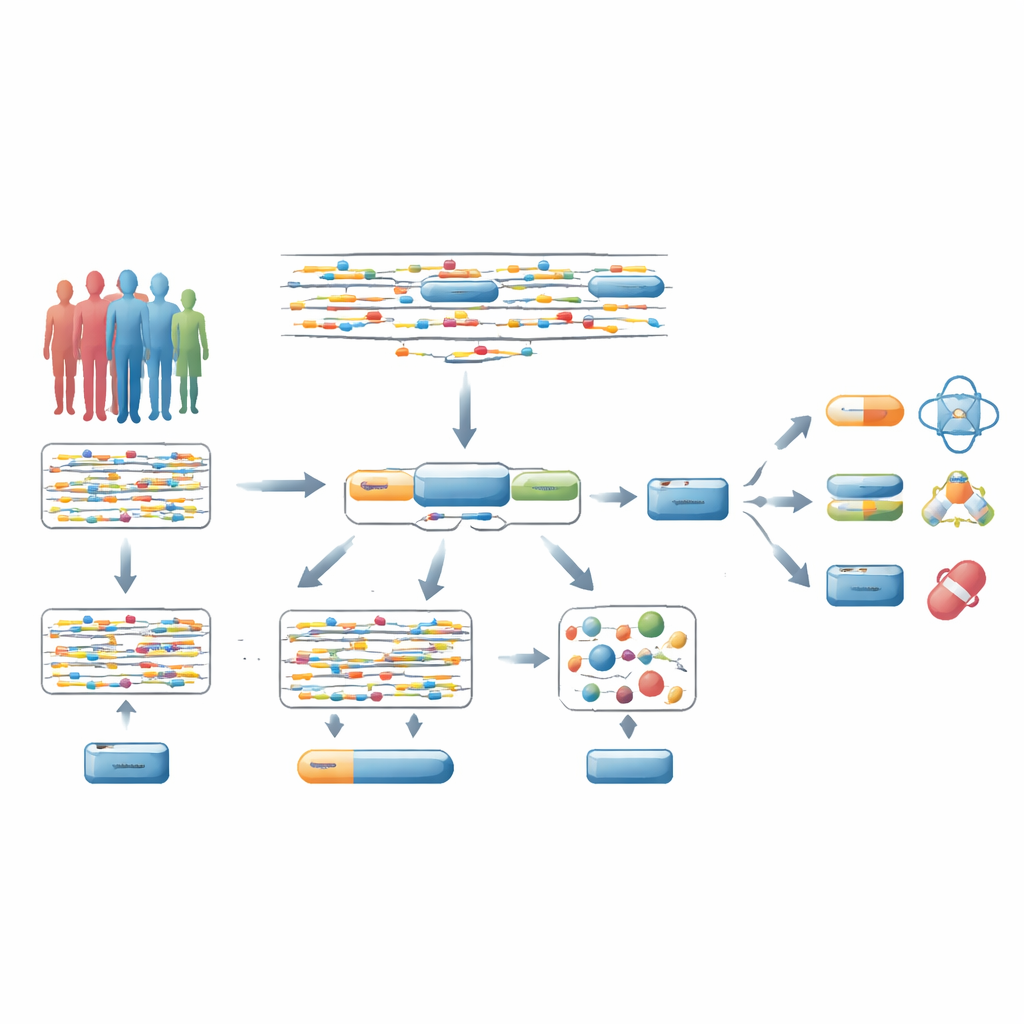
Da segnali di DNA sparsi a geni interi
La maggior parte degli studi di associazione genome-wide (GWAS) analizza milioni di singoli cambiamenti del DNA uno per uno e verifica se ciascuno è collegato a una malattia. Tipicamente, i ricercatori poi assumono che la variante più fortemente associata vicino a un gene indichi quel gene. Ma questa scorciatoia spesso è sbagliata: solo una piccola frazione di queste varianti “lead” causa realmente la malattia, e possono influenzare geni lontani. Per questo motivo, le stringenti correzioni statistiche applicate su milioni di test rendono difficile trovare i veri geni della malattia, in particolare quelli che farmaci esistenti o potenziali possono prendere di mira.
Un nuovo set di strumenti per leggere la mappa genetica
Gli autori presentano una famiglia di test «basati sui geni», guidata da un metodo chiamato GenT. Invece di valutare le singole varianti del DNA in isolamento, GenT raggruppa tutte le varianti rilevanti attorno a ciascun gene e le testa insieme. In modo cruciale, il gruppo ha messo a punto la matematica sottostante in modo da sapere esattamente come GenT dovrebbe comportarsi in assenza di un segnale reale, evitando i falsi allarmi che possono affliggere approcci basati sui geni precedenti. Le estensioni di questo quadro—MuGenT per dati multi-ancestrali o multi-trait e xGenT per integrare misure molecolari come l’espressione genica o i livelli proteici—consentono ai ricercatori di combinare informazioni attraverso popolazioni e strati biologici pur lavorando con statistiche di sintesi ampiamente disponibili.
Scoprire bersagli farmacologici nascosti nel cervello e nel corpo
Applicando GenT a grandi studi genetici sulla malattia di Alzheimer, la sclerosi laterale amiotrofica, la depressione maggiore e la schizofrenia, gli autori hanno analizzato oltre 18.000 geni. Hanno individuato 415 geni i cui prodotti proteici possono essere bersagliati da composti esistenti o sperimentali, molti dei quali erano stati mancati dai metodi standard dei GWAS. Dozzine di questi geni farmacologicamente sfruttabili si trovano in regioni del genoma che non mostravano segnali forti a livello di singola variante, suggerendo che il rischio è distribuito su molti effetti modesti che diventano visibili solo se osservati a livello genico. Esempi notevoli includono SYK per la malattia di Alzheimer e THRB per la schizofrenia, entrambi supportati da precedenti evidenze biologiche ma finora sfuggiti alle analisi convenzionali.
La potenza della diversità e dei livelli molecolari
MuGenT estende questa strategia per combinare dati genetici di persone di ascendenza europea, africana, dell’Asia orientale, dell’Asia meridionale e ispano-latina con il diabete di tipo 2. Poiché molte varianti di rischio sono condivise ma variano in frequenza e intensità tra i gruppi, raggrupparle a livello genico aumenta notevolmente la potenza statistica. MuGenT ha identificato 269 geni associati al diabete privi di singole varianti del DNA statisticamente significative, 45 dei quali codificano proteine farmacologicamente bersagliabili in regioni prima insospettate. Per collegare i geni alla biologia effettiva, il metodo xGenT sovrappone la genetica della malattia a misure di come le varianti influenzano l’attività genica e l’abbondanza proteica nei tessuti cerebrali. Nella malattia di Alzheimer, xGenT ha evidenziato 26 geni farmacologicamente sfruttabili al di fuori delle regioni di rischio note, inclusi NTRK1 e RIPK2, e ha indicato specifiche regioni cerebrali e tipi cellulari in cui sono attivi.
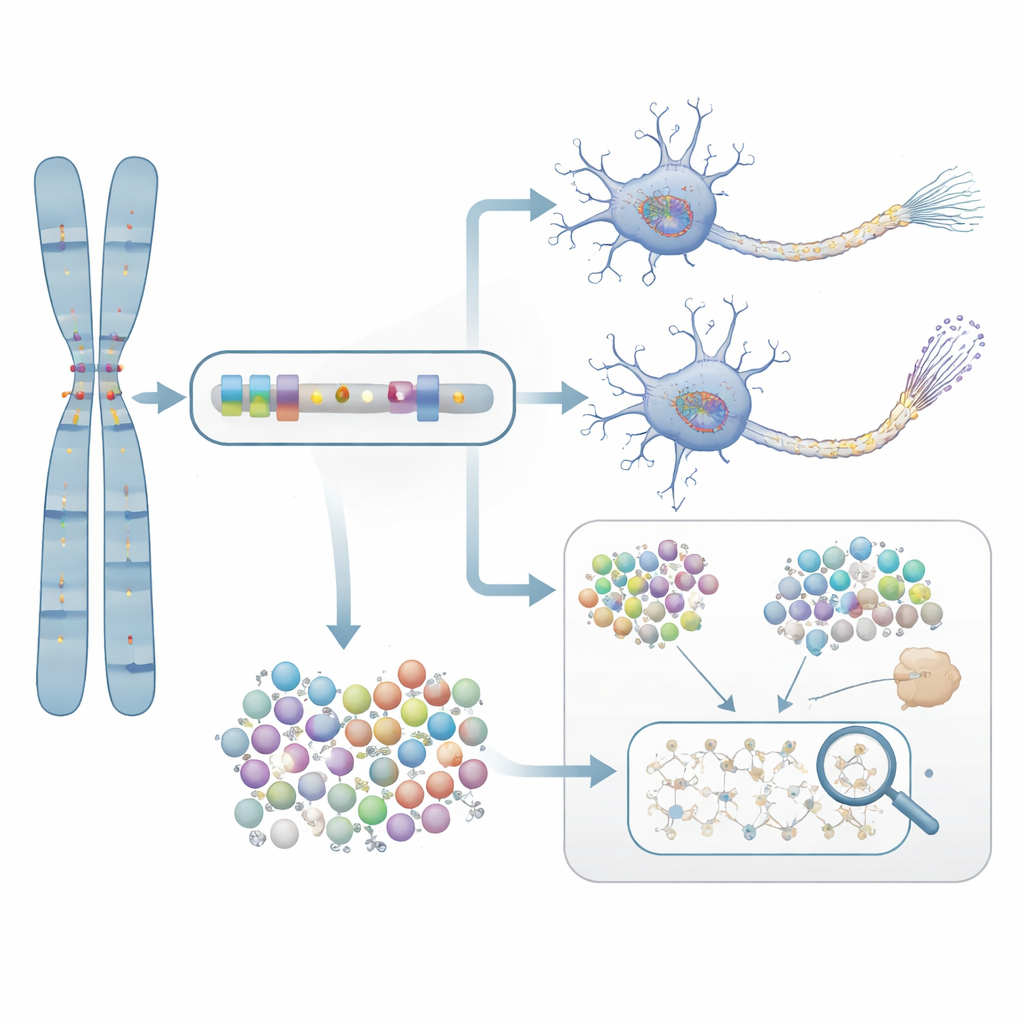
Dalla previsione all’evidenza di laboratorio
Per verificare se questi geni segnalati statisticamente contano davvero nella malattia, i ricercatori si sono concentrati su NTRK1, un gene coinvolto nella sopravvivenza dei neuroni. Hanno trattato neuroni coltivati a partire dalle cellule di pazienti con Alzheimer con un composto selettivo inibitore di NTRK1. In questi neuroni coltivati in laboratorio, l’inibizione di NTRK1 ha ridotto marcature chimiche anomale sulla proteina tau—modifiche strettamente legate agli ammassi proteici intrecciati osservati nei cervelli affetti da Alzheimer. Questo esperimento fornisce un ponte meccanicistico dalle statistiche basate sui geni a un processo biologico che, in linea di principio, può essere preso di mira da farmaci.
Cosa significa per i trattamenti futuri
Considerato nel suo insieme, il lavoro mostra che spostare l’attenzione dai singoli marcatori del DNA ai geni interi, attingendo a dati provenienti da popolazioni diverse e da più livelli molecolari, può rivelare molti più potenziali bersagli farmacologici per malattie complesse. Gli autori sostengono che molti geni realmente importanti influenzano la malattia attraverso reti di effetti modesti e distribuiti che sono mal rappresentati dalle scansioni GWAS tradizionali. Il loro quadro GenT, insieme alle estensioni multi-ancestrali e molecolari, offre un modo statisticamente rigoroso per far emergere questi segnali nascosti e prioritizzare i geni per approfondimenti sperimentali. Pur richiedendo ulteriori studi di laboratorio e clinici prima che qualsiasi terapia raggiunga i pazienti, questo approccio amplia significativamente i punti di partenza genetici per la scoperta di farmaci in condizioni che richiedono con urgenza terapie migliori.
Citazione: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Parole chiave: associazione basata sui geni, Malattia di Alzheimer, diabete di tipo 2, bersagli farmacologici, genetica multi-ancestrale