Clear Sky Science · sv
Kombinera xQTL och genomomfattande associationstudier från olika populationer förbättrar upptäckten av läkemedelsbara gener
Varför gener spelar roll för framtida läkemedel
Modern genetik har avslöjat tusentals DNA-markörer kopplade till vanliga sjukdomar, men att omvandla dessa ledtrådar till faktiska läkemedelsmål har gått frustrerande långsamt. Denna studie tar sig an en central flaskhals: våra vanliga sätt att läsa stora genetiska studier missar ofta de gener som läkemedel faktiskt kan påverka. Genom att ompröva hur man analyserar genetiska data över olika populationer och biologiska nivåer vill författarna avslöja dolda, men läkemedelsbara, svagheter i sjukdomar som Alzheimers, depression, schizofreni och typ 2-diabetes.
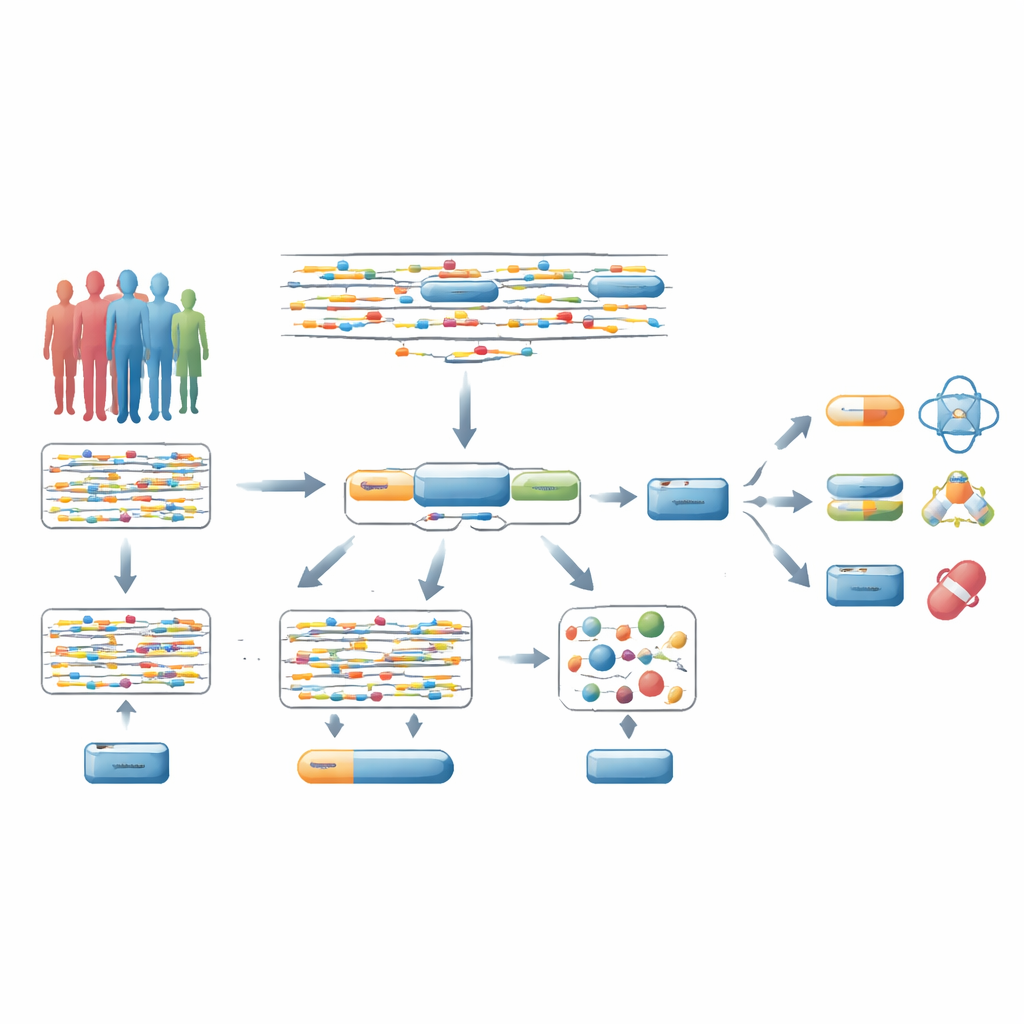
Från spridda DNA-signaler till hela gener
De flesta genomomfattande associationsstudier (GWAS) undersöker miljontals enskilda DNA-förändringar en och en och frågar om var och en är kopplad till en sjukdom. Vanligtvis antar forskare sedan att den starkast associerade DNA-förändringen nära en gen pekar mot den genen. Men den genvägen är ofta felaktig: endast en liten andel av dessa ”lead”-varianter orsakar verkligen sjukdom, och de kan påverka avlägsna gener. På grund av detta sprids strikta statistiska korrigeringar över miljontals tester, vilket gör det svårt att hitta verkliga sjukdomsgener, särskilt sådana som befintliga eller potentiella läkemedel kan rikta in sig på.
En ny uppsättning verktyg för att läsa den genetiska kartan
Författarna introducerar en familj av ”genbaserade” tester, lett av en metod kallad GenT. Istället för att bedöma enskilda DNA-förändringar isolerat grupperar GenT alla relevanta varianter runt varje gen och testar dem tillsammans. Avgörande är att teamet härlett den underliggande matematiken så att de vet exakt hur GenT bör bete sig när det inte finns någon verklig signal, vilket undviker falsklarm som kan plåga tidigare genbaserade tillvägagångssätt. Förlängningar av detta ramverk—MuGenT för data med flera härkomster eller flera egenskaper, och xGenT för att integrera molekylära mätningar som genuttryck eller proteinnivåer—låter forskare kombinera information över populationer och biologiska lager samtidigt som de arbetar från sammanfattande statistik som är allmänt tillgänglig.
Hitta dolda läkemedelsmål i hjärna och kropp
När GenT tillämpades på stora genetiska studier av Alzheimers sjukdom, amyotrofisk lateralskleros, svår depression och schizofreni analyserade författarna över 18 000 gener. De upptäckte 415 gener vars proteiner kan riktas av befintliga eller experimentella föreningar, många som standard GWAS-metoder hade missat. Flera av dessa läkemedelsbara gener ligger i regioner av genomet som inte visade någon stark signal från enskilda varianter, vilket tyder på att risken är utspridd över många måttliga effekter som först blir synliga när man ser till gen-nivån. Noterbara exempel inkluderar SYK för Alzheimers sjukdom och THRB för schizofreni, båda stödda av tidigare biologiskt arbete men tidigare under radarn för konventionella analyser.
Kraften i mångfald och molekylära lager
MuGenT förlänger denna strategi för att kombinera genetiska data från personer med europeisk, afrikansk, östasiatisk, sydasiatisk och latinamerikansk härkomst med typ 2-diabetes. Eftersom många riskvarianter delas men varierar i frekvens och styrka mellan grupper, ger sammanslagning på gen-nivå en stor ökning av statistisk styrka. MuGenT identifierade 269 diabetesassocierade gener utan några individuellt signifikanta DNA-varianter, varav 45 kodar för läkemedelsbara proteiner i tidigare oidentifierade områden. För att koppla gener till faktisk biologi överlappar xGenT sjukdomsgenetiken med mätningar av hur varianter påverkar genaktivitet och proteinabundans i hjärnvävnader. I Alzheimers sjukdom framhöll xGenT 26 läkemedelsbara gener utanför kända riskregioner, inklusive NTRK1 och RIPK2, och pekade på specifika hjärnregioner och celltyper där de är aktiva.
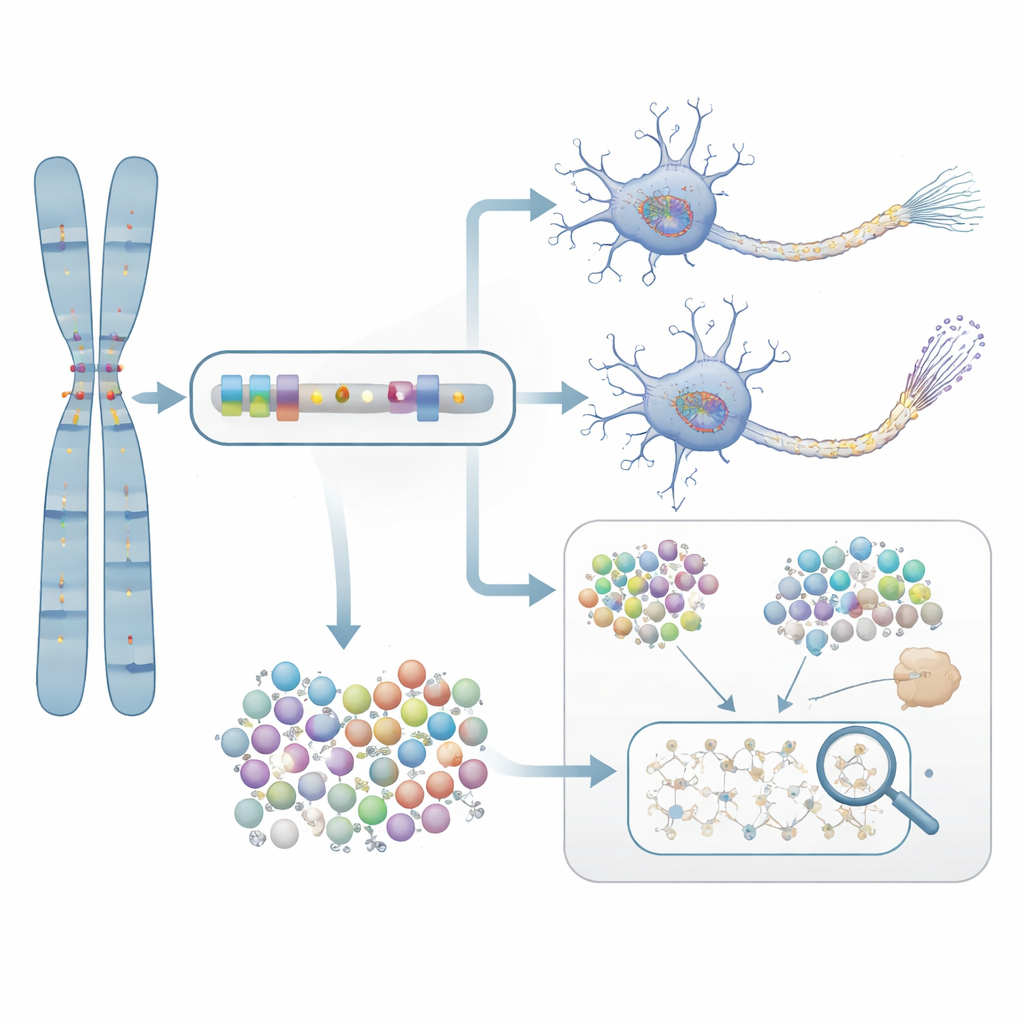
Från prediktion till laboratoriebevis
För att testa om dessa statistiskt flaggade gener verkligen spelar roll för sjukdom fördjupade forskarna studien kring NTRK1, en gen involverad i nervcellsöverlevnad. De behandlade neuroner odlade från celler från Alzheimerspatienter med en selektiv NTRK1-blockerande förening. I dessa laboratorieodlade neuroner minskade hämning av NTRK1 onormala kemiska märkningar på tau-proteinet—förändringar starkt kopplade till de trasslade proteinansamlingar som ses i Alzheimers hjärnor. Denna experimentella observation ger en mekanistisk bro från de genbaserade statistikerna till en biologisk process som i princip kan riktas med läkemedel.
Vad detta betyder för framtida behandlingar
Tillsammans visar arbetet att en förskjutning av fokus från enskilda DNA-markörer till hela gener, samtidigt som man utnyttjar data från olika populationer och flera molekylära lager, kan avslöja många fler trovärdiga läkemedelsmål för komplexa sjukdomar. Författarna menar att många verkligt viktiga gener påverkar sjukdom via nätverk av måttliga, utspridda effekter som fångas dåligt av traditionella GWAS-skanningar. Deras GenT-ramverk, tillsammans med dess multi-härkomst- och molekylära förlängningar, erbjuder ett statistiskt rigoröst sätt att exponera dessa dolda signaler och prioritera gener för djupare experimentell prövning. Även om ytterligare laboratorie- och kliniska studier krävs innan någon terapi når patienter, utvidgar detta tillvägagångssätt avsevärt de genetiska utgångspunkterna för läkemedelsupptäckt i tillstånd som akut behöver bättre behandlingar.
Citering: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Nyckelord: genbaserad association, Alzheimers sjukdom, typ 2-diabetes, läkemedelsbara mål, genetik från flera härkomster