Clear Sky Science · pt
Combinando xQTL e estudos de associação genômica de populações diversas melhora a descoberta de genes atrizáveis
Por que os genes importam para os medicamentos do futuro
A genética moderna descobriu milhares de marcadores de DNA ligados a doenças comuns, mas transformar essas pistas em alvos reais de medicamentos tem sido frustrantemente lento. Este estudo enfrenta um gargalo central: nossas formas padrão de interpretar grandes estudos genéticos frequentemente deixam de identificar os genes sobre os quais os medicamentos podem realmente agir. Repensando como analisar dados genéticos entre populações diversas e camadas biológicas, os autores buscam revelar pontos fracos ocultos, porém atrizáveis, em doenças como Alzheimer, depressão, esquizofrenia e diabetes tipo 2.
De sinais de DNA dispersos para genes inteiros
A maioria dos estudos de associação genômica (GWAS) analisa milhões de mudanças individuais no DNA uma a uma e pergunta se cada uma está ligada a uma doença. Tipicamente, os pesquisadores pressupõem que a variação mais fortemente associada próxima a um gene aponta para esse gene. Mas esse atalho costuma falhar: apenas uma pequena fração dessas variantes “líderes” realmente causa a doença, e elas podem influenciar genes distantes. Por causa disso, correções estatísticas rigorosas distribuídas por milhões de testes dificultam encontrar genes verdadeiramente envolvidos na doença, especialmente aqueles que medicamentos existentes ou potenciais poderiam atingir.
Um novo conjunto de ferramentas para ler o mapa genético
Os autores apresentam uma família de testes “baseados em genes”, liderada por um método chamado GenT. Em vez de avaliar mudanças individuais do DNA isoladamente, o GenT agrupa todas as variantes relevantes ao redor de cada gene e as testa em conjunto. Crucialmente, a equipe trabalhou a matemática subjacente para saber exatamente como o GenT deve se comportar quando não há sinal real, evitando falsos positivos que podem afetar abordagens anteriores baseadas em genes. Extensões desse quadro — MuGenT para dados multi-ancestrais ou multi-traço, e xGenT para integrar medidas moleculares como expressão gênica ou níveis proteicos — permitem que os pesquisadores combinem informações entre populações e camadas biológicas mantendo o uso de estatísticas resumidas amplamente disponíveis.
Encontrando alvos farmacológicos ocultos no cérebro e no corpo
Aplicando o GenT a grandes estudos genéticos de doença de Alzheimer, esclerose lateral amiotrófica, depressão major e esquizofrenia, os autores analisaram mais de 18.000 genes. Eles identificaram 415 genes cujos produtos proteicos podem ser alvo de compostos existentes ou experimentais, muitos dos quais métodos GWAS padrão haviam perdido. Dezenas desses genes atrizáveis estão em regiões do genoma que não exibiam sinal forte em variantes individuais, sugerindo que o risco está espalhado por muitos efeitos modestos que só se tornam visíveis quando vistos ao nível do gene. Exemplos notáveis incluem SYK para Alzheimer e THRB para esquizofrenia, ambos apoiados por trabalhos biológicos prévios, mas anteriormente abaixo do radar das análises convencionais.
O poder da diversidade e das camadas moleculares
O MuGenT estende essa estratégia para combinar dados genéticos de pessoas de ascendência europeia, africana, leste asiática, sul-asiática e hispânica com o diabetes tipo 2. Como muitas variantes de risco são compartilhadas mas variam em frequência e magnitude entre grupos, agregá-las ao nível do gene aumenta muito o poder estatístico. O MuGenT identificou 269 genes associados ao diabetes sem variantes de DNA individualmente significativas, dos quais 45 codificam proteínas atrizáveis em regiões até então não suspeitas. Para conectar genes à biologia real, o método xGenT sobrepõe a genética da doença com medidas de como variantes afetam a atividade gênica e a abundância proteica em tecidos cerebrais. Na doença de Alzheimer, o xGenT destacou 26 genes atrizáveis fora de regiões de risco conhecidas, incluindo NTRK1 e RIPK2, e indicou regiões cerebrais e tipos celulares específicos onde eles são ativos.
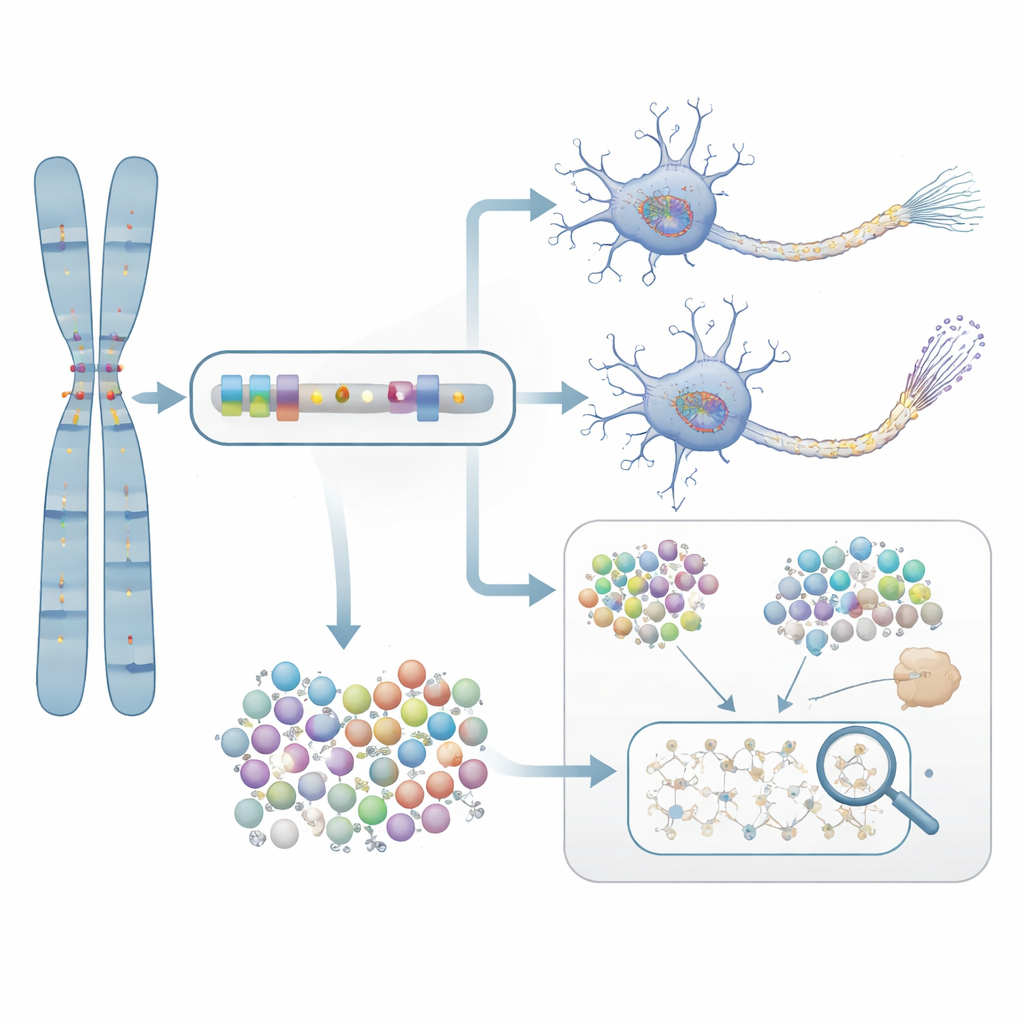
Da predição para a evidência em laboratório
Para testar se esses genes sinalizados estatisticamente realmente importam para a doença, os pesquisadores concentraram-se em NTRK1, um gene envolvido na sobrevivência de neurônios. Eles trataram neurônios cultivados a partir de células de pacientes com Alzheimer com um composto seletivo bloqueador de NTRK1. Nesses neurônios cultivados, a inibição de NTRK1 reduziu marcas químicas anormais na proteína tau — alterações fortemente associadas aos emaranhados proteicos observados nos cérebros de Alzheimer. Esse experimento fornece uma ponte mecanicista das estatísticas baseadas em genes para um processo biológico que, em princípio, pode ser alvo de medicamentos.
O que isso significa para tratamentos futuros
Visto em conjunto, o trabalho mostra que mudar o foco de marcadores de DNA individuais para genes inteiros, ao mesmo tempo em que se aproveita dados de populações diversas e múltiplas camadas moleculares, pode revelar muitos mais alvos plausíveis de medicamentos para doenças complexas. Os autores argumentam que muitos genes realmente importantes influenciam a doença por redes de efeitos modestos e distribuídos, que são mal capturados por varreduras GWAS tradicionais. Seu arcabouço GenT, juntamente com suas extensões multi-ancestrais e moleculares, oferece uma maneira estatisticamente rigorosa de expor esses sinais ocultos e priorizar genes para testes experimentais mais aprofundados. Embora mais estudos laboratoriais e clínicos sejam necessários antes que qualquer terapia chegue aos pacientes, essa abordagem amplia significativamente os pontos de partida genéticos para a descoberta de medicamentos em condições que necessitam urgentemente de tratamentos melhores.
Citação: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Palavras-chave: associação baseada em genes, Doença de Alzheimer, diabetes tipo 2, alvos farmacológicos, genética multi-ancestral