Clear Sky Science · pl
Łączenie badań xQTL i badań asocjacyjnych obejmujących cały genom z różnych populacji poprawia wykrywanie genów możliwych do leczenia
Dlaczego geny mają znaczenie dla przyszłych leków
Współczesna genetyka odkryła tysiące markerów DNA powiązanych z powszechnymi chorobami, lecz przekucie tych wskazówek w rzeczywiste cele lekowe przebiega frustrująco wolno. To badanie podejmuje kluczowy wątek: nasze standardowe sposoby analizowania dużych badań genetycznych często pomijają geny, na które leki mogą rzeczywiście działać. Przez przemyślenie sposobu analizowania danych genetycznych w różnych populacjach i na różnych poziomach biologii autorzy dążą do ujawnienia ukrytych, ale możliwych do zaadresowania farmakologicznie, słabych punktów w chorobach takich jak Alzheimer, depresja, schizofrenia i cukrzyca typu 2.
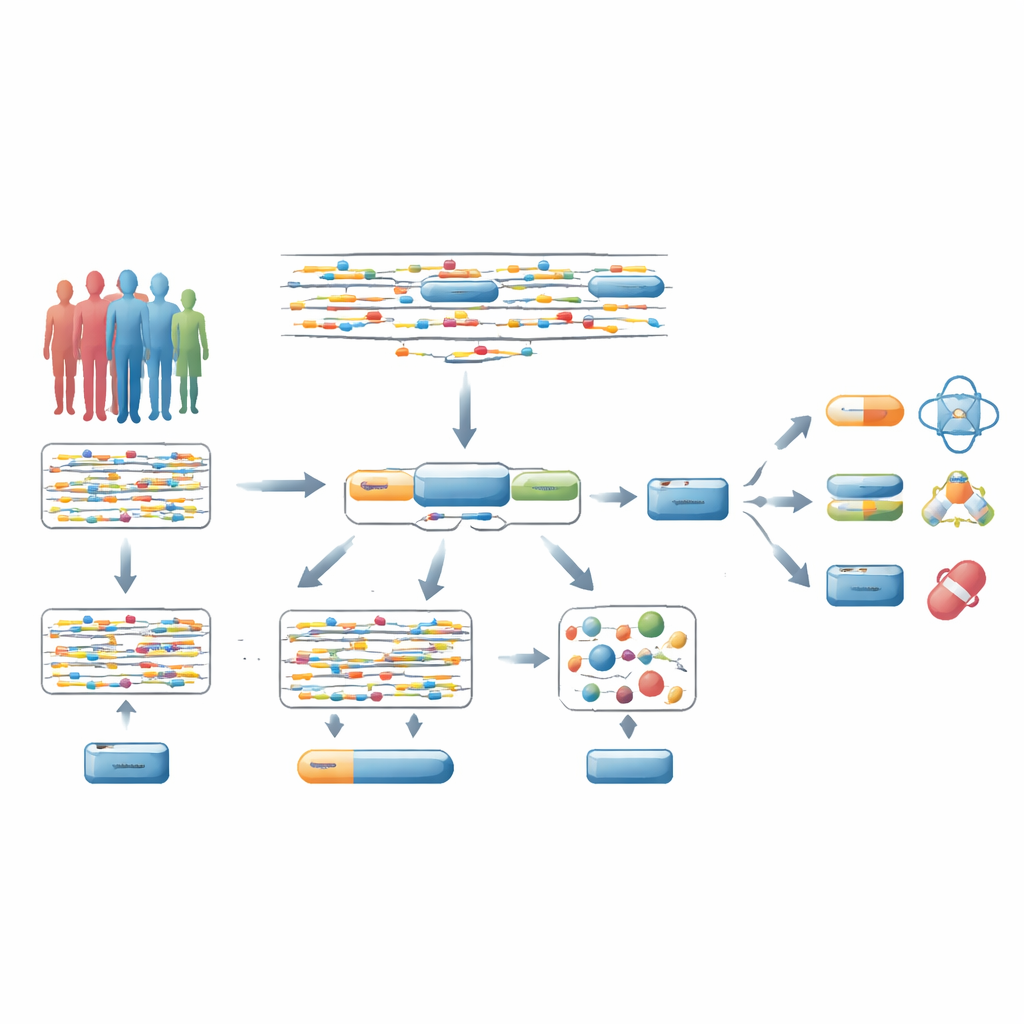
Od rozproszonych sygnałów DNA do całych genów
Większość badań asocjacyjnych obejmujących cały genom (GWAS) analizuje miliony pojedynczych zmian w DNA pojedynczo i sprawdza, czy każda z nich wiąże się z chorobą. Zazwyczaj badacze zakładają potem, że najsilniej skorelowana zmiana w pobliżu genu wskazuje na ten gen. Ten skrót myślowy często jednak myli: tylko niewielka część tych „wiodących” wariantów rzeczywiście powoduje chorobę, a warianty te mogą wpływać na odległe geny. Z tego powodu surowe korekty statystyczne rozciągnięte na miliony testów utrudniają odnalezienie prawdziwych genów choroby, szczególnie takich, które istniejące lub potencjalne leki mogłyby celować.
Nowy zestaw narzędzi do odczytywania mapy genetycznej
Autorzy przedstawiają rodzinę testów „opartych na genie”, na czele z metodą nazwaną GenT. Zamiast oceniania pojedynczych zmian w izolacji, GenT grupuje wszystkie istotne warianty wokół każdego genu i testuje je razem. Co istotne, zespół opracował matematykę leżącą u podstaw metody, dzięki czemu dokładnie wiedzą, jak GenT powinien się zachowywać przy braku rzeczywistego sygnału, unikając fałszywych alarmów, które mogą prześladować wcześniejsze podejścia genowe. Rozszerzenia tego frameworku — MuGenT dla danych wieloetnicznych lub wielocechowych oraz xGenT do integrowania molekularnych odczytów takich jak ekspresja genów czy poziomy białek — pozwalają badaczom łączyć informacje z różnych populacji i warstw biologii, pracując jednocześnie na podsumowujących statystykach, które są szeroko dostępne.
Odnajdywanie ukrytych celów lekowych w mózgu i organizmie
Zastosowawszy GenT do dużych badań genetycznych choroby Alzheimera, stwardnienia zanikowego bocznego, ciężkiej depresji i schizofrenii, autorzy przeanalizowali ponad 18 000 genów. Odkryli 415 genów, których produkty białkowe można celować istniejącymi lub eksperymentalnymi związkami, z których wiele zostało przeoczonych przez standardowe metody GWAS. Dziesiątki z tych genów możliwych do leczenia znajdują się w regionach genomu, które nie wykazywały silnego sygnału pojedynczego wariantu, co sugeruje, że ryzyko jest rozłożone na wiele umiarkowanych efektów widocznych dopiero na poziomie genu. Warty uwagimi przykładami są SYK w chorobie Alzheimera i THRB w schizofrenii — oba poparte wcześniejszymi badaniami biologicznymi, lecz wcześniej niewidoczne dla konwencjonalnych analiz.
Moc różnorodności i warstw molekularnych
MuGenT rozszerza tę strategię, łącząc dane genetyczne osób pochodzenia europejskiego, afrykańskiego, wschodnioazjatyckiego, południowoazjatyckiego i latynoskiego w analizie cukrzycy typu 2. Ponieważ wiele wariantów ryzyka jest współdzielonych, ale różni się częstością i siłą efektu między grupami, agregowanie ich na poziomie genu znacząco zwiększa moc statystyczną. MuGenT zidentyfikował 269 genów związanych z cukrzycą, które nie miały żadnych indywidualnie istotnych wariantów DNA, z czego 45 koduje białka możliwe do leczenia w wcześniej niespodziewanych regionach. Aby połączyć geny z rzeczywistą biologią, metoda xGenT nakłada genetykę choroby na pomiary, jak warianty wpływają na aktywność genów i obfitość białek w tkankach mózgu. W chorobie Alzheimera xGenT wyróżnił 26 genów możliwych do leczenia poza znanymi regionami ryzyka, w tym NTRK1 i RIPK2, oraz wskazał konkretne regiony mózgu i typy komórek, w których są aktywne.
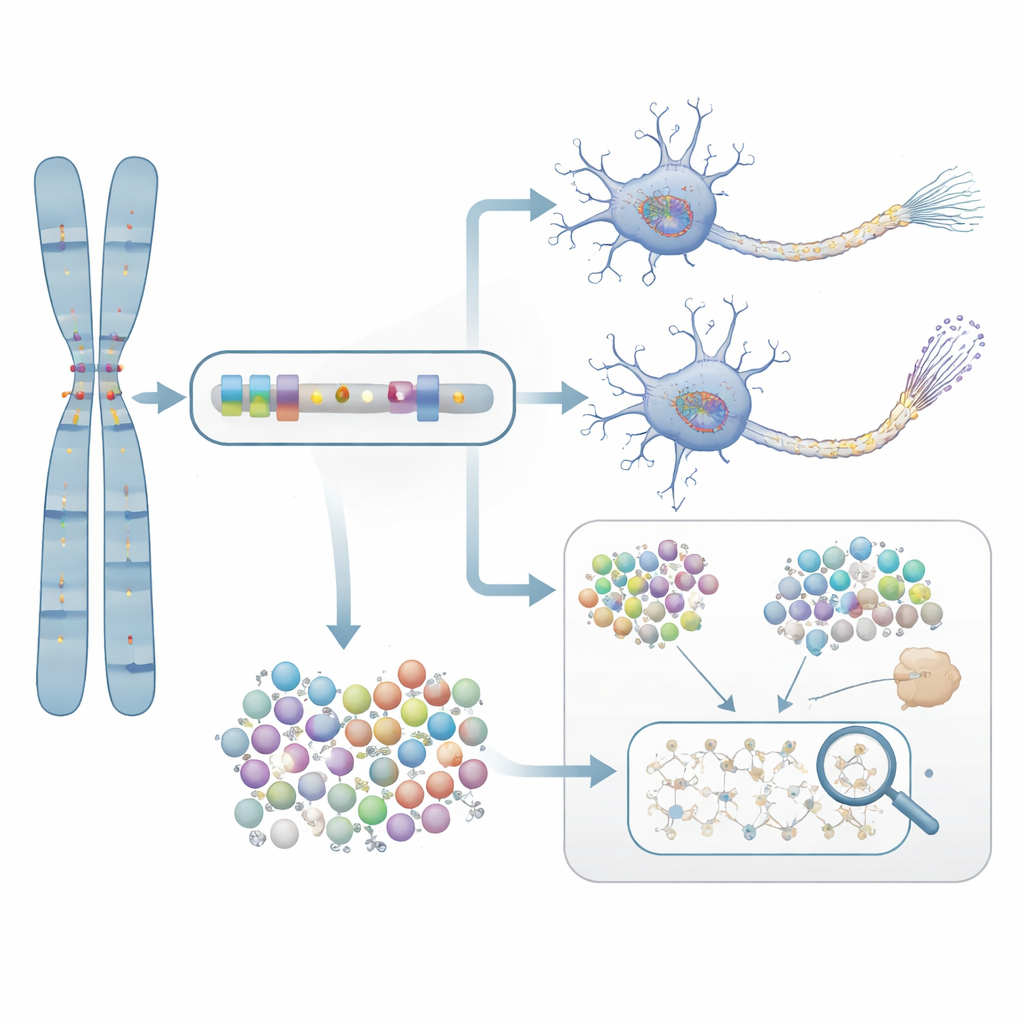
Od predykcji do dowodów w laboratorium
Aby sprawdzić, czy te statystycznie wskazane geny rzeczywiście mają znaczenie dla choroby, badacze skupili się na NTRK1, genie zaangażowanym w przeżycie komórek nerwowych. Leczyli neurony wyhodowane z komórek pacjentów z chorobą Alzheimera selektywnym związkiem blokującym NTRK1. W tych hodowlach zahamowanie NTRK1 zmniejszyło nieprawidłowe chemiczne znaczniki na białku tau — zmiany ściśle powiązane z splątanymi skupiskami białka obserwowanymi w mózgach chorych na Alzheimera. Eksperyment ten tworzy mechanistyczny pomost od statystyk opartych na genach do procesu biologicznego, który można w zasadzie celować lekami.
Co to oznacza dla przyszłych terapii
W podsumowaniu praca pokazuje, że przesunięcie uwagi z pojedynczych markerów DNA na całe geny, przy jednoczesnym korzystaniu z danych z różnych populacji i wielu warstw molekularnych, może ujawnić znacznie więcej wiarygodnych celów lekowych dla chorób złożonych. Autorzy argumentują, że wiele naprawdę istotnych genów wpływa na chorobę przez sieci umiarkowanych, rozproszonych efektów, które słabo wychwytuje tradycyjne skanowanie GWAS. Ich ramy GenT wraz z rozszerzeniami wieloetnicznymi i molekularnymi oferują statystycznie rygorystyczny sposób ujawniania tych ukrytych sygnałów i priorytetyzacji genów do głębszych badań eksperymentalnych. Choć potrzebne będą dalsze badania laboratoryjne i kliniczne zanim jakaś terapia trafi do pacjentów, podejście to znacząco rozszerza genetyczne punkty wyjścia dla odkrywania leków w chorobach, które pilnie potrzebują lepszych terapii.
Cytowanie: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Słowa kluczowe: asocjacja genowa, choroba Alzheimera, cukrzyca typu 2, cele farmakologiczne, genetyka wieloetniczna