Clear Sky Science · nl
Combinatie van xQTL en genome-wide associatiestudies uit diverse populaties verbetert de ontdekking van geneesmiddelbare genen
Waarom genen belangrijk zijn voor toekomstige geneesmiddelen
De moderne genetica heeft duizenden DNA-markeringen aan het licht gebracht die gekoppeld zijn aan veelvoorkomende ziekten, maar het omzetten van die aanwijzingen in concrete medicijndoelen gaat frustrerend langzaam. Deze studie pakt een centraal knelpunt aan: onze gebruikelijke manieren om grote genetische studies te interpreteren missen vaak de genen waarop geneesmiddelen daadwerkelijk kunnen ingrijpen. Door te herdenken hoe genetische data over verschillende populaties en biologische lagen geanalyseerd worden, proberen de auteurs verborgen maar geneesmiddelbare zwakke plekken in ziekten zoals Alzheimer, depressie, schizofrenie en type 2 diabetes bloot te leggen.
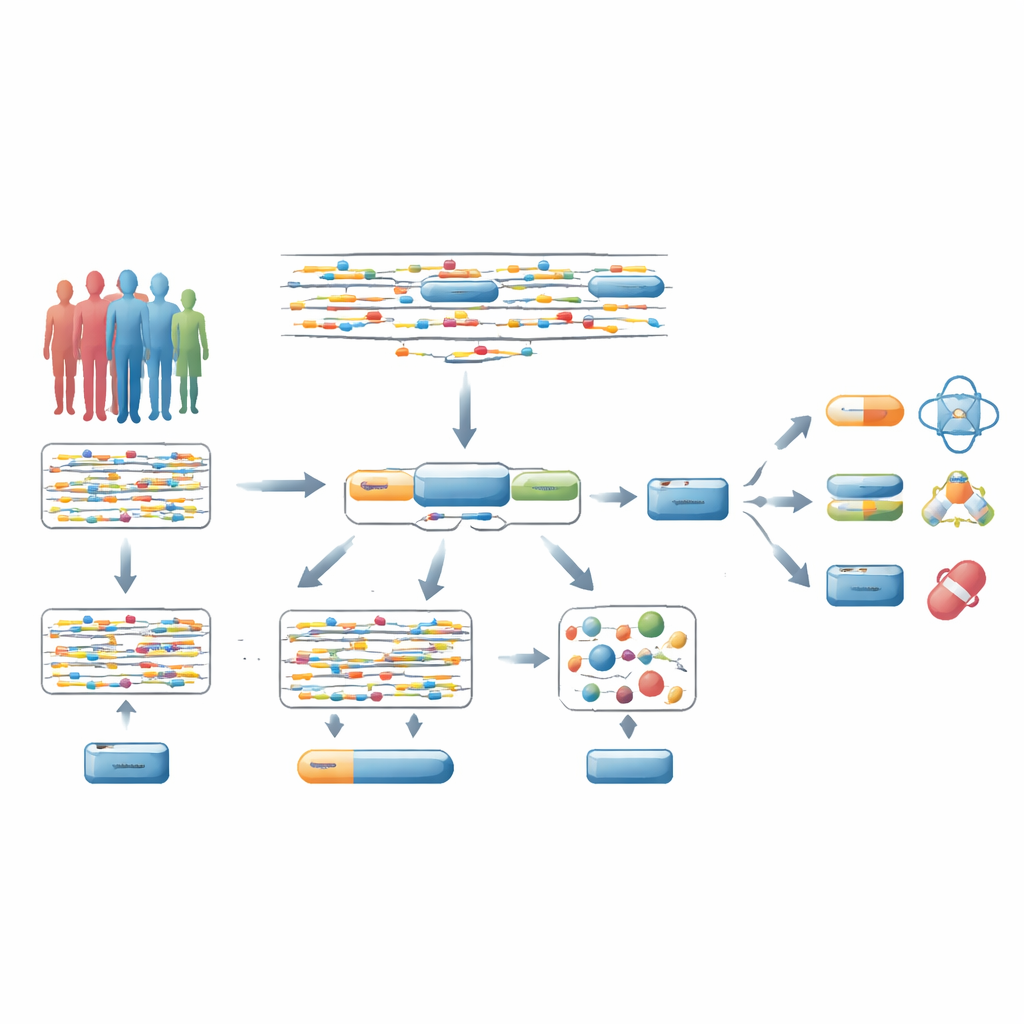
Van verspreide DNA-signalen naar hele genen
De meeste genome-wide associatiestudies (GWAS) bekijken miljoenen individuele DNA-veranderingen één voor één en vragen of elk afzonderlijk verband houdt met een ziekte. Onderzoekers nemen vaak aan dat de meest sterk geassocieerde variant nabij een gen dat gen aanwijst. Maar die vuistregel is vaak onjuist: slechts een klein deel van deze “lead”-varianten veroorzaakt daadwerkelijk ziekte, en ze kunnen ook invloed hebben op verre genen. Daarom zorgen strikte statistische correcties over miljoenen tests dat het moeilijk is echte ziektegenen te vinden, vooral diegenen die bestaande of potentiële geneesmiddelen kunnen aanspreken.
Een nieuwe set instrumenten om de genetische kaart te lezen
De auteurs introduceren een familie van “gen-gebaseerde” toetsen, met als hoofdtechniek GenT. In plaats van individuele DNA-veranderingen los van elkaar te beoordelen, groepeert GenT alle relevante varianten rond elk gen en test ze samen. Cruciaal is dat het team de onderliggende wiskunde heeft uitgewerkt zodat ze precies weten hoe GenT zich hoort te gedragen wanneer er geen echt signaal is, waardoor valse alarmen die eerdere gen-gebaseerde methoden teisteren worden vermeden. Uitbreidingen van dit kader—MuGenT voor multi-afkomst of multi-trait gegevens, en xGenT voor het integreren van moleculaire metingen zoals genexpressie of proteïneniveaus—laten onderzoekers informatie over populaties en biologische lagen combineren terwijl ze nog steeds werken met samenvattende statistieken die veelal beschikbaar zijn.
Verborgen geneesmiddeldoelen in hersenen en lichaam vinden
Toepassing van GenT op grote genetische studies van de ziekte van Alzheimer, amyotrofische laterale sclerose, majeure depressie en schizofrenie bracht meer dan 18.000 genen onder de loep. Ze ontdekten 415 genen waarvan de eiwitproducten gericht kunnen worden door bestaande of experimentele verbindingen, waarvan er veel door standaard GWAS-methoden waren gemist. Tientallen van deze geneesmiddelbare genen liggen in regio’s van het genoom zonder sterk enkel-variantensignaal, wat suggereert dat het risico zich verspreidt over vele bescheiden effecten die alleen zichtbaar worden als je op genniveau kijkt. Opvallende voorbeelden zijn SYK bij de ziekte van Alzheimer en THRB bij schizofrenie, beide ondersteund door eerder biologisch werk maar eerder onder de radar van conventionele analyses.
De kracht van diversiteit en moleculaire lagen
MuGenT breidt deze strategie uit om genetische data van mensen van Europese, Afrikaanse, Oost-Aziatische, Zuid-Aziatische en Hispaanse afkomst te combineren bij type 2 diabetes. Omdat veel risicovarianten gedeeld worden maar in frequentie en effectgrootte per groep verschillen, versterkt het samenvoegen op genniveau de statistische kracht aanzienlijk. MuGenT identificeerde 269 diabetes-geassocieerde genen zonder individuele significante DNA-varianten, waarvan 45 eiwitten coderen die geneesmiddelbaar zijn in eerder onopgemerkte regio’s. Om genen aan werkelijke biologie te koppelen legt de xGenT-methode ziektegenetica naast metingen van hoe varianten genactiviteit en eiwitniveaus in hersenweefsels beïnvloeden. Bij Alzheimer markeerde xGenT 26 geneesmiddelbare genen buiten bekende risicoregions, inclusief NTRK1 en RIPK2, en wees het op specifieke hersengebieden en celtypen waar ze actief zijn.
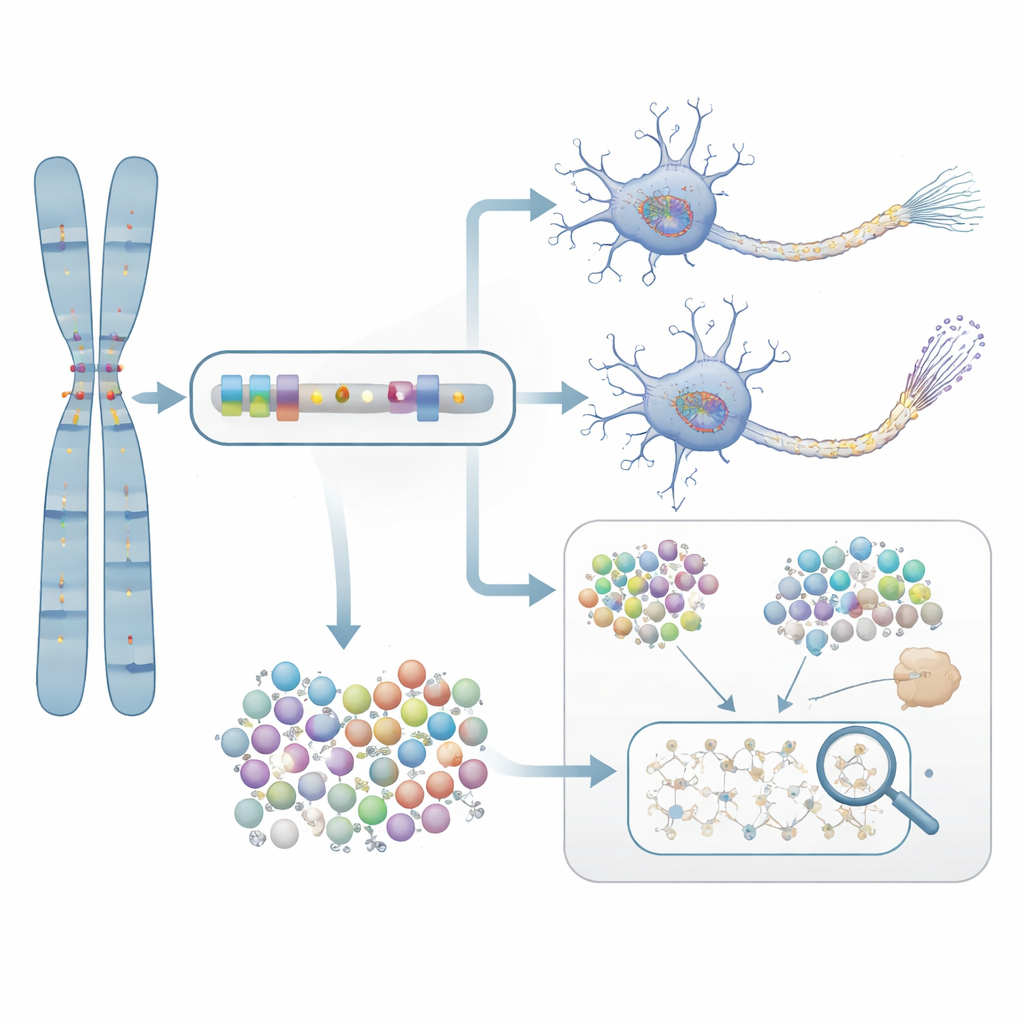
Van voorspelling naar laboratoriumbewijs
Om te testen of deze statistisch aangeduide genen daadwerkelijk van belang zijn voor ziekte, zochten de onderzoekers NTRK1 nader uit, een gen dat betrokken is bij het overleven van zenuwcellen. Ze behandelden neuronen gekweekt uit cellen van Alzheimerpatiënten met een selectieve NTRK1-remmende stof. In deze laboratoriumgekweekte neuronen verminderde het remmen van NTRK1 abnormale chemische tags op het tau-eiwit—veranderingen die sterk samenhangen met de verwarde eiwitklonten die in Alzheimerhersenen worden gezien. Dit experiment vormt een mechanische brug tussen de gen-gebaseerde statistiek en een biologisch proces dat in principe door geneesmiddelen aangetast kan worden.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk laat het werk zien dat verleggen van de focus van individuele DNA-markeringen naar hele genen, en daarbij putten uit gegevens van diverse populaties en meerdere moleculaire lagen, veel meer plausibele geneesmiddeldoelen voor complexe aandoeningen kan onthullen. De auteurs betogen dat veel echt belangrijke genen ziekte beïnvloeden via netwerken van bescheiden, verspreide effecten die slecht worden vastgelegd door traditionele GWAS-scans. Hun GenT-kader, samen met de multi-afkomst- en moleculaire uitbreidingen, biedt een statistisch rigoureuze manier om deze verborgen signalen bloot te leggen en genen te prioriteren voor verder experimenteel onderzoek. Hoewel aanvullende laboratorium- en klinische studies nodig zullen zijn voordat een therapie patiënten bereikt, vergroot deze aanpak significant de genetische uitgangspunten voor geneesmiddelontdekking bij aandoeningen die dringend betere behandelingen behoeven.
Bronvermelding: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Trefwoorden: gen-gebaseerde associatie, Ziekte van Alzheimer, type 2 diabetes, geneesmiddelbare doelen, multi-afkomst genetica