Clear Sky Science · es
Combinar xQTL y estudios de asociación del genoma completo en poblaciones diversas mejora el descubrimiento de genes farmacológicamente abordables
Por qué los genes importan para los medicamentos del futuro
La genética moderna ha descubierto miles de marcadores de ADN asociados a enfermedades comunes, pero convertir esas pistas en dianas farmacológicas reales ha sido frustrantemente lento. Este estudio aborda un cuello de botella central: nuestras maneras estándar de leer grandes estudios genéticos a menudo pasan por alto los genes sobre los que los fármacos pueden actuar. Repensando cómo analizar datos genéticos a través de poblaciones diversas y capas biológicas, los autores aspiran a descubrir puntos débiles ocultos, pero abordables con fármacos, en enfermedades como el Alzheimer, la depresión, la esquizofrenia y la diabetes tipo 2.
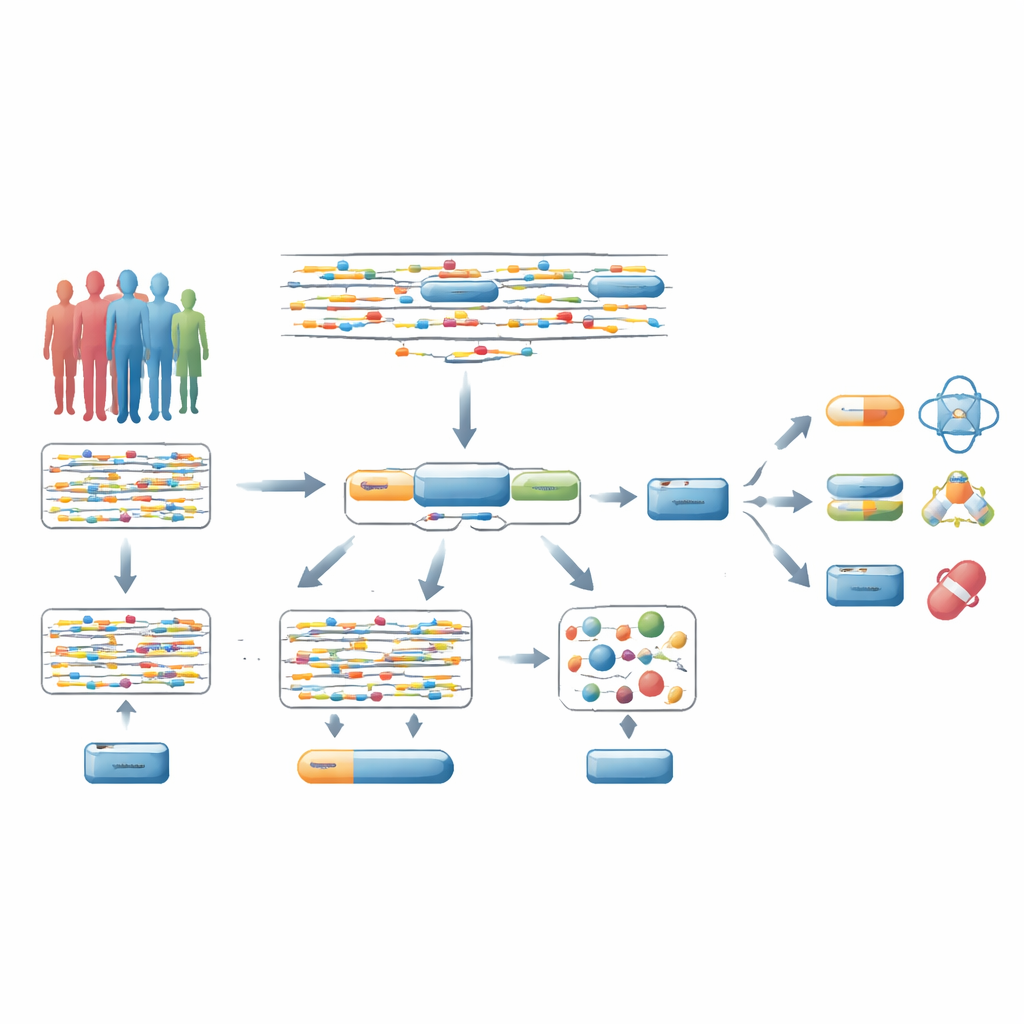
De señales de ADN dispersas a genes completos
La mayoría de los estudios de asociación del genoma completo (GWAS) examinan millones de cambios individuales en el ADN uno por uno y preguntan si cada uno está vinculado a una enfermedad. Normalmente, los investigadores suponen que el cambio de ADN más fuertemente asociado cerca de un gen señala ese gen. Pero este atajo suele ser erróneo: solo una pequeña fracción de esas variantes “líderes” causan realmente la enfermedad, y además pueden influir en genes distantes. Debido a esto, las correcciones estadísticas estrictas distribuidas a través de millones de pruebas dificultan encontrar genes causantes reales, especialmente aquellos que los fármacos existentes o potenciales pueden targetear.
Un nuevo conjunto de herramientas para leer el mapa genético
Los autores presentan una familia de pruebas “basadas en genes”, encabezadas por un método llamado GenT. En lugar de valorar cambios individuales de ADN de forma aislada, GenT agrupa todas las variantes relevantes alrededor de cada gen y las prueba en conjunto. De forma crucial, el equipo resolvió la matemática subyacente para saber exactamente cómo debe comportarse GenT cuando no hay una señal real, evitando las falsas alarmas que pueden afectar a enfoques basados en genes anteriores. Extensiones de este marco —MuGenT para datos multi-ancestrales o multi-rasgo, y xGenT para integrar lecturas moleculares como la expresión génica o los niveles de proteínas— permiten a los investigadores combinar información entre poblaciones y capas biológicas manteniéndose en estadísticas sumarias que están ampliamente disponibles.
Encontrar dianas terapéuticas ocultas en cerebro y organismo
Aplicando GenT a grandes estudios genéticos de la enfermedad de Alzheimer, esclerosis lateral amiotrófica, depresión mayor y esquizofrenia, los autores analizaron más de 18.000 genes. Descubrieron 415 genes cuyos productos proteicos pueden ser dianas de compuestos existentes o experimentales, muchos de los cuales los métodos GWAS estándar habían pasado por alto. Docenas de estos genes farmacológicamente abordables residen en regiones del genoma que no mostraban señales fuertes por variante individual, lo que sugiere que el riesgo está distribuido en muchos efectos modestos que solo se hacen visibles cuando se analizan a nivel de gen. Ejemplos notables incluyen SYK en la enfermedad de Alzheimer y THRB en la esquizofrenia, ambos respaldados por trabajos biológicos previos pero previamente fuera del radar de los análisis convencionales.
El poder de la diversidad y de las capas moleculares
MuGenT amplía esta estrategia para combinar datos genéticos de personas de ascendencias europea, africana, esteasiática, surasiática e hispana con datos de diabetes tipo 2. Debido a que muchas variantes de riesgo se comparten pero varían en frecuencia y efecto entre grupos, agruparlas a nivel de gen incrementa considerablemente la potencia estadística. MuGenT identificó 269 genes asociados a la diabetes que carecían de variantes de ADN individualmente significativas, 45 de los cuales codifican proteínas farmacológicamente abordables en regiones previamente insospechadas. Para conectar genes con la biología real, el método xGenT superpone la genética de la enfermedad con medidas de cómo las variantes afectan la actividad génica y la abundancia proteica en tejidos cerebrales. En la enfermedad de Alzheimer, xGenT resaltó 26 genes farmacológicamente abordables fuera de las regiones de riesgo conocidas, incluidos NTRK1 y RIPK2, y apuntó a regiones y tipos celulares cerebrales específicos donde están activos.
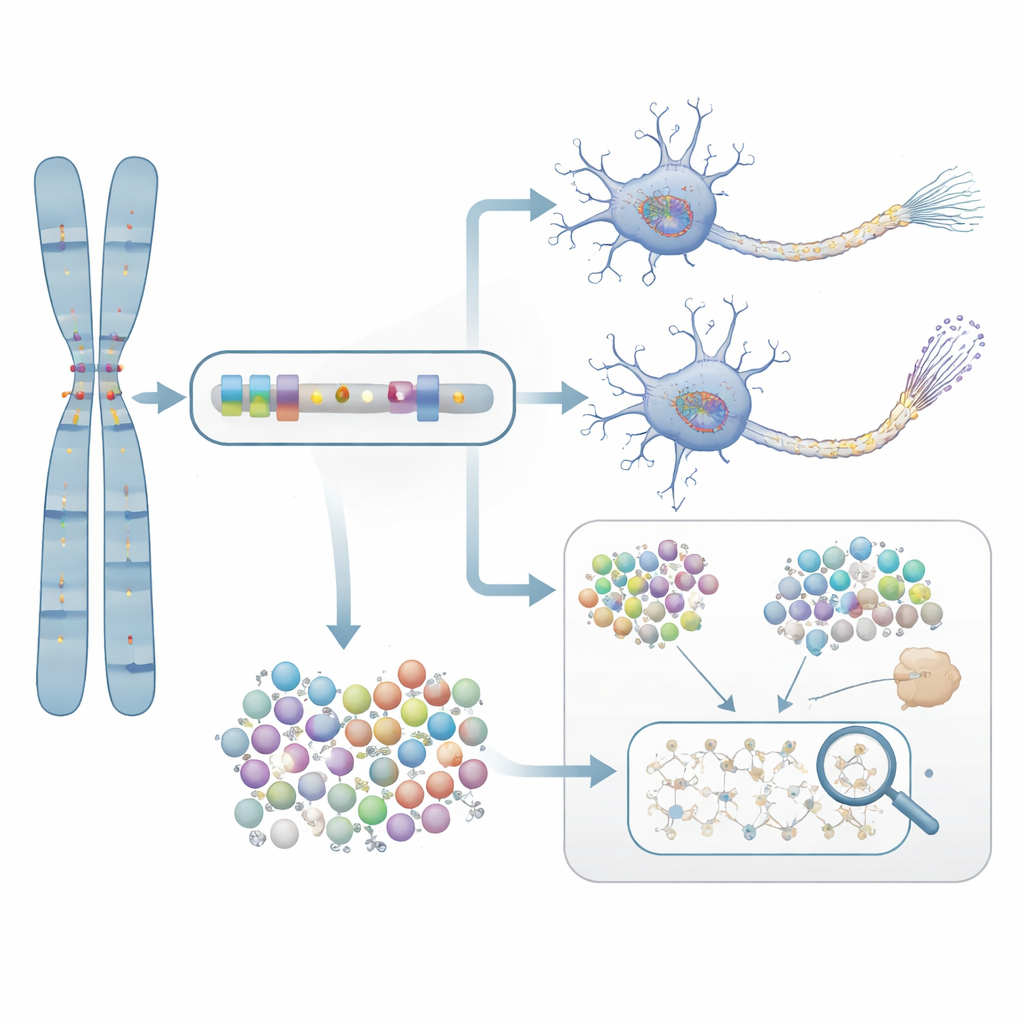
De la predicción a la evidencia en el laboratorio
Para probar si estos genes señalados estadísticamente importan realmente para la enfermedad, los investigadores profundizaron en NTRK1, un gen implicado en la supervivencia de las neuronas. Trataron neuronas cultivadas a partir de células de pacientes con Alzheimer con un compuesto selectivo bloqueador de NTRK1. En estas neuronas en cultivo, la inhibición de NTRK1 redujo marcas químicas anómalas en la proteína tau —cambios estrechamente ligados a los enredos proteicos observados en cerebros con Alzheimer. Este experimento proporciona un puente mecanístico desde las estadísticas basadas en genes hacia un proceso biológico que, en principio, puede ser abordado por fármacos.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo muestra que cambiar el enfoque de marcadores de ADN individuales a genes completos, aprovechando datos de poblaciones diversas y múltiples capas moleculares, puede revelar muchas más dianas plausibles para enfermedades complejas. Los autores sostienen que muchos genes realmente importantes influyen en la enfermedad a través de redes de efectos modestos y distribuidos que los escaneos GWAS tradicionales capturan mal. Su marco GenT, junto con sus extensiones multi-ancestrales y moleculares, ofrece una forma estadísticamente rigurosa de exponer estas señales ocultas y priorizar genes para pruebas experimentales más profundas. Aunque serán necesarios más estudios de laboratorio y clínicos antes de que cualquier terapia llegue a los pacientes, este enfoque amplía de forma significativa los puntos de partida genéticos para el descubrimiento de fármacos en afecciones que necesitan con urgencia mejores tratamientos.
Cita: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Palabras clave: asociación basada en genes, enfermedad de Alzheimer, diabetes tipo 2, blancos farmacológicos, genética multi-ancestral