Clear Sky Science · de
Kombination von xQTL- und populationsübergreifenden genomweiten Assoziationsstudien verbessert die Entdeckung von medizinisch adressierbaren Genen
Warum Gene für zukünftige Medikamente wichtig sind
Die moderne Genetik hat Tausende von DNA-Markern aufgedeckt, die mit häufigen Erkrankungen verknüpft sind, aber diese Hinweise in konkrete Arzneimittelziele zu übersetzen, geht frustrierend langsam voran. Diese Studie adressiert einen zentralen Engpass: Unsere üblichen Methoden zur Auswertung großer genetischer Studien übersehen oft die Gene, auf die Medikamente tatsächlich wirken könnten. Indem die Autoren die Analyse genetischer Daten über vielfältige Populationen und biologische Ebenen neu denken, wollen sie versteckte, aber medikamentös angreifbare Schwachstellen bei Krankheiten wie Alzheimer, Depression, Schizophrenie und Typ‑2‑Diabetes aufdecken.
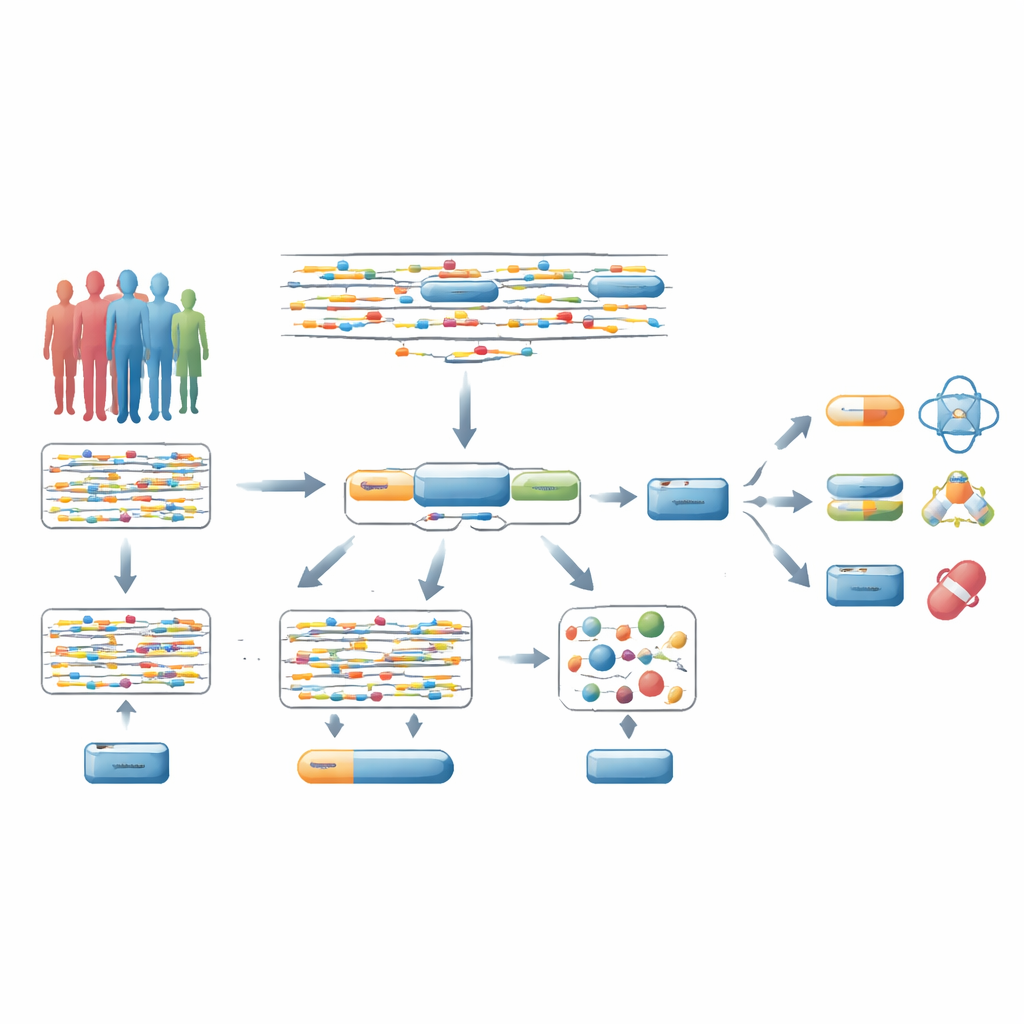
Von verstreuten DNA-Signalen zu ganzen Genen
Die meisten genomweiten Assoziationsstudien (GWAS) betrachten Millionen einzelner DNA-Veränderungen getrennt und prüfen, ob jede mit einer Krankheit verbunden ist. Üblicherweise nehmen Forschende dann an, dass die stärkste Assoziation in der Nähe eines Gens auf dieses Gen hindeutet. Diese Abkürzung ist jedoch oft falsch: Nur ein kleiner Bruchteil dieser „lead“-Varianten verursacht tatsächlich die Krankheit, und sie können entfernte Gene beeinflussen. Aufgrund dessen machen strikte statistische Korrekturen über Millionen Tests es schwer, echte Krankheitsgene zu finden—insbesondere solche, die von vorhandenen oder potenziellen Medikamenten adressierbar wären.
Ein neues Werkzeugset, um die genetische Karte zu lesen
Die Autoren stellen eine Familie von „genbasierten“ Tests vor, an deren Spitze eine Methode namens GenT steht. Statt einzelne DNA-Veränderungen isoliert zu bewerten, fasst GenT alle relevanten Varianten um jedes Gen zusammen und testet sie gemeinsam. Entscheidend ist, dass das Team die zugrunde liegende Mathematik so ausgearbeitet hat, dass bekannt ist, wie sich GenT genau verhält, wenn kein echtes Signal vorliegt, wodurch Fehlalarme vermieden werden, die frühere genbasierte Ansätze plagen können. Erweiterungen dieses Rahmens—MuGenT für multi-ethnische oder multi-Phänotyp-Daten und xGenT zur Integration molekularer Messwerte wie Genexpression oder Proteinmengen—ermöglichen es Forschenden, Informationen über Populationen und biologische Ebenen zu kombinieren, während sie weiterhin mit Zusammenfassungsstatistiken arbeiten, die weit verbreitet verfügbar sind.
Versteckte Medikamentenziele im Gehirn und Körper finden
Bei der Anwendung von GenT auf große genetische Studien zu Alzheimer, amyotropher Lateralsklerose, Major Depression und Schizophrenie analysierten die Autoren mehr als 18.000 Gene. Sie entdeckten 415 Gene, deren Proteinprodukte durch vorhandene oder experimentelle Verbindungen angesteuert werden können, viele davon hatten Standard‑GWAS‑Methoden übersehen. Dutzende dieser medikamentös adressierbaren Gene liegen in Regionen des Genoms, die kein starkes Einzelvarianten-Signal zeigten, was darauf hindeutet, dass das Risiko über viele moderate Effekte verteilt ist, die erst auf Genebene sichtbar werden. Auffällige Beispiele sind SYK bei Alzheimer und THRB bei Schizophrenie, beide durch frühere biologische Arbeiten gestützt, aber zuvor unter dem Radar konventioneller Analysen.
Die Kraft von Diversität und molekularen Ebenen
MuGenT erweitert diese Strategie, indem genetische Daten von Menschen europäischer, afrikanischer, ostasiatischer, südasiatischer und hispanischer Abstammung für Typ‑2‑Diabetes kombiniert werden. Da viele Risikovarianten geteilt werden, aber in Häufigkeit und Effektstärke zwischen Gruppen variieren, steigert deren Zusammenfassung auf Genebene die statistische Power erheblich. MuGenT identifizierte 269 diabetesassoziierte Gene ohne einzelne signifikante DNA‑Varianten, von denen 45 Proteine kodieren, die in zuvor nicht erwarteten Regionen pharmakologisch adressierbar sind. Um Gene mit konkreter Biologie zu verknüpfen, überlagert die xGenT‑Methode die Krankheitsgenetik mit Messungen, wie Varianten die Genaktivität und Proteinan- zahl in Gehirngeweben beeinflussen. Bei Alzheimer hob xGenT 26 medikamentös adressierbare Gene außerhalb bekannter Risiko- Regionen hervor, darunter NTRK1 und RIPK2, und wies auf spezifische Hirnregionen und Zelltypen hin, in denen sie aktiv sind.
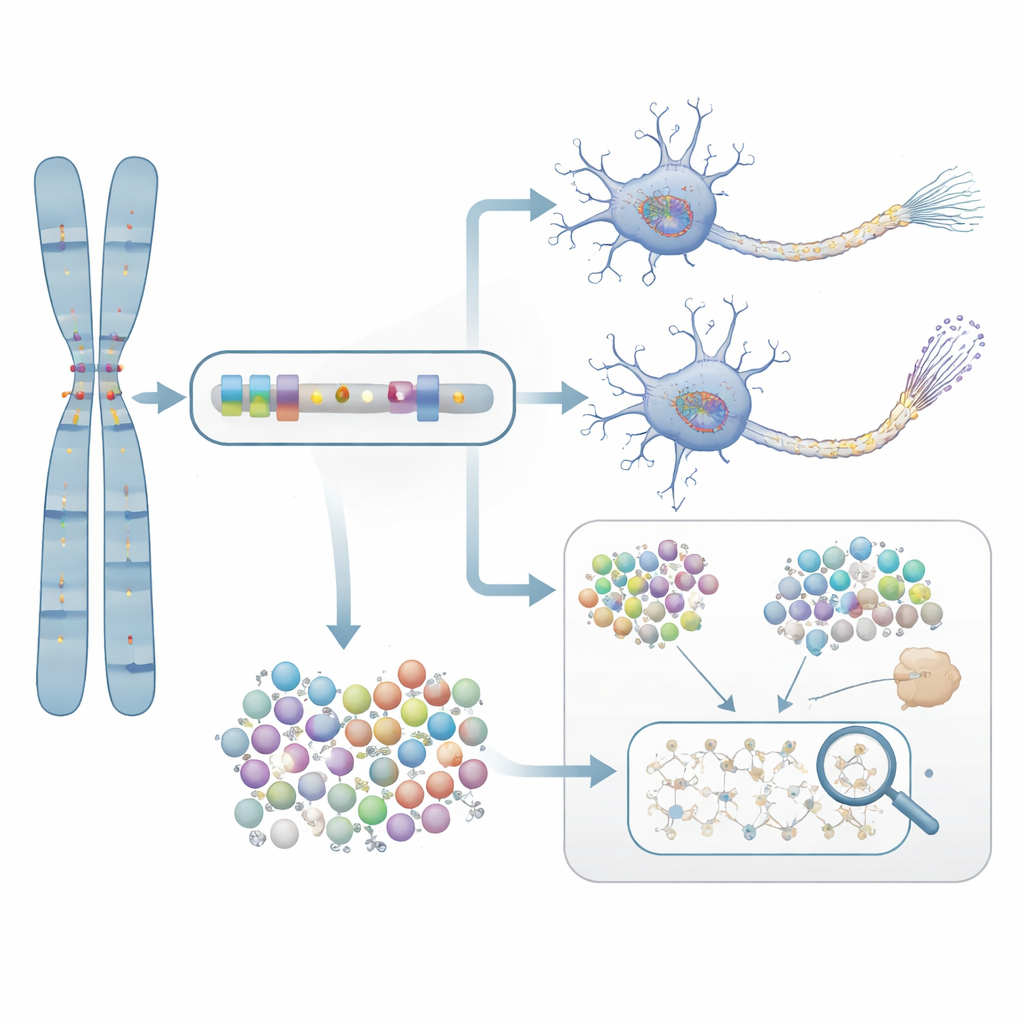
Von der Vorhersage zum Labornachweis
Um zu prüfen, ob diese statistisch markierten Gene tatsächlich für die Krankheit relevant sind, fokussierten die Forschenden auf NTRK1, ein Gen, das am Überleben von Nervenzellen beteiligt ist. Sie behandelten aus den Zellen von Alzheimer‑Patienten gezüchtete Neuronen mit einer selektiven NTRK1‑blockierenden Verbindung. In diesen im Labor gezüchteten Neuronen reduzierte die Hemmung von NTRK1 abnorme chemische Markierungen des Tau‑Proteins—Veränderungen, die eng mit den verfilzten Proteinablagerungen im Gehirn von Alzheimer‑Patienten verknüpft sind. Dieses Experiment liefert eine mechanistische Brücke von den genbasierten Statistiken zu einem biologischen Prozess, der prinzipiell pharmakologisch angreifbar ist.
Was das für künftige Therapien bedeutet
In der Gesamtschau zeigt die Arbeit, dass die Verlagerung des Fokus von einzelnen DNA-Markern hin zu ganzen Genen—unter Nutzung von Daten aus vielfältigen Populationen und mehreren molekularen Ebenen—viel mehr plausible Arzneimittelziele für komplexe Erkrankungen offenlegen kann. Die Autoren argumentieren, dass viele wirklich wichtige Gene die Krankheit durch Netzwerke moderater, verteilter Effekte beeinflussen, die von traditionellen GWAS‑Scans nur schlecht erfasst werden. Ihr GenT‑Rahmen zusammen mit den multi‑ethnischen und molekularen Erweiterungen bietet eine statistisch robuste Möglichkeit, diese versteckten Signale zu enthüllen und Gene für weiterführende experimentelle Tests zu priorisieren. Obwohl weitere Labor‑ und klinische Studien nötig sind, bevor eine Therapie Patienten erreicht, erweitert dieser Ansatz die genetischen Ausgangspunkte für die Arzneimittelentdeckung bei Erkrankungen, die dringend bessere Behandlungen benötigen, deutlich.
Zitation: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
Schlüsselwörter: genbasierte Assoziation, Alzheimer-Krankheit, Typ-2-Diabetes, medikamentös adressierbare Ziele, multi-ethnische Genetik