Clear Sky Science · he
שילוב xQTL ומחקרי אסוציאציה ברמת הגנום מאוכלוסיות מגוונות משפר גילוי גנים ניתנים לתרופה
למה גנים חשובים עבור תרופות עתידיות
הגנטיקה המודרנית גילתה אלפי סימני DNA המקושרים למחלה השכיחה, אך המרת הרמזים האלה ליעדי תרופות ממשיים התקדמה בעצבנות לאט. המחקר הזה מתמודד עם צוואר בקבוק מרכזי: שיטותינו הסטנדרטיות לניתוח מחקרי גנום רחבי לעתים קרובות מפספסות את הגנים שעליהם אפשר ליישם תרופות. על‑ידי חשיבה מחדש על הדרך לנתח נתונים גנטיים מאוכלוסיות מגוונות ושכבות ביולוגיות שונות, הכותבים שואפים לחשוף נקודות תורפה נסתרות אך ניתנות לטיפול במחלות כמו אלצהיימר, דיכאון, סכיזופרניה וסכרת סוג 2.
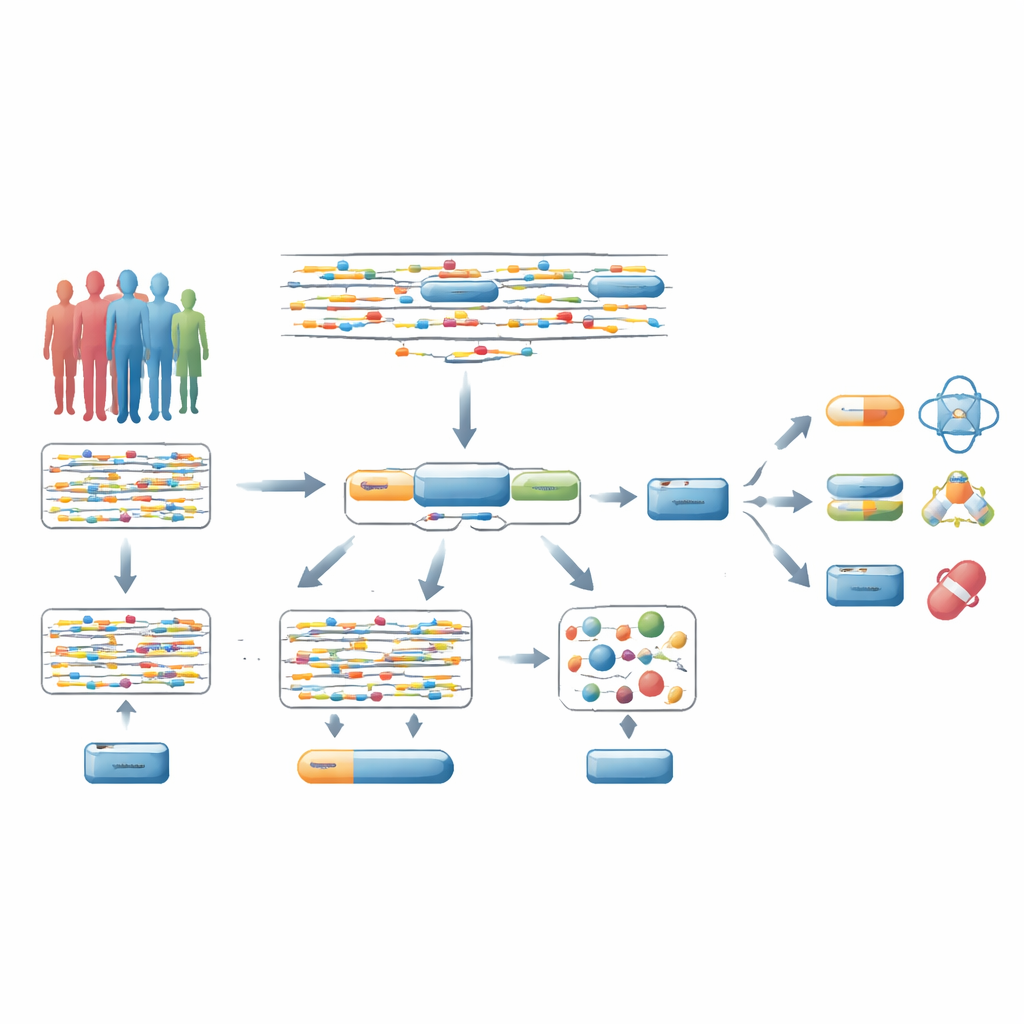
מאותות DNA מפוזרים לגנים שלמים
רוב מחקרי האסוציאציה ברמת הגנום (GWAS) בוחנים מיליוני שינויים בודדים ב‑DNA אחד־אחד ושואלים האם כל אחד מהם מקושר למחלה. בדרך כלל, החוקרים מניחים שהשינוי החזק ביותר שממוקם סמוך לגן מצביע על אותו גן. קיצור דרך זה לעתים קרובות שגוי: רק חלק קטן מ«המשתנים המובילים» אכן גורם למחלה, והם עלולים להשפיע על גנים מרוחקים. בשל כך, תיקונים סטטיסטיים קפדניים שמחולקים על פני מיליוני בדיקות מקשים לאתר גנים אמיתיים של מחלה, במיוחד כאלה שתרופות קיימות או פוטנציאליות יכולות לפעול נגדם.
ערכת כלים חדשה לקריאת המפה הגנטית
הכותבים מציגים משפחה של מבחנים «מבוססי־גן», בראשה שיטה בשם GenT. במקום לשפוט שינויים בודדים ב‑DNA בבידוד, GenT מקבצת את כל המשתנים הרלוונטיים סביב כל גן ובודקת אותם ביחד. מהותית, הצוות פיתח את המתמטיקה הבסיסית כך שיודעים בדיוק כיצד GenT אמורה להתנהג כאשר אין אות אמיתי, ובכך נמנעו אזעקות שווא שמזינות שיטות מבוססות־גן קודמות. הרחבות של המסגרת הזאת—MuGenT לנתוני רב‑אנסטריה או רב‑תכונות, ו‑xGenT לאינטגרציה של מדידות מולקולריות כמו ביטוי גנים או רמות חלבון—מאפשרות לחוקרים לשלב מידע בין אוכלוסיות ושכבות ביולוגיות תוך עבודה מתוך סטטיסטיקות מסכמות שמרחבות זמינות.
גילוי יעדי תרופה נסתרות במוח ובגוף
ביישום GenT על מחקרי גנטיקה גדולים של מחלת אלצהיימר, טרשת־שרירים ניוונית (ALS), דיכאון מג'ורי וסכיזופרניה נבחנו מעל 18,000 גנים. הם חשפו 415 גנים שמוצרי החלבון שלהם ניתנים ליעד על־ידי תרכובות קיימות או ניסיוניות, רבים מהם נעדרו מהשיטות הסטנדרטיות של GWAS. עשרות מהגנים הניתנים לתרופה נמצאים באזורים בגנום שבהם לא נצפה אות חזק של משתנה יחיד, מה שמעיד שהסיכון מפוזר על פני השפעות קטנות מרובות שבולטות רק ברמת הגן. דוגמאות בולטות כוללות את SYK למחלת אלצהיימר ואת THRB לסכיזופרניה, שתמכו בעבודות ביולוגיות קודמות אך נשארו מתחת לסף הזיהוי של ניתוחים קונבנציונליים.
עוצמת הגיוון והשכבות המולקולריות
MuGenT מרחיבה את האסטרטגיה הזו לשילוב נתונים גנטיים מאנשים ממוצא אירופי, אפריקאי, מזרח־אסיאתי, דרום־אסיאתי והיספני בהקשר של סכרת סוג 2. מאחר שרבים מהמוטציות המסכנות משותפות אך משתנות בתדירות ובחוזקה בין קבוצות, איחודן ברמת הגן מגדיל משמעותית את העוצמה הסטטיסטית. MuGenT זיהה 269 גנים מקושרי סכרת החסרים כל משתנה DNA בודד חשוב לפי עצמו, 45 מתוכם מקודדים חלבונים ניתנים לתרופה באזורי genome שלא תוארו בעבר. כדי לקשר גנים לביולוגיה ממשית, שיטת xGenT מחברת גנטיקה של מחלות עם מדידות כיצד המשתנים משפיעים על פעילות גנים וכמות חלבונים ברקמות מוח. באלצהיימר, xGenT הדגישה 26 גנים ניתנים לתרופה שנמצאים מחוץ לאזורי סיכון ידועים, כולל NTRK1 ו‑RIPK2, והצביעה אל אזורים מוחיים וסוגי תאים ספציפיים שבהם הם פעילים.
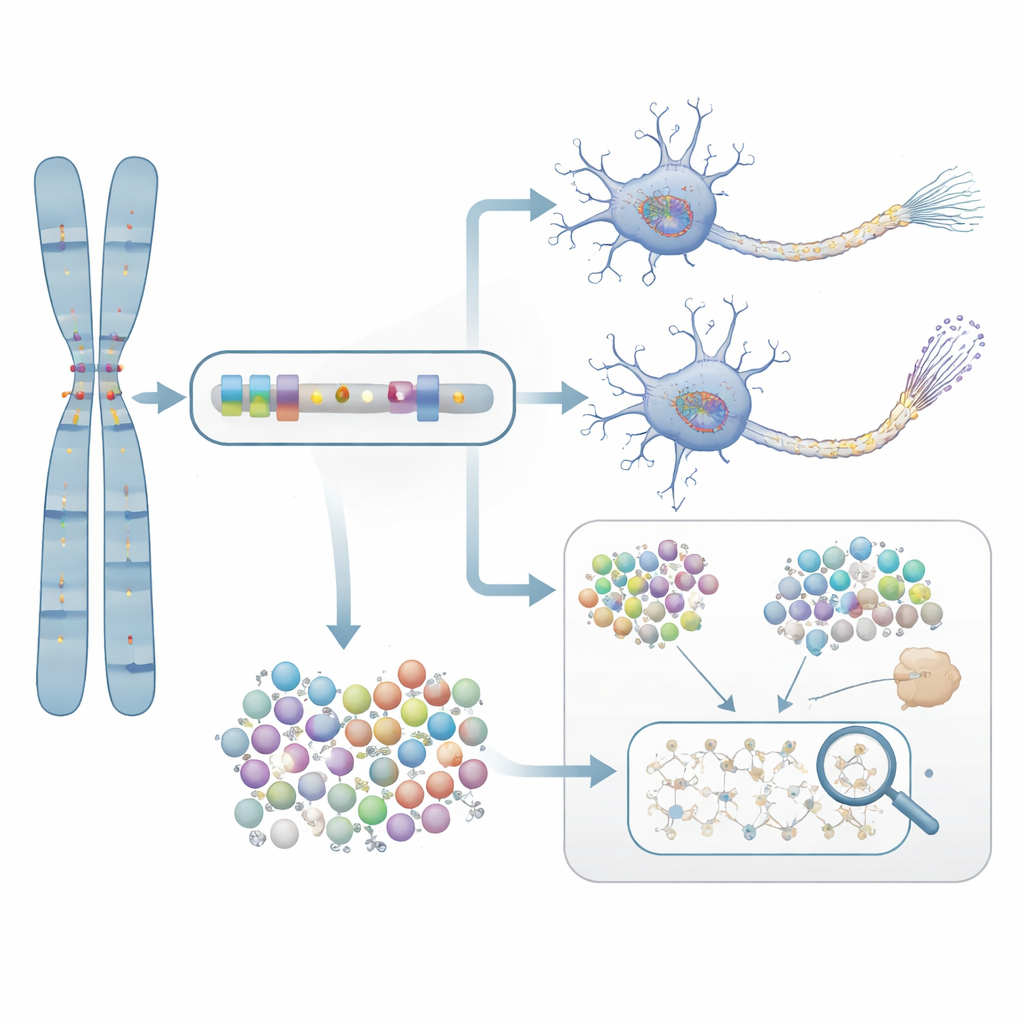
מהניבוי עד הראיות במעבדה
כדי לבדוק האם הגנים שצוינו סטטיסטית באמת חשובים למחלה, החוקרים התרכזו ב‑NTRK1, גן המעורב בהישרדות תאי עצב. הם טיפלו בניורונים שגודלו מתאים של חולי אלצהיימר בתרכובת סלקטיבית החוסמת NTRK1. בתאים הגודלים במעבדה, עיכוב NTRK1 הקטין את התגים הכימיים הלא־תקינים על חלבון הטאו—שינויים הקשורים בצמדי החלבון המלופפים שנצפים במוחם של חולי אלצהיימר. הניסוי הזה מספק גשר מכניסטי מהסטטיסטיקה המבוססת־גן לתהליך ביולוגי שניתן, מבחינה עקרונית, לכוונו בתרופות.
מה המשמעות לטיפולים עתידיים
בהסתכלות כוללת, העבודה מראה שמעבר ממיקוד בסימני DNA בודדים לגנים שלמים, תוך שילוב נתונים מאוכלוסיות מגוונות ומרבדי מולקולות, יכול לחשוף הרבה יותר יעדי תרופה סבירים במחלות מורכבות. המחברים טוענים שרבים מהגנים החשובים באמת משפיעים על המחלה דרך רשתות של השפעות מתונות ומפוזרות שאינן נתפסות היטב בסריקות GWAS המסורתיות. מסגרת GenT שלהם, יחד עם ההרחבות הרב‑אנסטרליות והמולקולריות, מציעה דרך סטטיסטית קפדנית לחשוף אותות נסתרים אלו ולהעדיף גנים לבחינות ניסוי מעמיקות יותר. בעוד שיידרשו מחקרים נוספים במעבדה ובקליניקה לפני שכל טיפול יגיע לחולים, הגישה הזו מרחיבה משמעותית את נקודות ההתחלה הגנטיות לגילוי תרופות במצבים שזקוקים בדחיפות לטיפולים טובים יותר.
ציטוט: Lorincz-Comi, N., Song, W., Chen, X. et al. Combining xQTL and genome-wide association studies from diverse populations improves druggable gene discovery. Nat Commun 17, 2801 (2026). https://doi.org/10.1038/s41467-026-69236-z
מילות מפתח: אסוציאציה מבוססת־גן, מחלת אלцיימר, סכרת סוג 2, יעדי תרופה ניתנים, גנטיקה רב‑אנסטרלית