Clear Sky Science · tr
IFI16, akut böbrek hasarında DNA hasarı ile ferroptozu bağlamada vazgeçilmezdir
Böbrek stresinin ve hücre ölümünün önemi
Akut böbrek hasarı, genellikle büyük cerrahi, enfeksiyonlar veya düşük kan basıncı sonrasında hastanede görülen ani böbrek fonksiyon kaybıdır. Sık, tehlikeli olup, şu anda esas olarak sıvı tedavisi ve diyaliz gibi destekleyici yaklaşımlarla yönetilmekte, hedefe yönelik ilaçlar sınırlıdır. Bu çalışma, böbrek tübül hücrelerinde DNA hasarını daha yeni tanımlanmış bir demir kaynaklı hücre ölümü biçimi olan ferroptozla bağlayan daha önce gizli kalan bir olay zincirini açığa çıkarıyor. Tek bir “anahtar” molekülü belirleyerek, iş kan akışı kesilip yeniden sağlandığında—birçok tıbbi acil durumda görülen—böbrekleri korumanın yeni yollarını öneriyor.
Böbrek hücreleri içinde gizli bir tetikleyici
Araştırmacılar, kan ve oksijen arzı kesilip yeniden sağlandığında özellikle savunmasız olan böbreğin küçük tüplerini kaplayan hücrelere odaklandı; bu sürece iskemi/reperfüzyon denir. Normalde hücrelerin yabancı veya hasarlı DNA’yı algılayıp onarım, iltihaplanma ya da hücre intiharı arasında karar vermesine yardım eden IFI16 adlı protein (fare karşılığı p204) üzerinde yoğunlaştılar. Akut tübüler nekroz adı verilen ağır bir akut böbrek hasarı formu olan hastalardan alınan böbrek biyopsilerini inceleyince, tübül hücrelerinde sağlıklı böbreklere kıyasla çok daha yüksek IFI16 düzeyleri buldular ve IFI16 miktarı kötü böbrek fonksiyonunun kan belirteçleriyle koreleydi. Böbrekleri iskemi/reperfüzyona uğrayan farelerde, fare versiyonu p204 zaman içinde özellikle proksimal tübül hücrelerinin çekirdeklerinde belirgin şekilde arttı. 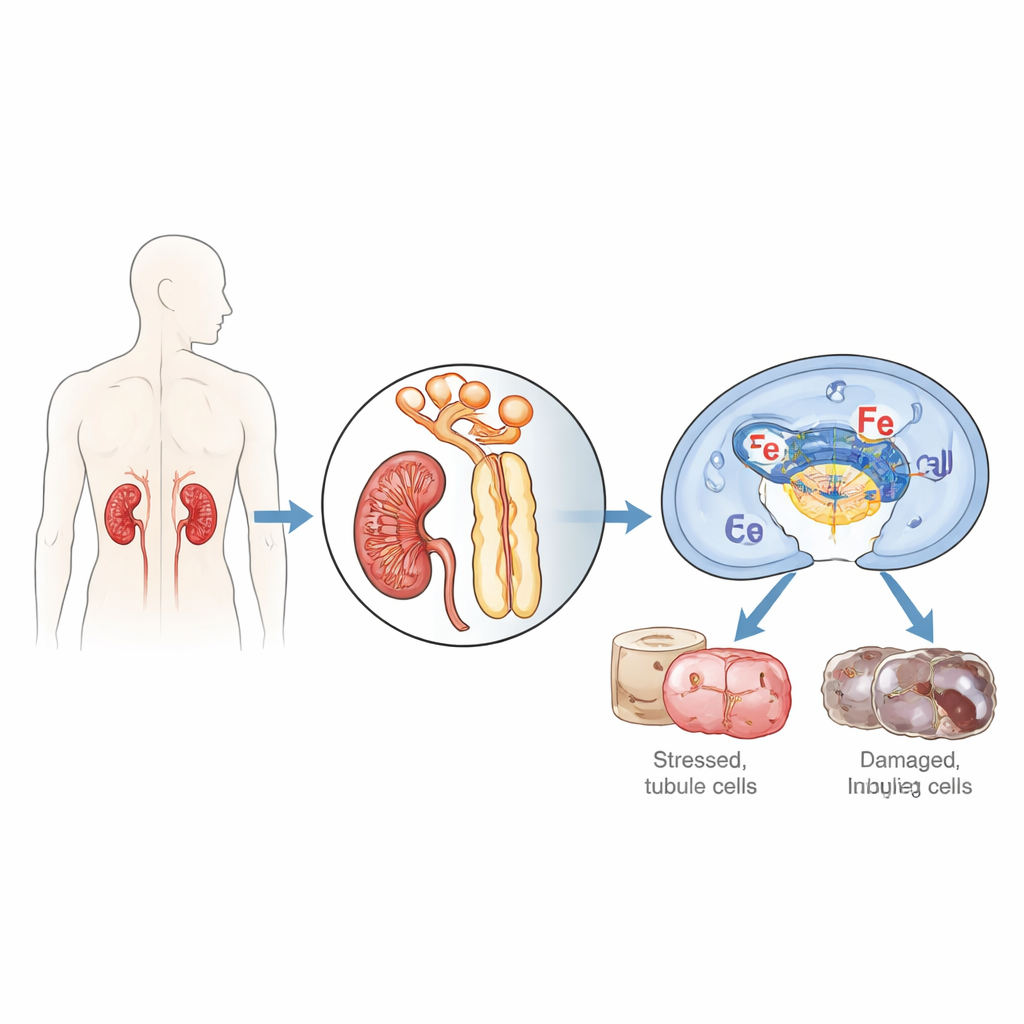
p204’ü kapatmak böbrek hasarını hafifletiyor
Bu proteinin aktif olarak böbreğe zarar verip vermediğini yoksa sadece bir seyirci mi olduğunu test etmek için ekip, tübül hücrelerinde özel olarak p204 eksik olan fareler tasarladı. Bu hayvanlar genel olarak sağlıklı görünüyordu, ancak böbrekleri iskemi/reperfüzyona maruz kaldığında normal farelere göre çok daha iyi durumdaydılar. Kan testleri, böbrek filtrasyonunun daha iyi olduğunu gösteren daha düşük kreatinin ve üre seviyeleri ortaya koydu. Mikroskop altında, tübüllerinde daha az yapısal hasar ve daha az stres belirteci vardı ve inflamatuar bağışıklık hücrelerinin invazyonu azalmıştı. Kültürlenmiş insan böbrek tübül hücrelerinde CRISPR gen düzenlemesiyle IFI16’nın silinmesi, hücreleri düşük oksijen ve ardından reoksijenasyonun neden olduğu hasara karşı daha dirençli hale getirerek hem sızıntılı, nekrotik hücre ölümünü hem de programlı apoptozu azalttı.
Demir, yağlar ve yıkıcı bir hücre ölümü biçimi
Klasik apoptozun ötesinde, yazarlar IFI16 ve p204’ün ferroptozu güçlü şekilde teşvik ettiğini gösterdiler; ferroptoz, demir ve hücre zarlarındaki yağların oksidatif hasarıyla beslenen bir hücre ölümü biçimidir. Yaralanmış fare böbreklerinde p204 kaybı, 4-hidroksinonenal ve malondialdehit gibi lipit hasarının kimyasal izlerini azalttı ve hassas yağ asitlerini zarara yükleyen enzim ACSL4 düzeylerini düşürdü. İnsan tübül hücrelerinde IFI16’nın yok edilmesi lipid peroksit birikimini azalttı, koruyucu antioksidan sistemleri (glutatyon yolunu ve enzim GPX4 dahil) güçlendirdi ve indirgenmiş/oksitlenmiş glutatyon dengesini geri getirdi. Ayrıca hücre içindeki serbest demir artışını, demir depolayan proteinleri koruyarak ve bir metal algılayıcı faktörün çekirdeğe geçişini destekleyerek sınırladı. Araştırmacılar farklı ölüm yollarını bloke eden ilaçlar kullandıklarında, ferroptozu engellemenin IFI16 fazla eksprese edilen hücreleri kurtarmada en güçlü etkiyi gösterdi; bu da bu proteinin yol açtığı yıkımda ferroptozun ana rota olduğunu vurguluyor.
DNA hasarından ferroptoz’a moleküler bir zincir
Daha derine inen çalışma, IFI16’nın hasar görmüş DNA ile ferroptoz arasındaki bir röle görevi gördüğünü haritalandırdı. İskemi/reperfüzyona benzer stres sonrası, IFI16 DNA kırıklarına ilk yanıt verenler arasında yer alan PARP-1’e bağlanıyor ve onun aktivitesini artırıyor. Bu, ATM kinazı merkezli ve ünlü bekçi protein p53’ü içeren bir DNA hasarı sinyal yolunun aşırı aktivasyonuna yol açıyor. Bu eksen aracılığıyla IFI16, hücresel enerji taşıyıcılarını tüketen, demir mevcudiyetini artıran, antioksidan savunmaları zayıflatan ve oksidatif zar hasarını teşvik eden sinyalleri yükseltiyor. PARP-1 veya ATM’in kimyasal engelleyicileri bu zararlı zinciri kırdı: antioksidan ve demir tamponlayıcı proteinleri geri getirdiler, demir ve lipid peroksidasyonunu azalttılar ve IFI16 düzeyleri yüksek olsa bile hücre ölümünü hafiflettiler. Yapısal deneyler ayrıca IFI16’nın hem DNA bağlayan HIN domainleri hem de protein etkileşimi sağlayan PYRIN domaininin PARP-1 ile etkileşim kurmak, DNA hasar yanıtını güçlendirmek ve ferroptozu tetiklemek için gerekli olduğunu ortaya koydu. 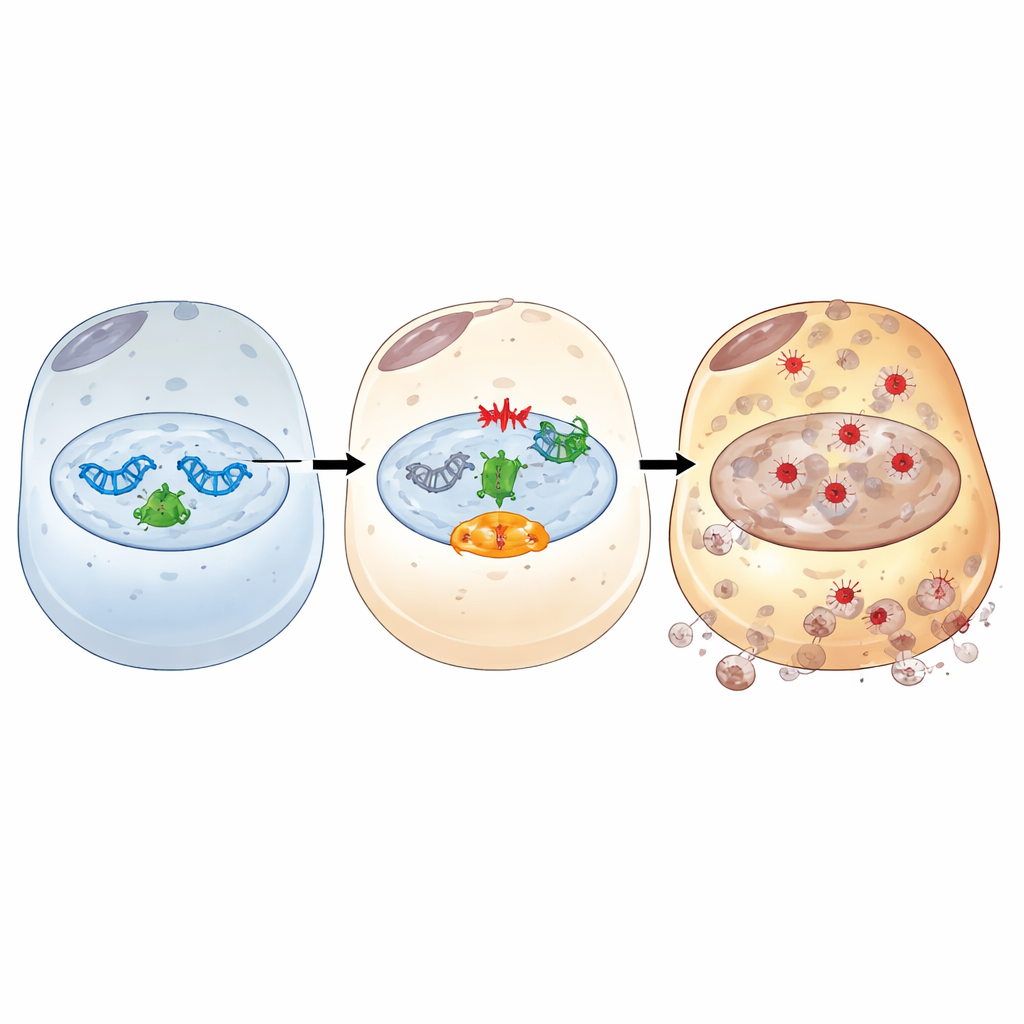
Yaralanmış böbrekleri korumak için yeni umut
Bu bulgular IFI16/p204’ü, böbrek tübül hücrelerindeki DNA yaralanmasını demirle beslenen bir yıkım dalgasına çeviren merkezi bir merkez olarak konumlandırıyor. DNA onarım mekanizmasını geniş çapta kapatmak—ki bu böbrek sonuçlarını kötüleştirebilir—yerine çalışma daha hassas bir strateji öneriyor: hücreleri hayatta kalmaktan ölüme iten aşırı, IFI16 kaynaklı hasar yanıtı kolunu baskılamak. Pratik olarak IFI16 aktivitesini azaltan, onun PARP-1 ile etkileşimini engelleyen veya hasarlı DNA’ya bağlanma yeteneğini bozacak terapiler akut böbrek hasarının etkisini hafifletebilir; ferroptozu ve birbirine bağlı diğer ölüm yollarını sınırlayabilir. Bu tür tedaviler geliştirilip insanlarda test edilmeyi beklese de, bu çalışma hedefe yönelik böbrek koruyucu ilaçlara doğru açık bir moleküler yol haritası çiziyor.
Atıf: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Anahtar kelimeler: akut böbrek hasarı, ferroptoz, DNA hasarına yanıt, böbrek tübül hücreleri, IFI16