Clear Sky Science · es
IFI16 es esencial para vincular el daño en el ADN y la ferroptosis en la lesión renal aguda
Por qué importa el estrés renal y la muerte celular
La lesión renal aguda es una pérdida repentina de la función renal que a menudo afecta a personas hospitalizadas tras cirugías mayores, infecciones o bajadas de presión arterial. Es frecuente, peligrosa y actualmente se trata en su mayoría con medidas de soporte como fluidos y diálisis, en lugar de fármacos dirigidos. Este estudio descubre una cadena de sucesos hasta ahora oculta dentro de las células del túbulo renal que conecta el daño en su ADN con una forma relativamente nueva de muerte celular impulsada por el hierro denominada ferroptosis. Al identificar una única molécula “interruptora”, el trabajo sugiere nuevas maneras de proteger los riñones cuando el flujo sanguíneo se corta y luego se restablece, como ocurre en muchas emergencias médicas.
Un desencadenante oculto dentro de las células renales
Los investigadores se centraron en las células que recubren los diminutos túbulos del riñón, que son especialmente vulnerables cuando el suministro de sangre y oxígeno se interrumpe y luego se reanuda, un proceso conocido como isquemia/reperfusión. Se fijaron en una proteína llamada IFI16 (y su homóloga en ratón p204), que normalmente ayuda a las células a detectar ADN extraño o dañado y decidir si reparar, inflamar o autodestruirse. Al examinar biopsias renales de pacientes con necrosis tubular aguda, una forma grave de lesión renal aguda, encontraron niveles mucho más altos de IFI16 en las células tubulares en comparación con riñones sanos, y la cantidad de IFI16 se correlacionó con marcadores sanguíneos de función renal deficiente. En ratones sometidos a isquemia/reperfusión renal, la versión murina p204 aumentó con el tiempo, especialmente en los núcleos de las células del túbulo proximal, el segmento que soporta la mayor parte del daño. 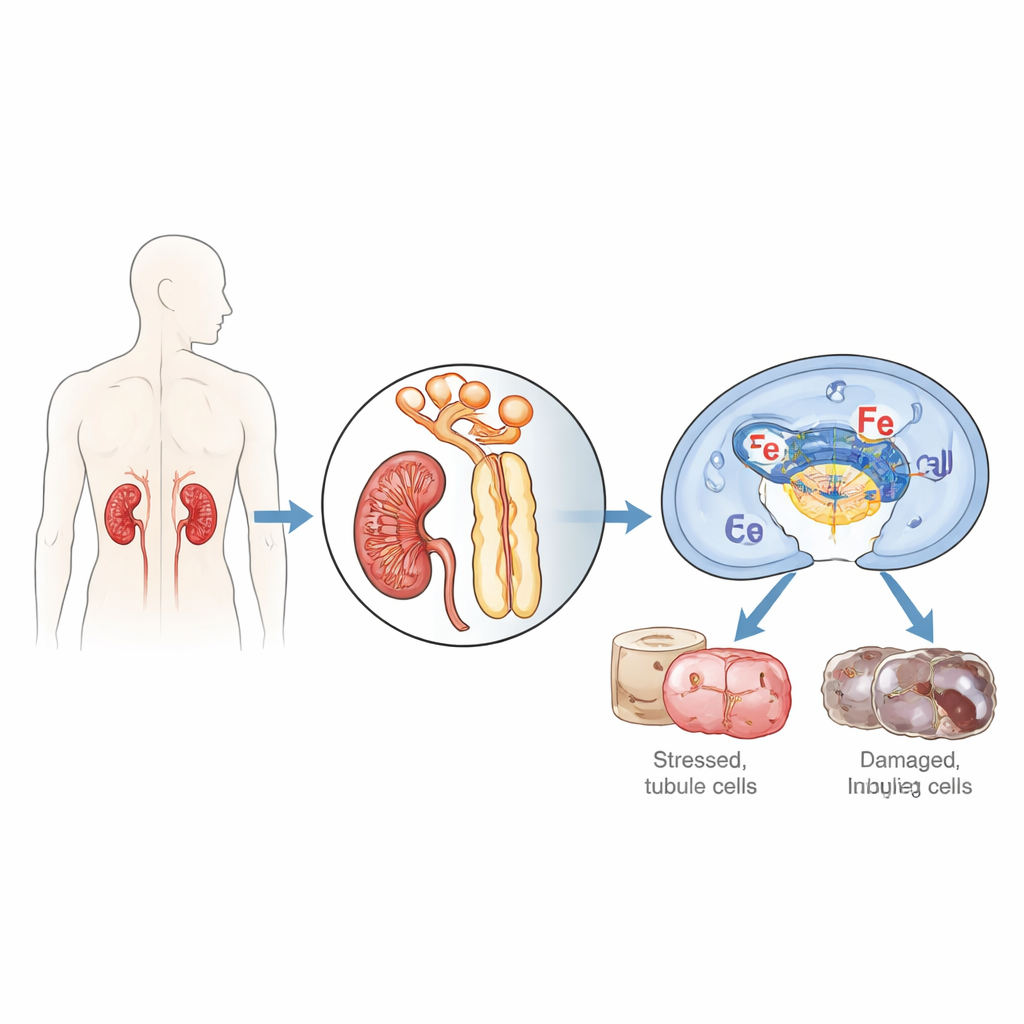
Apagar p204 atenúa el daño renal
Para comprobar si esta proteína perjudica activamente al riñón o solo es un mero espectador, el equipo generó ratones cuyos túbulos carecían específicamente de p204. Estos animales estaban sanos en lo general, pero cuando sus riñones se expusieron a isquemia/reperfusión, se comportaron mucho mejor que los ratones normales. Las pruebas sanguíneas mostraron creatinina y urea más bajas, lo que indica una mejor filtración renal. Al microscopio, sus túbulos presentaban menos daño estructural y menos marcadores de estrés, y hubo una menor invasión de células inmunitarias inflamatorias. En células tubulares humanas cultivadas, la eliminación de IFI16 mediante edición génica CRISPR también hizo que las células fueran más resistentes al daño por hipoxia seguida de reoxigenación, reduciendo tanto la muerte celular necrótica por filtración como la apoptosis programada.
Hierro, lípidos y una forma destructiva de muerte celular
Más allá de la apoptosis clásica, los autores demostraron que IFI16 y p204 promueven con fuerza la ferroptosis, una forma de muerte celular alimentada por el hierro y el daño oxidativo de los lípidos en las membranas. En riñones de ratón lesionados, la pérdida de p204 redujo las huellas químicas de daño lipídico, como 4-hidroxinonenal y malondialdehído, y atenuó los niveles de ACSL4, una enzima que incorpora ácidos grasos vulnerables en las membranas. En células tubulares humanas, la eliminación de IFI16 disminuyó la acumulación de peróxidos lipídicos, reforzó los sistemas antioxidantes protectores (incluida la vía del glutatión y la enzima GPX4) y restauró el equilibrio entre el glutatión reducido y el oxidado. También limitó el aumento de hierro libre dentro de las células al preservar proteínas almacenadoras de hierro y favorecer que un factor sensor de metales se traslade al núcleo. Cuando los investigadores emplearon fármacos para bloquear diferentes vías de muerte, la inhibición de la ferroptosis tuvo el efecto más potente para rescatar células con sobreexpresión de IFI16, lo que subraya a la ferroptosis como la ruta principal de destrucción impulsada por esta proteína.
Una cadena molecular desde el daño del ADN hasta la ferroptosis
Profundizando, el estudio trazó cómo IFI16 actúa como un relevo entre el ADN dañado y la ferroptosis. Tras un estrés similar a la isquemia/reperfusión, IFI16 se une a PARP-1, un primer respondededor clave ante roturas de ADN, y potencia su actividad. Esto hiperactiva una vía de señalización del daño del ADN centrada en la quinasa ATM y la famosa proteína guardiana p53. A través de este eje, IFI16 amplifica señales que agotan los portadores de energía celular, aumentan la disponibilidad de hierro, debilitan las defensas antioxidantes y favorecen el daño oxidativo de las membranas. Los bloqueadores químicos de PARP-1 o ATM rompieron esta cadena nociva: restauraron proteínas antioxidantes y tamponadoras de hierro, redujeron el hierro y la peroxidación lipídica, y disminuyeron la muerte celular, incluso cuando los niveles de IFI16 eran altos. Experimentos estructurales mostraron además que tanto los dominios HIN de unión al ADN como el dominio PYRIN de interacción proteica de IFI16 son necesarios para enganchar a PARP-1, potenciar la respuesta al daño del ADN y conducir a la ferroptosis. 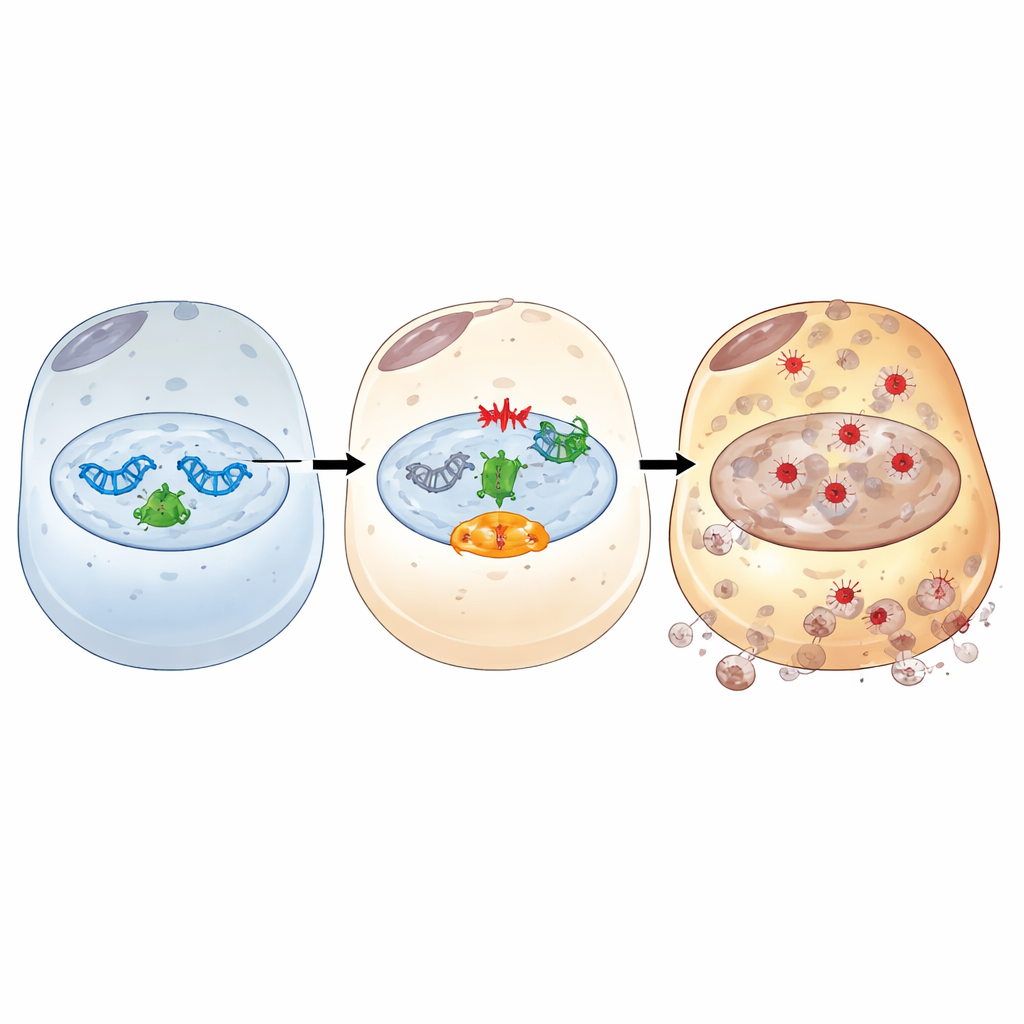
Nueva esperanza para proteger riñones lesionados
En conjunto, estos hallazgos sitúan a IFI16/p204 como un nodo central que convierte el daño del ADN en las células del túbulo renal en una ola de destrucción alimentada por hierro. En lugar de apagar de forma general la maquinaria de reparación del ADN —lo que puede empeorar los resultados renales—, el estudio sugiere una estrategia más precisa: atenuar el brazo excesivo impulsado por IFI16 de la respuesta al daño que inclina a las células desde la supervivencia hacia la muerte. En términos prácticos, terapias que reduzcan la actividad de IFI16, bloqueen su interacción con PARP-1 o dificulten su capacidad de unirse al ADN dañado podrían mitigar el impacto de la lesión renal aguda, limitando la ferroptosis así como otras vías de muerte entrelazadas. Aunque tales tratamientos aún deben desarrollarse y probarse en humanos, este trabajo traza una hoja de ruta molecular clara hacia fármacos protectores dirigidos al riñón.
Cita: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Palabras clave: lesión renal aguda, ferroptosis, respuesta al daño del ADN, células del túbulo renal, IFI16