Clear Sky Science · pl
IFI16 jest niezbędny do powiązania uszkodzenia DNA z ferroptozą w ostrym uszkodzeniu nerek
Dlaczego stres nerek i śmierć komórek mają znaczenie
Ostre uszkodzenie nerek to nagła utrata funkcji nerek, która często dotyka pacjentów hospitalizowanych po poważnych zabiegach chirurgicznych, infekcjach lub w przebiegu niskiego ciśnienia krwi. Jest powszechne, niebezpieczne i obecnie leczone głównie za pomocą wsparcia objawowego, takiego jak płyny i dializa, zamiast leków celowanych. To badanie ujawnia wcześniej nieznany ciąg zdarzeń wewnątrz komórek kanalików nerkowych, łączący uszkodzenie ich DNA z nowym rodzajem śmierci komórkowej napędzanej żelazem, zwanym ferroptozą. Wskazanie pojedynczej „przełączającej” cząsteczki sugeruje nowe sposoby ochrony nerek, gdy przepływ krwi jest odcinany, a potem przywracany, jak ma to miejsce w wielu sytuacjach kryzysowych medycznie.
Ukryty wyzwalacz wewnątrz komórek nerek
Naukowcy skupili się na komórkach wyścielających drobne kanaliki nerkowe, które są szczególnie podatne, gdy dopływ krwi i tlenu zostaje przerwany, a następnie wznowiony — proces znany jako niedokrwienie/ reperfuzja. Skoncentrowali się na białku nazwanym IFI16 (oraz jego mysim odpowiedniku p204), które normalnie pomaga komórkom wykrywać obce lub uszkodzone DNA i decydować, czy naprawiać, uruchamiać stan zapalny, czy ulegać autodestrukcji. Analiza biopsji nerek od pacjentów z ostrą martwicą kanalików, ciężką postacią ostrego uszkodzenia nerek, wykazała znacznie wyższe poziomy IFI16 w komórkach kanalików w porównaniu ze zdrowymi nerkami, a ilość IFI16 korelowała z krwinkowymi wskaźnikami pogorszenia czynności nerek. U myszy poddanych niedokrwieniu/reperfuzji nerek mysi odpowiednik p204 gwałtownie wzrastał w czasie, zwłaszcza w jądrach komórek kanalika bliższego, odcinka najbardziej narażonego na uraz. 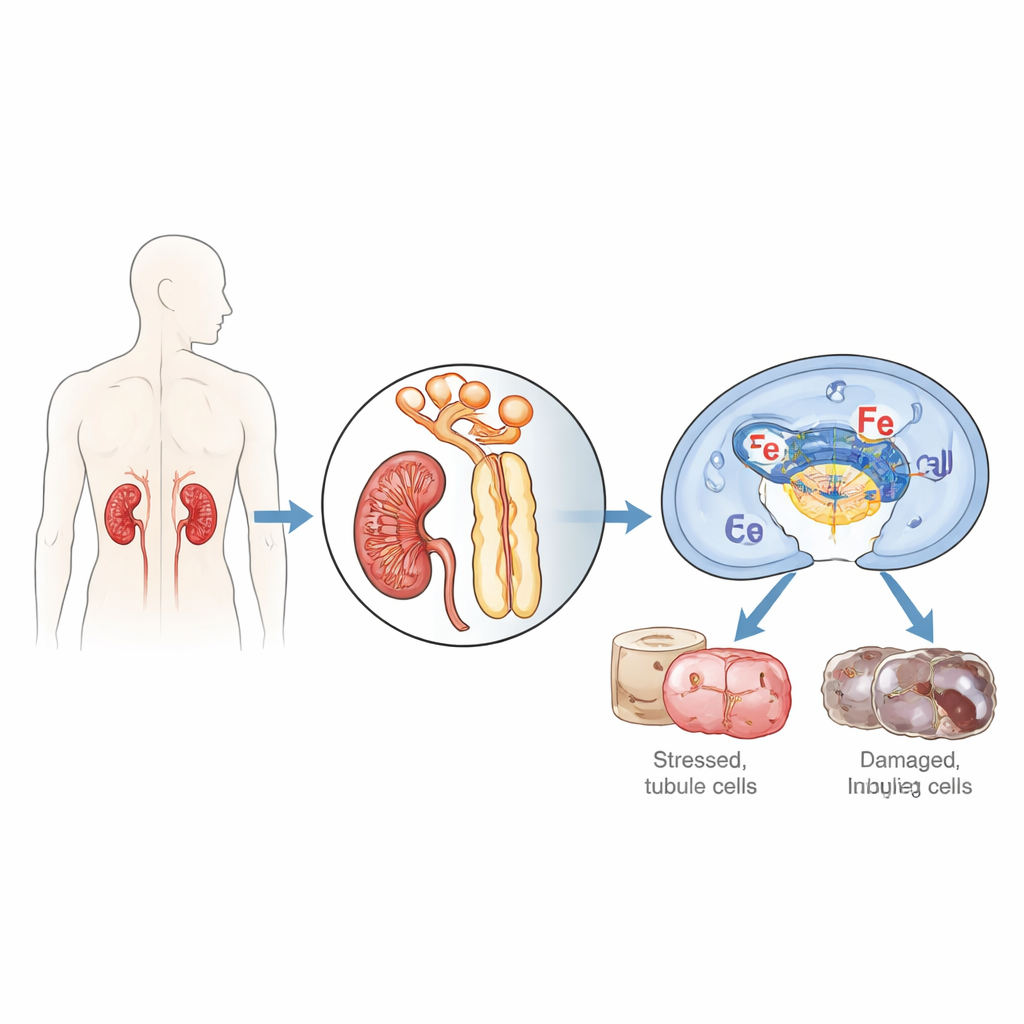
Wyłączenie p204 łagodzi uszkodzenie nerek
Aby sprawdzić, czy to białko aktywnie szkodzi nerce, czy jest tylko biernym obserwatorem, zespół zmodyfikował myszy tak, by ich komórki kanalików specyficznie nie posiadały p204. Zwierzęta te były w pozostałym zakresie zdrowe, ale gdy ich nerki zostały poddane niedokrwieniu/reperfuzji, radziły sobie znacznie lepiej niż myszy kontrolne. Badania krwi wykazały niższe stężenia kreatyniny i mocznika, co wskazuje na lepszą filtrację nerek. W preparatach mikroskopowych kanaliki miały mniejsze uszkodzenia strukturalne i mniej markerów stresu, a także zmniejszoną inwazję zapalnych komórek odpornościowych. W hodowlach ludzkich komórek kanalików nerkowych usunięcie IFI16 metodą edycji genów CRISPR również uczyniło komórki bardziej odpornymi na uraz wywołany niedotlenieniem i ponowną oksygenacją, ograniczając zarówno przeciekającą martwicę, jak i zaprogramowaną apoptozę.
Żelazo, tłuszcze i destrukcyjna forma śmierci komórki
Ponad klasyczną apoptozą autorzy wykazali, że IFI16 i p204 silnie wspierają ferroptozę, rodzaj śmierci komórkowej napędzanej żelazem i oksydacyjnym uszkodzeniem lipidów w błonach komórkowych. W uszkodzonych nerkach myszy utrata p204 zmniejszyła chemiczne ślady uszkodzeń lipidów, takie jak 4-hydroksynonenal i malondialdehyd, oraz obniżyła poziomy ACSL4, enzymu ładującego podatne kwasy tłuszczowe do błon. W ludzkich komórkach kanalików wyłączenie IFI16 ograniczyło gromadzenie nadtlenków lipidów, wzmocniło ochronne systemy antyoksydacyjne (w tym szlak glutationowy i enzym GPX4) oraz przywróciło równowagę zredukowanego i utlenionego glutationsu. Ograniczyło też nagły wzrost wolnego żelaza w komórkach poprzez zachowanie białek magazynujących żelazo i ułatwienie przeniesienia czynnika wykrywającego metale do jądra. Gdy badacze stosowali leki blokujące różne ścieżki śmierci komórkowej, hamowanie ferroptozy miało najsilniejszy efekt ratunkowy w komórkach nadekspresyjnych IFI16, wskazując ferroptozę jako główną drogę destrukcji napędzaną przez to białko.
Cząsteczkowy łańcuch od uszkodzenia DNA do ferroptozy
Zagłębiając się dalej, badanie nakreśliło, jak IFI16 działa jako przekaźnik między uszkodzonym DNA a ferroptozą. Po stresie podobnym do niedokrwienia/reperfuzji IFI16 wiąże się z PARP-1, kluczowym pierwszym reagującym na pęknięcia DNA, i zwiększa jego aktywność. To nadaktywowanie uruchamia szlak sygnalizacji uszkodzeń DNA skoncentrowany wokół kinazy ATM i znanego białka strażnika p53. Poprzez tę oś IFI16 wzmacnia sygnały prowadzące do wyczerpywania nośników energii komórkowej, zwiększenia dostępności żelaza, osłabienia obrony antyoksydacyjnej i sprzyjania oksydacyjnemu uszkodzeniu błon. Blokery chemiczne PARP-1 lub ATM przerwały ten szkodliwy łańcuch: przywracały białka antyoksydacyjne i buforujące żelazo, zmniejszały żelazo i peroksydację lipidów oraz łagodziły śmierć komórek, nawet gdy poziomy IFI16 były wysokie. Doświadczenia strukturalne dodatkowo wykazały, że zarówno domeny HIN wiążące DNA, jak i domena PYRIN łącząca się z białkami IFI16 są wymagane do zaangażowania PARP-1, wzmocnienia odpowiedzi na uszkodzenie DNA i napędzania ferroptozy. 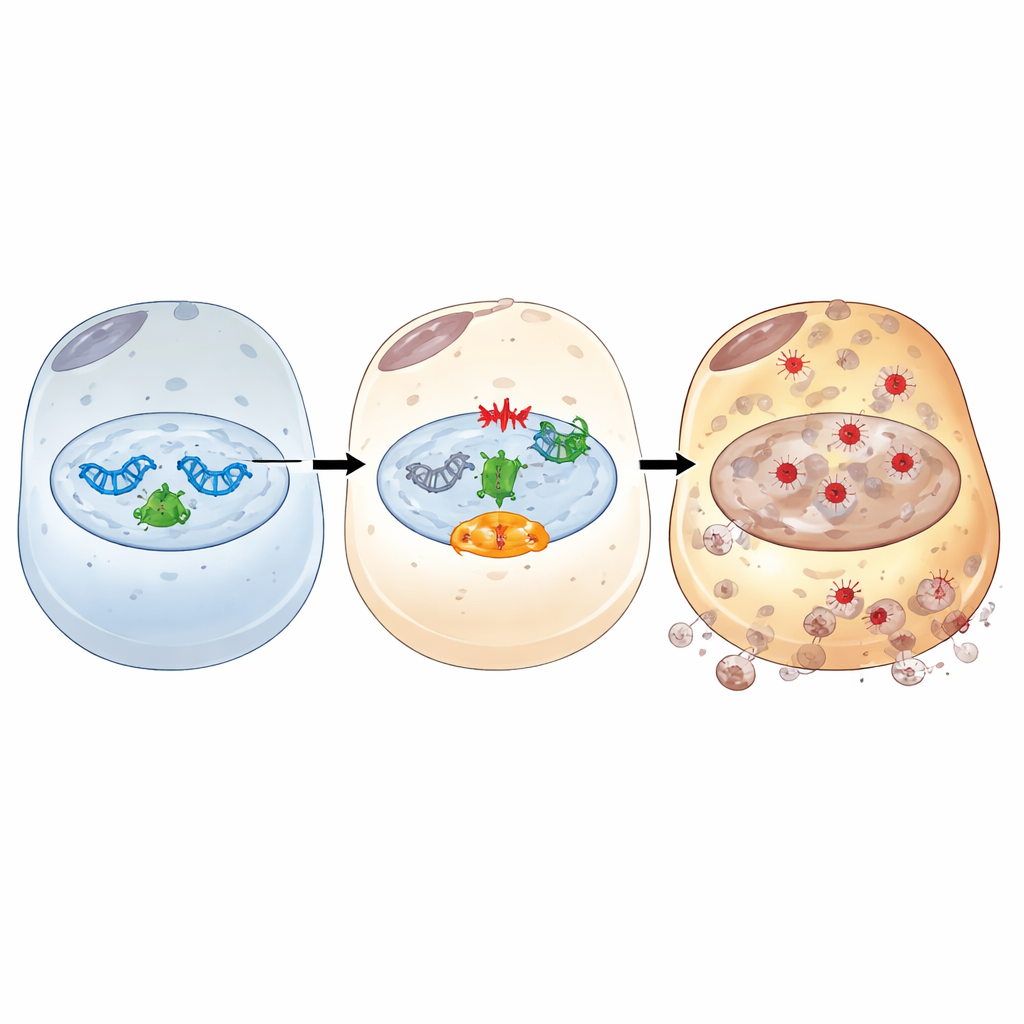
Nowa nadzieja na ochronę uszkodzonych nerek
W sumie te ustalenia lokują IFI16/p204 jako centralne ogniwo przekształcające uszkodzenie DNA w komórkach kanalików nerkowych w falę zniszczenia napędzanego żelazem. Zamiast szeroko hamować mechanizmy naprawy DNA — co może pogorszyć rokowanie nerek — badanie proponuje bardziej precyzyjną strategię: stłumienie nadmiernej, napędzanej przez IFI16 gałęzi odpowiedzi na uszkodzenie, która przesuwa komórki ze stanu przeżycia ku śmierci. W praktyce terapie zmniejszające aktywność IFI16, blokujące jego interakcję z PARP-1 lub zakłócające jego zdolność do wiązania uszkodzonego DNA mogłyby złagodzić skutki ostrego uszkodzenia nerek, ograniczając ferroptozę i inne powiązane drogi śmierci. Choć takie leki pozostają do opracowania i przetestowania u ludzi, praca ta wytycza jasną molekularną mapę drogową do celowanych leków chroniących nerki.
Cytowanie: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Słowa kluczowe: ostre uszkodzenie nerek, ferroptoza, odpowiedź na uszkodzenie DNA, komórki kanalików nerkowych, IFI16