Clear Sky Science · pt
IFI16 é essencial para conectar dano ao DNA e ferroptose na lesão renal aguda
Por que o estresse renal e a morte celular importam
A lesão renal aguda é uma perda súbita da função renal que frequentemente acomete pessoas hospitalizadas após cirurgias maiores, infecções ou episódios de pressão arterial baixa. É comum, perigosa e atualmente tratada em sua maior parte com medidas de suporte, como fluidos e diálise, em vez de fármacos direcionados. Este estudo revela uma cadeia de eventos até então oculta dentro das células dos túbulos renais que liga o dano ao DNA a uma forma mais recente de morte celular movida por ferro chamada ferroptose. Ao identificar uma única molécula “interruptora”, o trabalho sugere novas maneiras de proteger os rins quando o fluxo sanguíneo é interrompido e depois restaurado, como ocorre em muitas emergências médicas.
Um gatilho escondido dentro das células renais
Os pesquisadores concentraram-se nas células que revestem os minúsculos túbulos do rim, especialmente vulneráveis quando o suprimento de sangue e oxigênio é interrompido e depois reiniciado, processo conhecido como isquemia/reperfusão. Eles focalizaram uma proteína chamada IFI16 (e seu equivalente em camundongos, p204), que normalmente ajuda as células a detectar DNA estranho ou danificado e decidir se devem reparar, inflamar ou se autodestruir. Ao examinar biópsias renais de pacientes com necrose tubular aguda, uma forma grave de lesão renal aguda, encontraram níveis muito mais altos de IFI16 nas células dos túbulos em comparação com rins saudáveis, e a quantidade de IFI16 acompanhou marcadores sanguíneos de função renal prejudicada. Em camundongos submetidos à isquemia/reperfusão renal, a versão murina p204 aumentou ao longo do tempo, especialmente nos núcleos das células do túbulo proximal, o segmento que suporta a maior parte da lesão. 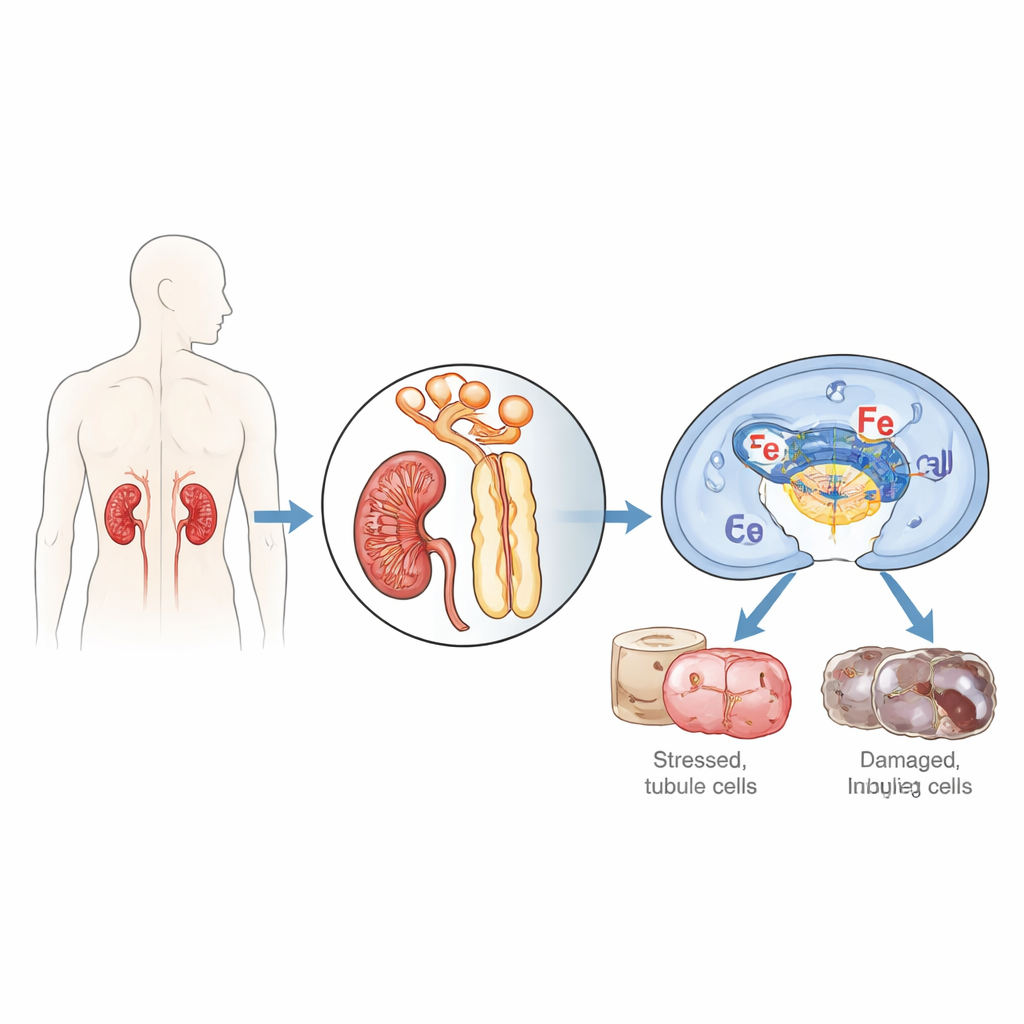
Desligar p204 alivia o dano renal
Para testar se essa proteína prejudica ativamente o rim ou é apenas uma espectadora, a equipe criou camundongos cujas células dos túbulos renalmente específicas não expressavam p204. Esses animais eram saudáveis por fora, mas quando seus rins foram expostos à isquemia/reperfusão, tiveram resultado muito melhor do que camundongos normais. Exames de sangue mostraram creatinina e uréia mais baixas, indicando filtração renal melhor. Ao microscópio, seus túbulos apresentaram menos dano estrutural e menos marcadores de estresse, além de menor invasão de células imunes inflamatórias. Em células de túbulo renal humano cultivadas, a deleção de IFI16 usando edição gênica CRISPR também tornou as células mais resistentes a lesão por baixo oxigênio seguida de reoxigenação, reduzindo tanto a morte celular necroticamente vazante quanto a apoptose programada.
Ferro, gorduras e uma forma destrutiva de morte celular
Além da apoptose clássica, os autores mostraram que IFI16 e p204 promovem fortemente a ferroptose, uma forma de morte celular alimentada por ferro e pelo dano oxidativo de lipídios nas membranas celulares. Em rins de camundongo lesionados, a perda de p204 reduziu sinais químicos de dano lipídico, como 4-hidroxinonenal e malondialdeído, e diminuiu os níveis de ACSL4, uma enzima que incorpora ácidos graxos vulneráveis às membranas. Em células de túbulo humano, a exclusão de IFI16 reduziu o acúmulo de peróxidos lipídicos, reforçou sistemas antioxidantes protetores (incluindo a via do glutationa e a enzima GPX4) e restaurou o equilíbrio entre glutationa reduzida e oxidada. Também limitou o aumento de ferro livre dentro das células ao preservar proteínas armazenadoras de ferro e ajudar um fator sensor de metal a translocar-se para o núcleo. Quando os pesquisadores usaram drogas para bloquear diferentes vias de morte, a inibição da ferroptose teve o efeito mais forte em resgatar células com superexpressão de IFI16, destacando a ferroptose como a principal rota de destruição conduzida por essa proteína.
Uma cadeia molecular do dano ao DNA à ferroptose
Avançando, o estudo mapeou como IFI16 atua como um relé entre o DNA danificado e a ferroptose. Após um estresse semelhante à isquemia/reperfusão, IFI16 liga-se à PARP-1, um respondededor inicial chave às quebras no DNA, e potencializa sua atividade. Isso hiperativa uma via de sinalização de dano ao DNA centrada na quinase ATM e na famosa proteína guardiã p53. Por esse eixo, IFI16 amplifica sinais que esgotam transportadores de energia celular, aumentam a disponibilidade de ferro, enfraquecem defesas antioxidantes e favorecem o dano oxidativo às membranas. Bloqueadores químicos de PARP-1 ou ATM interromperam essa cadeia nociva: restauraram proteínas antioxidantes e tamponadoras de ferro, reduziram ferro e peroxidação lipídica e diminuíram a morte celular, mesmo quando os níveis de IFI16 estavam altos. Experimentos estruturais revelaram ainda que tanto os domínios HIN de ligação ao DNA quanto o domínio PYRIN de interação proteica de IFI16 são necessários para engajar PARP-1, intensificar a resposta ao dano ao DNA e promover a ferroptose. 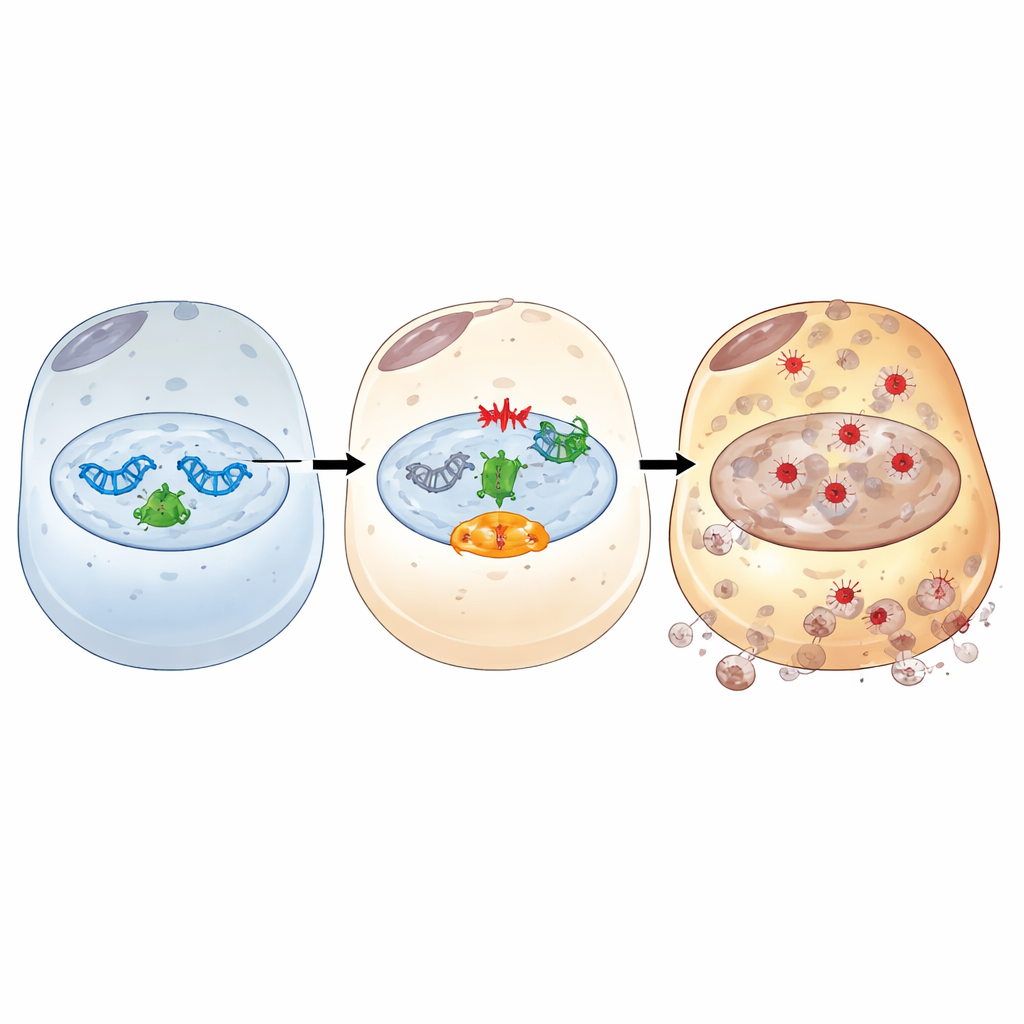
Nova esperança para proteger rins lesionados
Em conjunto, essas descobertas posicionam IFI16/p204 como um ponto central que transforma o dano ao DNA nas células dos túbulos renais em uma onda de destruição alimentada por ferro. Em vez de desligar amplamente a maquinaria de reparo do DNA — o que pode piorar os desfechos renais —, o estudo sugere uma estratégia mais precisa: conter o braço excessivo e dirigido por IFI16 da resposta ao dano que inclina as células da sobrevivência para a morte. Em termos práticos, terapias que reduzam a atividade de IFI16, bloqueiem sua interação com PARP-1 ou interrompam sua capacidade de ligar-se ao DNA danificado poderiam amenizar o impacto da lesão renal aguda, limitando a ferroptose e outras vias de morte interligadas. Embora tais tratamentos ainda precisem ser desenvolvidos e testados em humanos, este trabalho traça um roteiro molecular claro rumo a fármacos renoprotetores direcionados.
Citação: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Palavras-chave: lesão renal aguda, ferroptose, resposta ao dano ao DNA, células dos túbulos renais, IFI16