Clear Sky Science · ar
IFI16 ضروري لربط تلف الحمض النووي والفِرُوبتوسيس في الفشل الكلوي الحاد
لماذا يهم إجهاد الكلية وموت الخلايا
الفشل الكلوي الحاد هو فقدان مفاجئ لوظيفة الكلية يحدث غالبًا للمرضى في المستشفى بعد جراحة كبرى أو إصابات أو انخفاض ضغط الدم. إنه شائع وخطير، والعلاج الحالي يقوم بشكل أساسي على إجراءات داعمة مثل السوائل وغسيل الكلى بدلاً من أدوية موجهة حقيقية. تكشف هذه الدراسة سلسلة أحداث كانت مخفية سابقًا داخل خلايا أنابيب الكلية تربط تلف الحمض النووي لديها بشكل مباشر بنمط جديد من موت الخلايا المدفوع بالحديد يسمى الفِرُوبتوسيس. من خلال تحديد جزيء "مفتاح" واحد، يقترح العمل طرقًا جديدة لحماية الكليتين عندما يُقطع تدفق الدم ثم يُستعاد، كما يحدث في العديد من الطوارئ الطبية.
مثير خفي داخل خلايا الكلية
ركز الباحثون على الخلايا التي تبطن الأنابيب الدقيقة في الكلية، وهي عرضة بشكل خاص عندما ينقطع تزويد الدم والأكسجين ثم يُستعاد، وهي عملية تُعرف بنقص التروية/إعادة التروية. تم التركيز على بروتين يسمى IFI16 (ونظيره في الفأر p204)، الذي يساعد عادة الخلايا على استشعار الحمض النووي الأجنبي أو التالف واتخاذ قرار الإصلاح أو إحداث التهاب أو الانتحار الخلوي. عند فحص خزعات كلوية من مرضى لديهم نخر أنابيب حاد، وهو شكل شديد من الفشل الكلوي الحاد، وجدوا مستويات أعلى بكثير من IFI16 في خلايا الأنابيب مقارنة بالكلى السليمة، وكانت كمية IFI16 مرتبطة بعلامات في الدم تدل على ضعف وظيفة الكلية. في الفئران المعرضة لنقص التروية/إعادة التروية الكلوية، ارتفع مستوى p204 بمرور الوقت، خاصة في أنوية خلايا القناة القريبة، وهي القطعة التي تتحمل معظم الضرر. 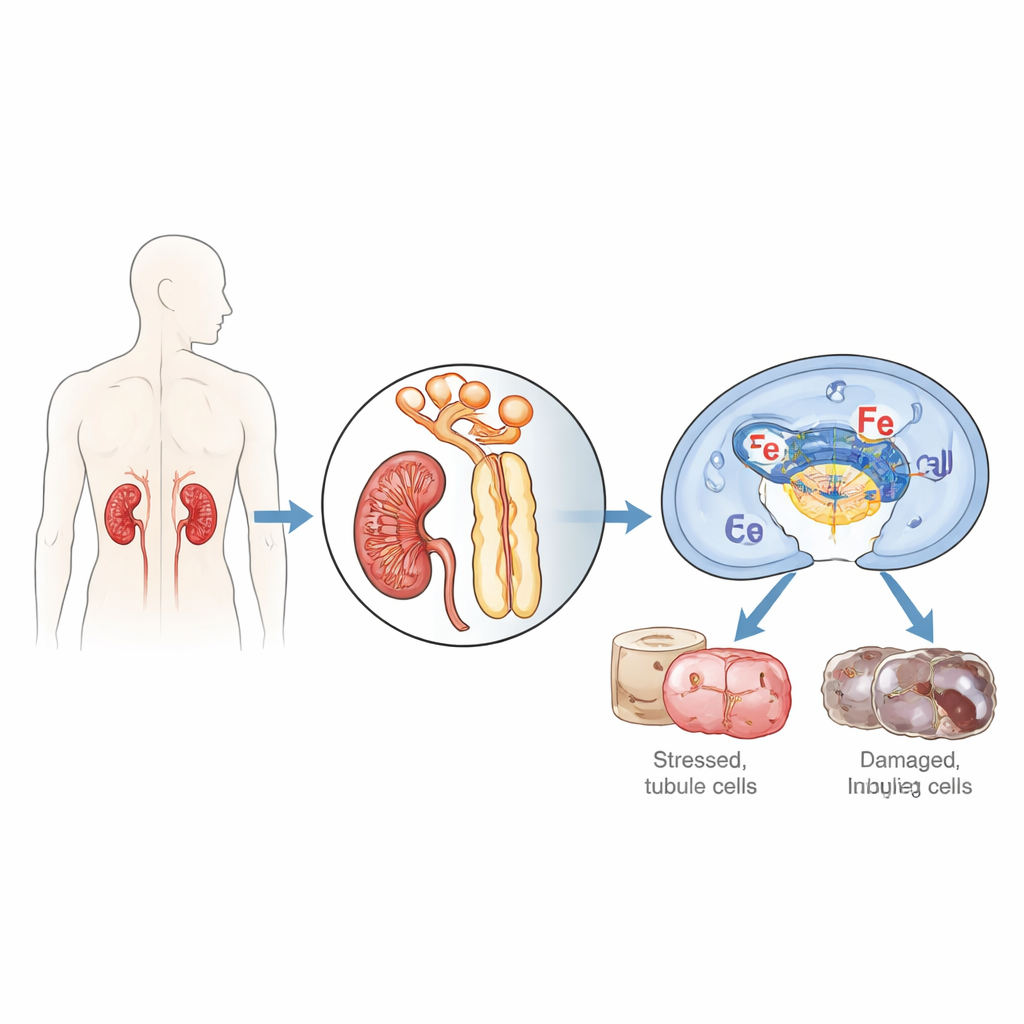
إيقاف p204 يخفف من ضرر الكلية
لاختبار ما إذا كان هذا البروتين يسبب الضرر فعلاً أم أنه مجرد مراقب، صنّع الفريق فئرانًا تفتقر خلايا أنابيبها بشكل محدد إلى p204. كانت هذه الحيوانات بصحة عامة جيدة، ولكن عندما تعرضت كليتاها لنقص التروية/إعادة التروية، كانت نتائجها أفضل بكثير من الفئران الطبيعية. أظهرت اختبارات الدم انخفاضًا في الكرياتينين واليوريا، مما يشير إلى ترشيح كلوي أفضل. تحت المجهر، كانت أنابيبها أقل تضررًا ومليئة بعلامات إجهاد أقل، كما لوحظ انخفاض في غزو الخلايا المناعية المسببة للالتهاب. في خلايا أنابيب بشرية مزروعة، جعلت إزالة IFI16 باستخدام تعديل الجينات بواسطة CRISPR الخلايا أكثر مقاومة للإصابة نتيجة نقص الأكسجين ثم إعادة التأكسج، فحدّت من كل من الموت التنكسي المتسرب والموت المبرمج (الاستماتة).
الحديد والدهون وشكل مدمّر من موت الخلايا
بعيدًا عن الاستماتة الكلاسيكية، أظهر المؤلفون أن IFI16 وp204 يعززان بقوة الفِرُوبتوسيس، وهو شكل من الموت الخلوي تغذيه الحديد والأضرار التأكسدية للدهون في أغشية الخلايا. في كلى الفئران المصابة، قلّ غياب p204 من آثار تفاعلية كيميائية لتلف الدهون، مثل 4-هيدروكسينونينال ومالونالديهايد، وتراجعت مستويات ACSL4، وهو إنزيم يحمّل الأحماض الدهنية الضعيفة إلى الأغشية. في خلايا الأنابيب البشرية، قلّ بناء فوق أكسيدات الدهون بعد حذف IFI16، وزادت أنظمة مضادات الأكسدة الوقائية (بما في ذلك مسار الغلوتاثيون والإنزيم GPX4)، وأعيد توازن الغلوتاثيون المختزل والمأكسد. كما حدّ ذلك من اندفاع الحديد الحر داخل الخلايا عن طريق الحفاظ على بروتينات تخزين الحديد ومساعدة عامل استشعار المعادن على الانتقال إلى النواة. عندما استخدم الباحثون أدوية لحجب مسارات موت مختلفة، كان تثبيط الفِرُوبتوسيس الأكثر فاعلية في إنقاذ الخلايا ذات الإفراط في التعبير عن IFI16، ما يبرز الفِرُوبتوسيس كالمسار الرئيسي للتدمير الذي يقوده هذا البروتين.
سلسلة جزيئية من تلف الحمض النووي إلى الفِرُوبتوسيس
بالتعمق أكثر، خرّطت الدراسة كيف يعمل IFI16 كمرحلة وصل بين الحمض النووي التالف والفِرُوبتوسيس. بعد إجهاد شبيه بنقص التروية/إعادة التروية، يرتبط IFI16 بـ PARP-1، المستجيب الأولي الرئيسي لكسور الحمض النووي، ويعزز نشاطه. هذا ينشط بشكل مفرط مسار إشارات تلف الحمض النووي المرتكز على كيناز ATM والبروتين الحارس الشهير p53. عبر هذا المحور، يضخم IFI16 الإشارات التي تُستنزف حاملات الطاقة الخلوية، وتزيد توفر الحديد، وتضعف دفاعات مضادات الأكسدة، وتميل نحو تلف الأغشية التأكسدي. مكبّحات كيميائية لـ PARP-1 أو ATM كسرت هذه السلسلة الضارة: أعادت بروتينات مضادات التأكسد وتخزين الحديد، وخفضت الحديد ودرجة أكسدة الدهون، وقللت موت الخلايا، حتى عندما كانت مستويات IFI16 مرتفعة. كشفت تجارب هيكلية كذلك أن كلًا من مجالات HIN المرتبطة بربط الحمض النووي والمجال PYRIN المتفاعل مع البروتين في IFI16 مطلوبة للالتقاء بـ PARP-1، وتعزيز استجابة تلف الحمض النووي، وتحفيز الفِرُوبتوسيس. 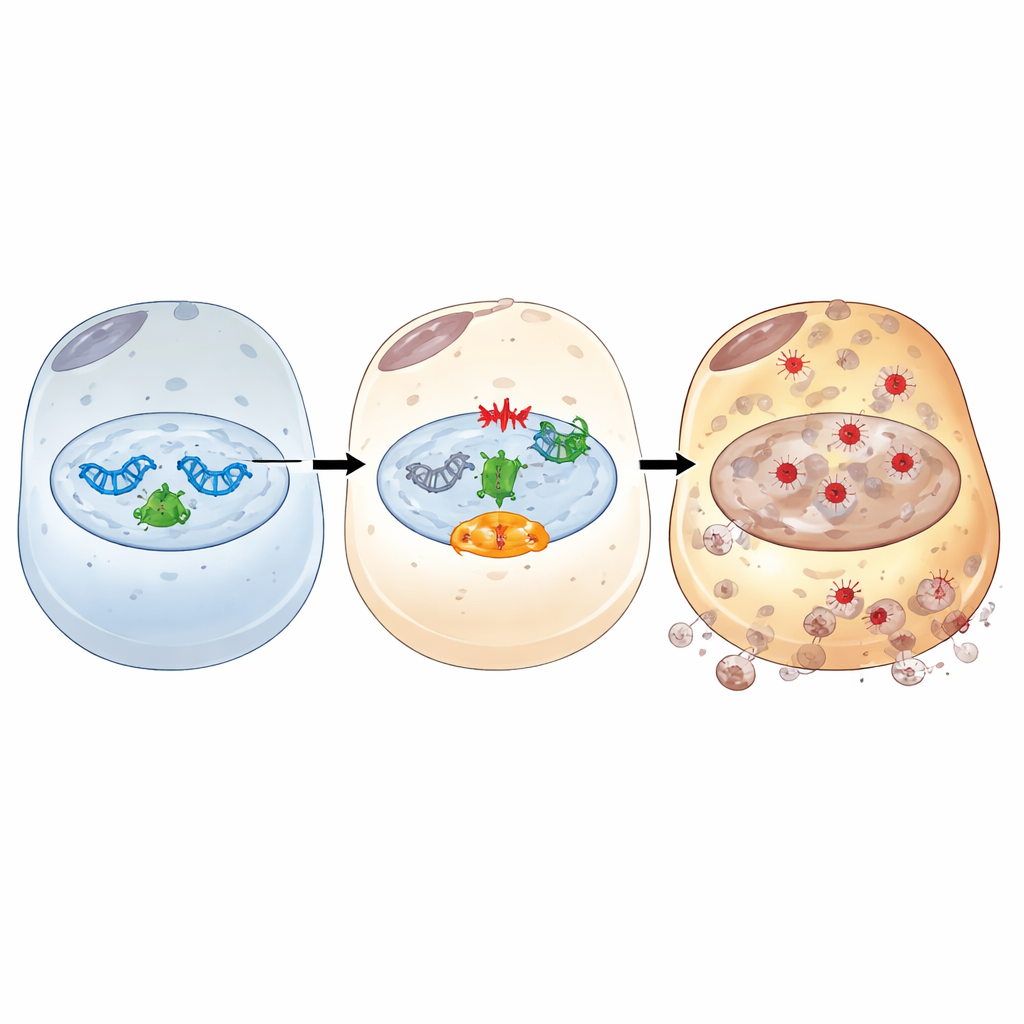
أمل جديد لحماية الكليتين المصابة
معًا، تضع هذه النتائج IFI16/p204 كمحور مركزي يحول إصابة الحمض النووي في خلايا أنابيب الكلية إلى موجة تدمير مدفوعة بالحديد. بدلاً من إيقاف آليات إصلاح الحمض النووي بشكل واسع—وهو ما قد يفاقم نتائج الكلية—تقترح الدراسة استراتيجية أكثر دقة: كبح الذراع المفرطة والمحفزة بواسطة IFI16 في استجابة التلف التي تقلب موازين الخلايا من البقاء إلى الموت. عمليًا، قد تخفف العلاجات التي تقلل نشاط IFI16 أو تمنع تفاعله مع PARP-1 أو تعطل قدرته على ربط الحمض النووي التالف من وطأة الفشل الكلوي الحاد، محدودةً الفِرُوبتوسيس وكذلك مسارات موت مترابطة أخرى. وبينما تظل مثل هذه العلاجات بحاجة للتطوير والاختبار في البشر، ترسم هذه الدراسة خارطة جزيئية واضحة نحو أدوية موجهة لحماية الكلية.
الاستشهاد: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
الكلمات المفتاحية: الفشل الكلوي الحاد, الفِرُوبتوسيس, استجابة تلف الحمض النووي, خلايا أنابيب الكلية, IFI16