Clear Sky Science · fr
IFI16 est essentiel pour relier les dommages à l’ADN et la ferroptose dans l’insuffisance rénale aiguë
Pourquoi le stress rénal et la mort cellulaire comptent
L’insuffisance rénale aiguë est une perte soudaine de la fonction rénale qui touche souvent des patients hospitalisés après une chirurgie majeure, des infections ou une baisse de tension artérielle. Elle est fréquente, dangereuse et traitée aujourd’hui principalement par des mesures de soutien — comme des perfusions et la dialyse — plutôt que par des médicaments ciblés. Cette étude dévoile une chaîne d’événements jusque-là cachée au sein des cellules tubulaires rénales qui relie les dommages de l’ADN à une forme plus récente de mort cellulaire conduite par le fer, appelée ferroptose. En identifiant une molécule « commutatrice » unique, le travail suggère de nouvelles pistes pour protéger les reins lorsque le flux sanguin est coupé puis rétabli, comme cela se produit lors de nombreux urgences médicales.
Un déclencheur caché à l’intérieur des cellules rénales
Les chercheurs se sont concentrés sur les cellules qui tapissent les petits tubes du rein, particulièrement vulnérables lorsque l’apport sanguin et en oxygène est interrompu puis rétabli, un processus connu sous le nom d’ischémie/reperfusion. Ils ont étudié une protéine nommée IFI16 (et son homologue murin p204), qui aide normalement les cellules à détecter de l’ADN étranger ou endommagé et à décider de réparer, d’induire une inflammation ou de s’autodétruire. En examinant des biopsies rénales de patients souffrant de nécrose tubulaire aiguë, une forme sévère d’insuffisance rénale aiguë, ils ont trouvé des niveaux beaucoup plus élevés d’IFI16 dans les cellules tubulaires par rapport à des reins sains, et la quantité d’IFI16 corrélait avec des marqueurs sanguins d’un mauvais fonctionnement rénal. Chez des souris soumises à une ischémie/reperfusion rénale, la version murine p204 augmentait fortement au fil du temps, en particulier dans les noyaux des cellules du tubule proximal, le segment le plus touché par la lésion. 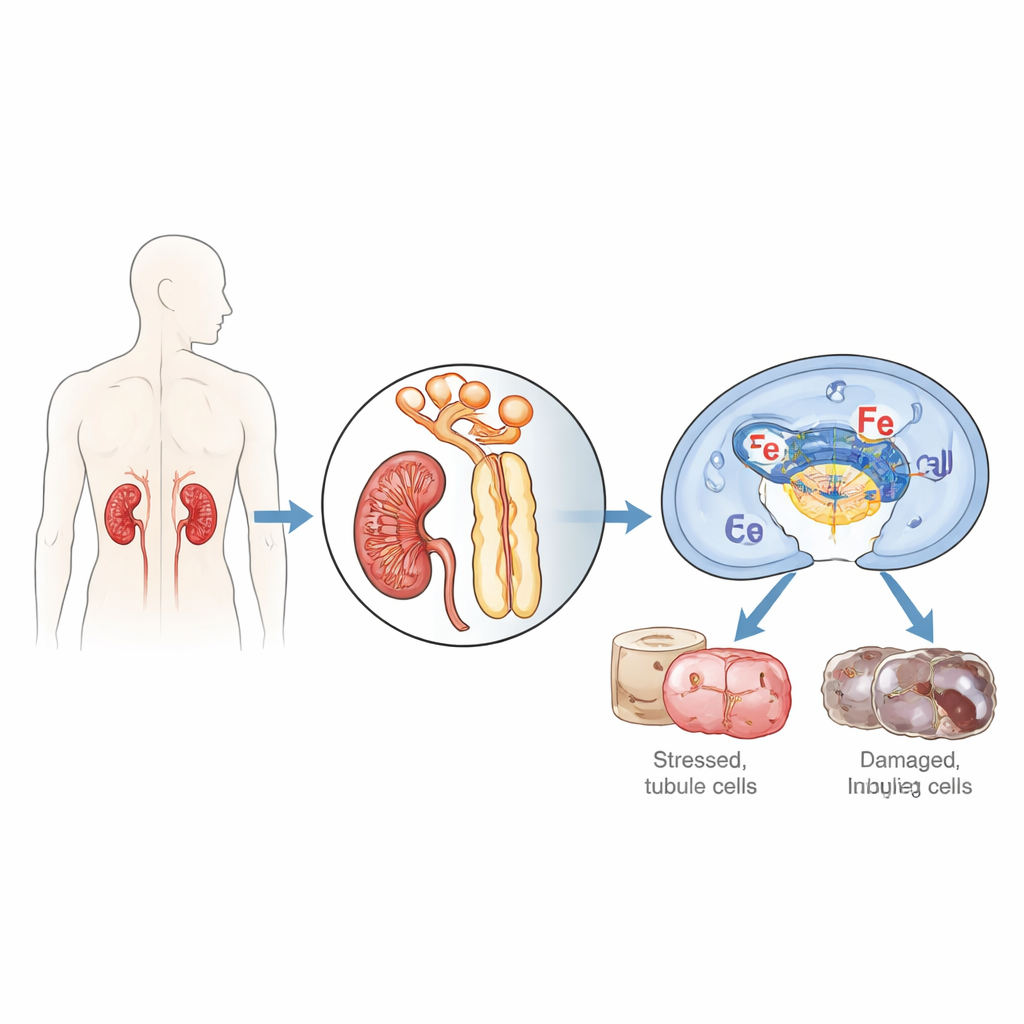
Éteindre p204 atténue les lésions rénales
Pour tester si cette protéine est activement dommageable ou simplement un spectateur, l’équipe a généré des souris dont les cellules tubulaires étaient spécifiquement dépourvues de p204. Ces animaux étaient par ailleurs en bonne santé, mais lorsque leurs reins ont été exposés à l’ischémie/reperfusion, ils se sont révélés bien mieux protégés que des souris normales. Les analyses sanguines montraient une créatinine et une urée plus basses, indiquant une meilleure filtration rénale. À la microscopy, leurs tubules présentaient moins de dégâts structurels et moins de marqueurs de stress, et l’infiltration de cellules immunitaires inflammatoires était réduite. Dans des cellules tubulaires rénales humaines en culture, la suppression d’IFI16 par édition génique CRISPR a également rendu les cellules plus résistantes aux lésions induites par l’hypoxie suivie de la réoxygénation, diminuant à la fois la mort nécrotique par fuite et l’apoptose programmée.
Fer, lipides et une forme destructrice de mort cellulaire
Au-delà de l’apoptose classique, les auteurs ont montré qu’IFI16 et p204 favorisent fortement la ferroptose, une forme de mort cellulaire alimentée par le fer et par l’oxydation des lipides membranaires. Dans les reins moussus lésés, la perte de p204 réduisait les empreintes chimiques de dégâts lipidiques, comme le 4-hydroxynonénal et le malondialdéhyde, et abaissait les niveaux d’ACSL4, une enzyme qui incorpore des acides gras vulnérables dans les membranes. Dans des cellules tubulaires humaines, l’inactivation d’IFI16 diminuait l’accumulation de peroxydes lipidiques, renforçait les systèmes antioxydants protecteurs (y compris la voie du glutathion et l’enzyme GPX4) et rétablissait l’équilibre entre glutathion réduit et oxydé. Elle limitait aussi la hausse du fer libre intracellulaire en préservant les protéines de stockage du fer et en favorisant la translocation nucléaire d’un facteur sensible au métal. Lorsque les chercheurs ont utilisé des médicaments pour bloquer différentes voies de mort, l’inhibition de la ferroptose a eu l’effet le plus marqué pour sauver des cellules surexprimant IFI16, mettant en évidence la ferroptose comme la principale voie de destruction induite par cette protéine.
Une chaîne moléculaire des dommages à l’ADN à la ferroptose
Allant plus loin, l’étude a cartographié comment IFI16 agit comme relais entre l’ADN endommagé et la ferroptose. Après un stress de type ischémie/reperfusion, IFI16 se lie à PARP-1, un acteur clé de la réponse immédiate aux cassures d’ADN, et en amplifie l’activité. Cela hyperactive une voie de signalisation des dommages de l’ADN centrée sur la kinase ATM et la célèbre protéine sentinelle p53. Par cet axe, IFI16 amplifie des signaux qui épuisent les transporteurs d’énergie cellulaire, augmentent la disponibilité du fer, affaiblissent les défenses antioxydantes et favorisent l’oxydation des membranes. Des bloqueurs chimiques de PARP-1 ou d’ATM interrompaient cette chaîne délétère : ils rétablissaient les protéines antioxydantes et de stockage du fer, réduisaient le fer et la peroxydation lipidique, et diminuaient la mort cellulaire, même lorsque les niveaux d’IFI16 étaient élevés. Des expériences structurelles ont en outre montré que les domaines HIN liant l’ADN et le domaine PYRIN d’interaction protéique d’IFI16 sont tous deux nécessaires pour engager PARP-1, renforcer la réponse aux dommages de l’ADN et conduire à la ferroptose. 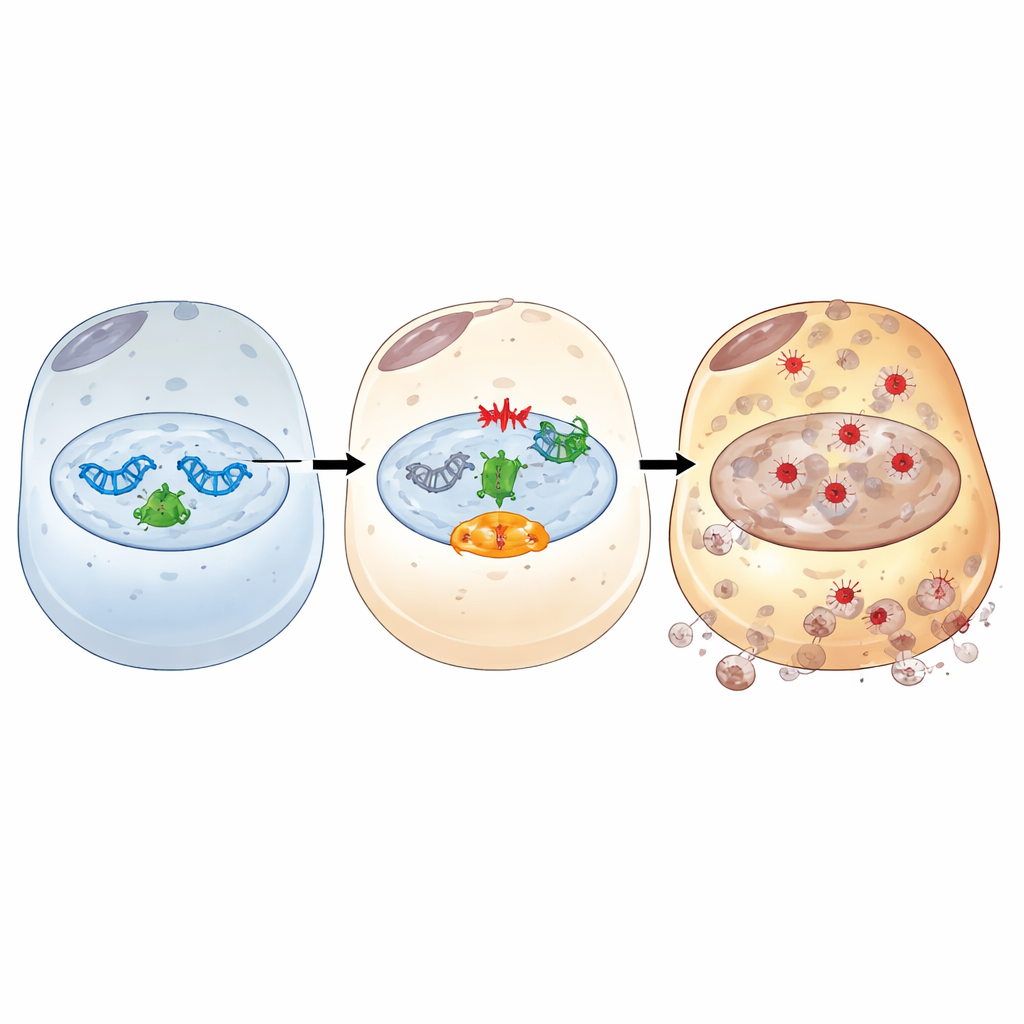
Un nouvel espoir pour protéger les reins lésés
Pris ensemble, ces résultats positionnent IFI16/p204 comme un carrefour central qui convertit les lésions de l’ADN dans les cellules tubulaires rénales en une vague de destruction alimentée par le fer. Plutôt que de couper de manière large la machinerie de réparation de l’ADN — ce qui peut aggraver le pronostic rénal — l’étude propose une stratégie plus précise : tempérer le bras excessif, piloté par IFI16, de la réponse aux dommages qui bascule les cellules de la survie vers la mort. Concrètement, des thérapies réduisant l’activité d’IFI16, bloquant son interaction avec PARP-1 ou perturbant sa capacité à se lier à l’ADN endommagé pourraient atténuer l’impact de l’insuffisance rénale aiguë, en limitant la ferroptose ainsi que d’autres voies de mort entremêlées. Bien que de tels traitements restent à développer et à tester chez l’humain, ce travail trace une feuille de route moléculaire claire vers des médicaments ciblés protecteurs pour le rein.
Citation: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Mots-clés: insuffisance rénale aiguë, ferroptose, réponse aux dommages de l’ADN, cellules des tubules rénaux, IFI16