Clear Sky Science · he
IFI16 חיוני לקישור בין נזק לדנ״א ופרוטופטוזיס בפגיעה חדה בכליה
מדוע מתח בכליות ומות תאים חשובים
פגיעה חריפה בכליה היא אובדן פתאומי של תפקוד כלייתי שמתרחש לעתים קרובות בחולים מאושפזים אחרי ניתוחים נרחבים, זיהומים או לחץ דם נמוך. היא נפוצה, מסוכנת וכיום מטופלת בעיקר באמצעים תומכים כמו נוזלים ודיאליזה ולא בתרופות ממוקדות אמיתיות. המחקר הזה חושף שרשרת אירועים שטמונה בתוך תאי צינורית הכליה, שמקשרת בין פגיעה בדנ״א לצורת מוות תאית חדשה המונעת על ידי ברזל בשם פרוטופטוזיס. בזיהוי מולקולת "מתג" בודדת, העבודה מציעה דרכים חדשות להגן על הכליות כאשר אספקת הדם מוקטנת ואז משוחזרת — כמו שקורה במצבים רפואיים רבים.
ציר סתרים בתוך תאי הכליה
החוקרים התרכזו בתאים המצפים את הצינורות הזעירים של הכליה, שנוטים להיפגע במיוחד כשאספקת הדם והחמצן מופרעת ואז מושהית, תהליך הידוע כאיסכמיה/רפרפוזיה. הם התמקדו בחלבון בשם IFI16 (ובמקביל בעכבר — p204), שלרוב מסייע לתאים לחוש דנ״א זר או פגום ולקבל החלטה אם לתקן, להפעיל דלקת או להיכנע למוות עצמי. בבדיקות ביופסיה של כליות מחולים עם נמק צינורי חריף, צורה קשה של פגיעה חריפה בכליה, נמצאו רמות גבוהות בהרבה של IFI16 בתאי הצינורית בהשוואה לכליות בריאות, וכמות IFI16 תואמת לסמנים בדם שמעידים על תפקוד כלייתי ירוד. בעכברים שנחשפו לאיסכמיה/רפרפוזיה בכליה, הגרסה העכברית p204 עלתה עם הזמן, במיוחד בגרעינים של תאי הצינורית הפרוקסימלית — המקטע שסובל את מירב הפגיעה. 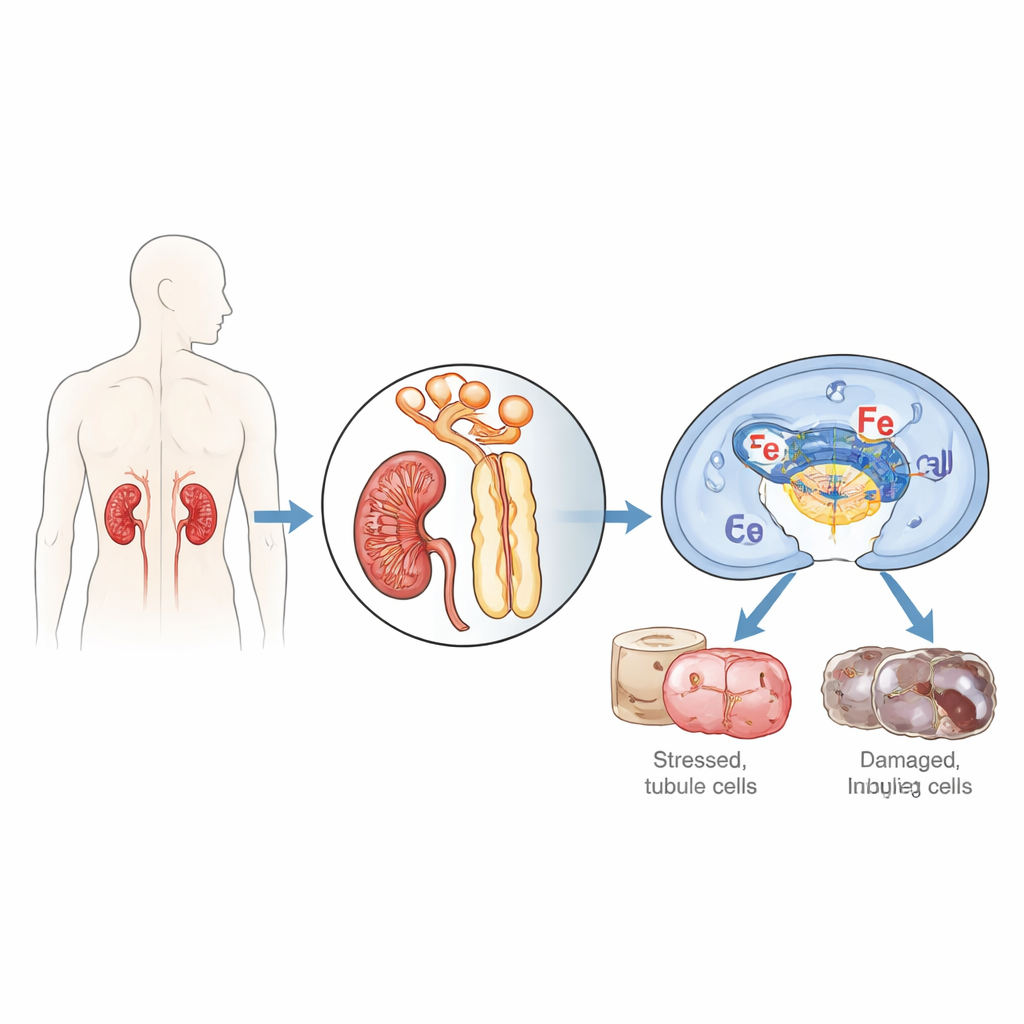
כיבוי p204 מקל על נזק כלייתי
כדי לבחון האם החלבון הזה מזיק באופן פעיל לכליה או שהוא רק צופה מהצד, הקבוצה מייצרת עכברים שתאי הצינורית שלהם חסרים ספציפית את p204. בעלי החיים היו בריאים במובנים אחרים, אך כאשר כליותיהם נחשפו לאיסכמיה/רפרפוזיה הם התמודדו הרבה יותר טוב מאשר עכברי בקרה. בדיקות דם הראו יצור נמוך יותר של קריאטינין ואוראה, דבר שמעיד על סינון כלייתי משופר. במיקרוסקופ נראו צינורות עם פחות נזק מבני ופחות סמנים של מתח, והייתה חדירה מופחתת של תאי מערכת החיסון דלקתיים. בתרביות של תאי צינורית כלייתית אנושיים, השמטת IFI16 בעזרת עריכת גנים CRISPR גם הפכה את התאים לעמידים יותר לפגיעה מחוסר חמצן ואחריו החזרת חמצן, והקטינה הן מוות נקרוטי מדולף והן אפופטוזה מתוכנתת.
ברזל, שומנים וצורת מוות הרסנית
מעבר לאפופטוזה הקלאסית, המחברים הראו ש־IFI16 ו־p204 מקדמים בחוזקה את הפרוטופטוזיס, צורת מוות תאית המונעת על ידי ברזל ונזק חמצוני לשומנים בממברנות התאים. בכליות פגועות של עכברים, חיסרון p204 הפחית טביעות כימיות של נזק לשומנים, כגון 4‑הידרוקסי־נוננל ומלדיאלדהיד, והוריד רמות של ACSL4 — אנזים שמטעין חומצות שומן פגיעות בממברנות. בתאי צינורית אנושיים, ניתוח IFI16 הוריד בניית פרוקסי־שמן (peroxide) של שומנים, חיזק מערכות אנטיאוקסידנטיות מגן (כולל מסלול גלוטתיון והאנזים GPX4), והשיב את האיזון בין גלוטתיון מחוזר למחומצן. הוא גם הגביל את גל העלייה של הברזל החופשי בתוך התאים על ידי שימור חלבונים המאחסנים ברזל וסיוע לגורם חישה מתכתי להיכנס לגרעין. כשחוקרים השתמשו בתרופות שחוסמות מסלולי מוות שונים, עיכוב הפרוטופטוזיס נתן את ההשפעה החזקה ביותר בהצלת תאים בעלי ביטוי יתר של IFI16, ובכך מדגיש את הפרוטופטוזיס כנתיב ההרס המרכזי שמונע על ידי חלבון זה.
שרשרת מולקולרית מנזק דנ״א לפרוטופטוזיס
בהעמקה, המחקר מיפוי איך IFI16 פועל כרלֶה בין דנ״א פגום לפרוטופטוזיס. אחרי מתח בדמה הדומה לאיסכמיה/רפרפוזיה, IFI16 נקשר ל־PARP‑1 — מגיב ראשון מרכזי לשברי דנ״א — ומגביר את פעילותו. זאת מובילה להיפראקטיבציה של מסלול איתות לנזק דנ״א שמרכזו קינאזת ATM וחלבון השומר המוכר p53. דרך ציר זה, IFI16 מרחיבה אותות שמדלדלות נשאי אנרגיה תאיים, מגדילות זמינות של ברזל, מחלישות הגנות אנטי־חמצוניות ומעדיפות נזק חמצוני לממברנות. חוסמים כימיים של PARP‑1 או ATM שבקו את השרשרת המזיקה: הם שיקמו חלבוני הגנה אנטיאוקסידנטיים ומאזני ברזל, הפחיתו ברזל ופרוקסיונציית שומנים, והקטינו מוות תאי — גם כאשר רמות IFI16 היו גבוהות. ניסויים מבניים חשפו בנוסף ששני מתחמי HIN הקשורים לקשירת דנ״א וכן מתחם PYRIN המשתתף באינטראקציה חלבון־חלבון של IFI16 נדרשים כדי להעסיק את PARP‑1, להגביר את תגובת הנזק בדנ״א ולדחוף פרוטופטוזיס. 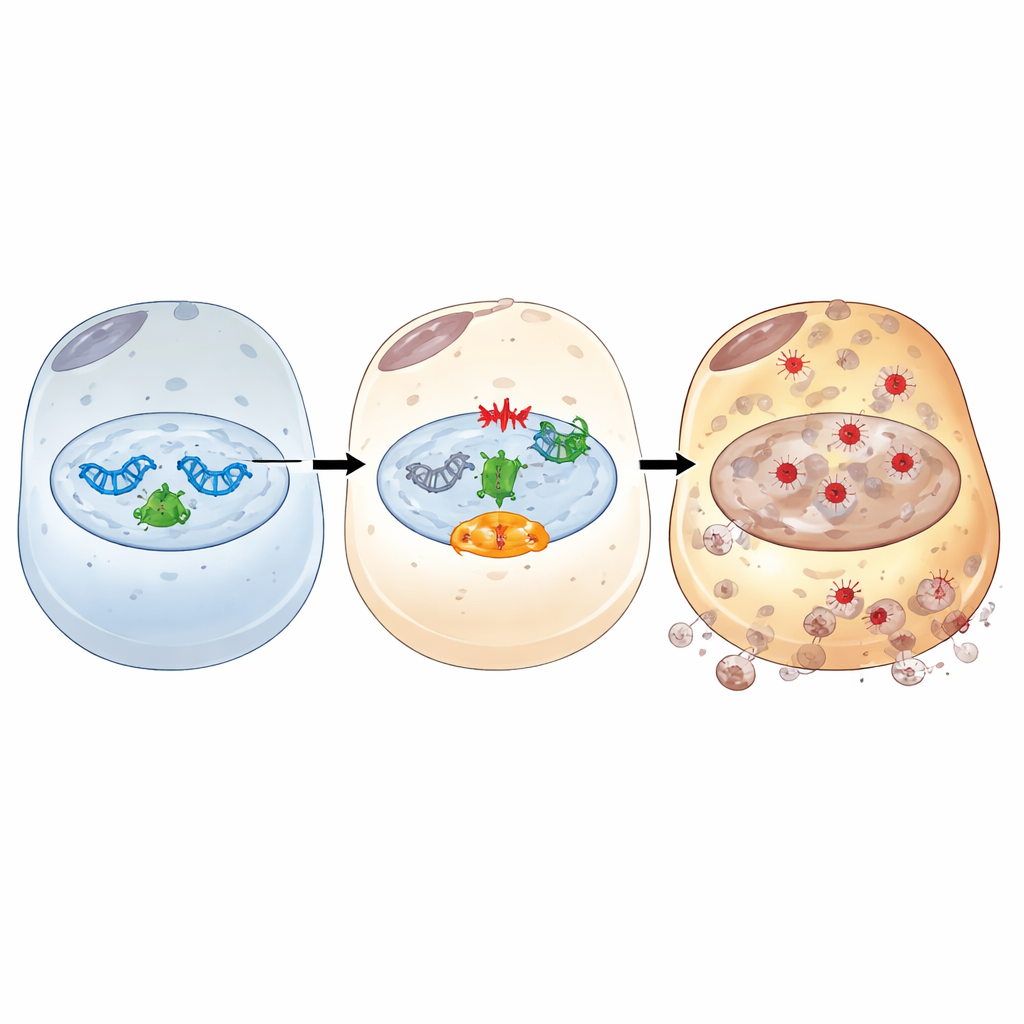
תקווה חדשה להגנה על כליות פגועות
ביחד, ממצאים אלה מציבים את IFI16/p204 כצומת מרכזית שהופכת פגיעה בדנ״א בתאי צינורית כלייתית לגל של הרס מונע ברזל. במקום לכבות באופן רחב את מכונת תיקון הדנ״א — מה שיכול להחמיר תוצאות כלייתיות — המחקר מציע אסטרטגיה מדויקת יותר: להקטין את הזרוע המופרזת המונעת על ידי IFI16 בתגובה לנזק, שמטה תאים מהישרדות אל מות. במונחים מעשיים, טיפולים שמפחיתים פעילות IFI16, חוסמים את אינטראקצייתו עם PARP‑1, או מפריעים ליכולתו לקשור דנ״א פגום יכולים להמתן את הפגיעה של פגיעה חריפה בכליה, ולהגביל את הפרוטופטוזיס כמו גם מסלולי מוות אחרים שמשולבים בו. אף שהטיפולים הללו עדיין נדרשים לפיתוח ומבחנים בבני אדם, עבודה זו משרטטת מפת דרך מולקולרית ברורה לעבר תרופות ממוקדות שיגנו על הכליה.
ציטוט: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
מילות מפתח: פגיעה חריפה בכליה, פרוטופטוזיס, תגובה לנזק דנ״א, תאי צינורית כלייתית, IFI16