Clear Sky Science · de
IFI16 ist entscheidend dafür, DNA-Schädigung mit Ferroptose bei akutem Nierenversagen zu verbinden
Warum Nierenstress und Zelltod wichtig sind
Akutes Nierenversagen ist ein plötzlicher Verlust der Nierenfunktion, der häufig bei Krankenhauspatienten nach größeren Operationen, Infektionen oder niedrigem Blutdruck auftritt. Es ist verbreitet, gefährlich und wird derzeit meist mit unterstützenden Maßnahmen wie Flüssigkeitszufuhr und Dialyse behandelt, statt mit gezielten Medikamenten. Diese Studie deckt eine bisher verborgene Abfolge von Ereignissen in Nierentubuluszellen auf, die Schäden an der DNA mit einer neueren Form des eisenabhängigen Zelltods, der Ferroptose, verbindet. Indem sie ein einzelnes „Schalters“molekül identifizieren, weist die Arbeit auf neue Wege hin, Nieren zu schützen, wenn der Blutfluss abgeschnitten und anschließend wiederhergestellt wird, wie es bei vielen medizinischen Notfällen vorkommt.
Ein verborgener Auslöser in Nierenzellen
Die Forscher konzentrierten sich auf die Zellen, die die winzigen Tubuli der Niere auskleiden und besonders empfindlich sind, wenn Blut- und Sauerstoffversorgung unterbrochen und dann wieder aufgenommen werden – ein Prozess, der als Ischämie/Reperfusion bezeichnet wird. Sie richteten ihr Augenmerk auf ein Protein namens IFI16 (und dessen Maus-Pendant p204), das normalerweise Zellen hilft, fremde oder beschädigte DNA zu erkennen und zu entscheiden, ob repariert, Entzündungen ausgelöst oder Selbstzerstörung eingeleitet werden soll. Bei der Untersuchung von Nierenbiopsien von Patienten mit akuter Tubulusnekrose, einer schweren Form des akuten Nierenversagens, fanden sie deutlich höhere IFI16-Werte in den Tubuluszellen im Vergleich zu gesunden Nieren, und die Menge an IFI16 korrelierte mit Blutwerten, die auf schlechte Nierenfunktion hinweisen. Bei Mäusen, die einer Nierenischämie/Reperfusion ausgesetzt wurden, stieg die Mausversion p204 im Zeitverlauf stark an, insbesondere in den Zellkernen der proximalen Tubuluszellen, jenem Abschnitt, der am stärksten vom Schaden betroffen ist. 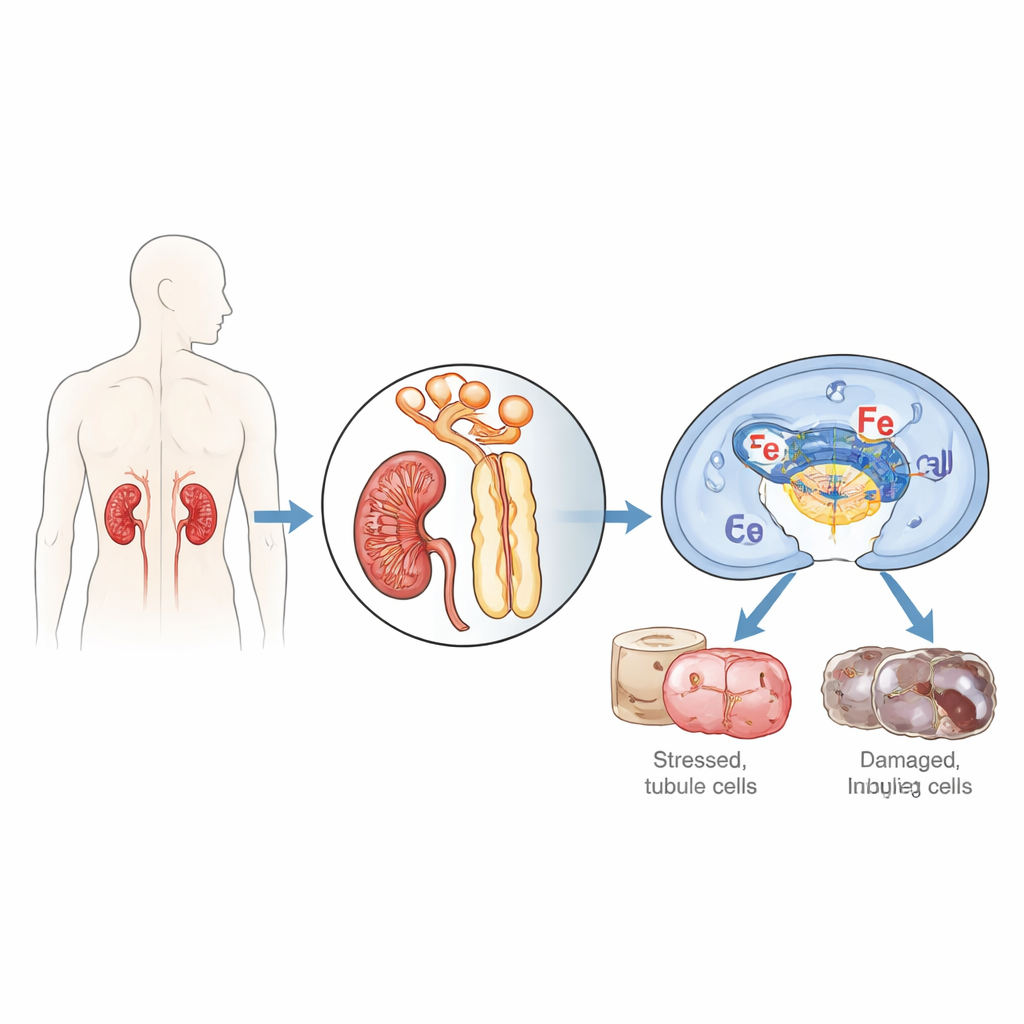
p204 auszuschalten lindert Nierenschäden
Um zu prüfen, ob dieses Protein aktiv der Niere schadet oder nur ein Beifang ist, erzeugte das Team Mäuse, deren Tubuluszellen gezielt kein p204 aufwiesen. Diese Tiere waren sonst gesund, erlitten aber bei Nierenischämie/Reperfusion deutlich weniger Schaden als normale Mäuse. Bluttests zeigten niedrigere Kreatinin- und Harnstoffwerte, was auf eine bessere Nierenfiltration hindeutet. Unter dem Mikroskop zeigten ihre Tubuli weniger strukturelle Schäden und weniger Stressmarker, außerdem war die Invasion entzündlicher Immunzellen reduziert. In kultivierten menschlichen Nierentubuluszellen machte die Deletion von IFI16 mittels CRISPR-Geneditierung die Zellen ebenfalls widerstandsfähiger gegen Verletzungen durch Sauerstoffmangel gefolgt von Reoxygenierung und verringerte sowohl das undichte, nekrotische Zelltodgeschehen als auch die programmierte Apoptose.
Eisen, Fette und eine zerstörerische Todesform
Über die klassische Apoptose hinaus zeigten die Autoren, dass IFI16 und p204 die Ferroptose stark fördern – eine Form des Zelltods, die von Eisen und der oxidativen Schädigung von Fetten in Zellmembranen angetrieben wird. In geschädigten Mäusenieren reduzierte der Verlust von p204 die chemischen Spuren von Lipidoxidation, wie 4-Hydroxynonenal und Malondialdehyd, und dämpfte die Mengen an ACSL4, einem Enzym, das anfällige Fettsäuren in Membranen einbaut. In menschlichen Tubuluszellen senkte das Ausschalten von IFI16 die Ansammlung von Lipidperoxiden, stärkte schützende Antioxidanssysteme (einschließlich des Glutathionwegs und des Enzyms GPX4) und stellte das Gleichgewicht von reduziertem und oxidiertem Glutathion wieder her. Es begrenzte auch den Anstieg von freiem Eisen in den Zellen, indem es eisenlagernde Proteine bewahrte und einem metall-sensitiven Faktor half, in den Zellkern zu gelangen. Als die Forscher Medikamente einsetzten, um verschiedene Todeswege zu blockieren, hatte die Hemmung der Ferroptose die stärkste Wirkung beim Rettungsversuch von IFI16-überexprimierenden Zellen, was Ferroptose als den hauptsächlichen vom Protein getriebenen Zerstörungsweg hervorhebt.
Eine molekulare Kette von DNA-Schäden bis zur Ferroptose
In tiefer gehenden Untersuchungen kartierten die Autoren, wie IFI16 als Relais zwischen beschädigter DNA und Ferroptose wirkt. Nach ischämieähnlichem Stress bindet IFI16 an PARP-1, einen wichtigen Ersthelfer bei DNA-Brüchen, und steigert dessen Aktivität. Dies hyperaktiviert eine DNA-Schadens-Signalkaskade, die vom ATM-Kinaseweg und dem bekannten Wächterprotein p53 ausgeht. Über diese Achse verstärkt IFI16 Signale, die zelluläre Energievorräte entleeren, die Eisenverfügbarkeit erhöhen, antioxidative Abwehr schwächen und oxidative Membranschäden begünstigen. Chemische Hemmer von PARP-1 oder ATM durchbrachen diese schädliche Kette: Sie stellten antioxidantische und eisen-puffernde Proteine wieder her, reduzierten Eisen- und Lipidperoxidation und verringerten den Zelltod, selbst bei hohen IFI16-Werten. Strukturuntersuchungen zeigten außerdem, dass sowohl die DNA-bindenden HIN-Domänen als auch die proteininteragierende PYRIN-Domäne von IFI16 erforderlich sind, um PARP-1 zu engagieren, die DNA-Schadensantwort zu verstärken und Ferroptose zu treiben. 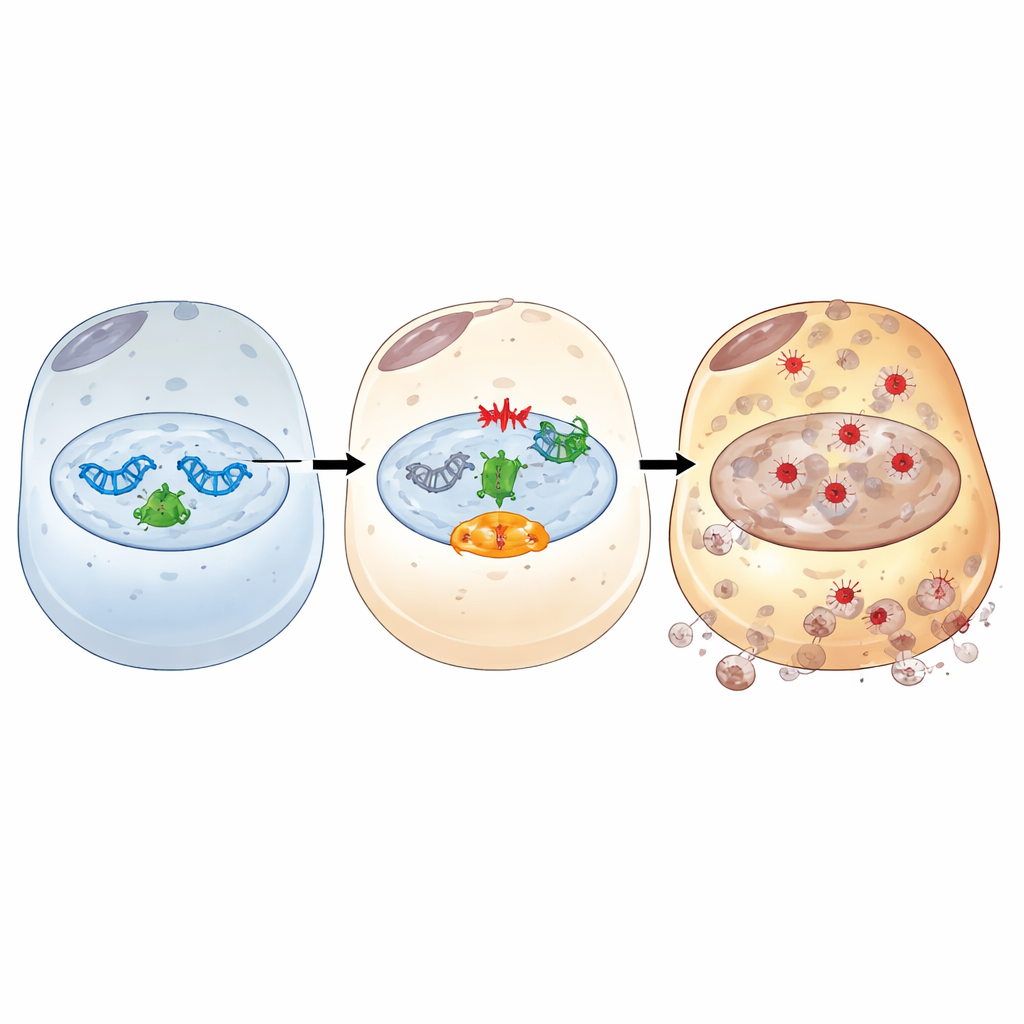
Neue Hoffnung zum Schutz geschädigter Nieren
Zusammen positionieren diese Befunde IFI16/p204 als zentrales Hub, das DNA-Schäden in Nierentubuluszellen in eine Welle eisengetriebener Zerstörung verwandelt. Anstatt die DNA-Reparaturmechanismen breit zu unterdrücken – was die Nierenfunktion verschlechtern kann – schlägt die Studie eine präzisere Strategie vor: das Abmildern des übermäßigen, IFI16-vermittelten Arms der Schadensantwort, der Zellen von Überleben zu Tod kippen lässt. Praktisch könnten Therapien, die die IFI16-Aktivität reduzieren, ihre Interaktion mit PARP-1 blockieren oder ihre Fähigkeit stören, beschädigte DNA zu binden, den Einschlag des akuten Nierenversagens abschwächen und sowohl Ferroptose als auch andere verwobene Todeswege begrenzen. Während solche Behandlungen noch entwickelt und am Menschen getestet werden müssen, zeichnet diese Arbeit eine klare molekulare Roadmap für gezielte nierenschützende Medikamente.
Zitation: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Schlüsselwörter: akutes Nierenversagen, Ferroptose, DNA-Schadensantwort, Nierentubuluszellen, IFI16