Clear Sky Science · nl
IFI16 is essentieel voor het koppelen van DNA-schade aan ferroptose bij acute nierletsels
Waarom nierstress en celdood ertoe doen
Acute nierinsufficiëntie is een plotseling verlies van nierfunctie dat vaak voorkomt bij ziekenhuispatiënten na grotere operaties, infecties of een lage bloeddruk. Het is veelvoorkomend, gevaarlijk en wordt momenteel vooral behandeld met ondersteunende maatregelen zoals vochttoediening en dialyse in plaats van gerichte geneesmiddelen. Deze studie onthult een eerder verborgen keten van gebeurtenissen in nier tubuluscellen die schade aan hun DNA koppelt aan een nieuwere vorm van ijzer-aangedreven celdood, ferroptose. Door één enkele ‘schakel’-molecule te identificeren, suggereert het werk nieuwe manieren om de nieren te beschermen wanneer de bloedtoevoer wordt onderbroken en daarna hersteld, zoals gebeurt bij veel medische noodsituaties.
Een verborgen trigger binnen niercellen
De onderzoekers richtten zich op de cellen die de kleine buisjes van de nier bekleden, die bijzonder kwetsbaar zijn wanneer de bloed- en zuurstoftoevoer wordt onderbroken en vervolgens weer op gang komt, een proces dat ischemie/reperfusie wordt genoemd. Zij concentreerden zich op een eiwit genaamd IFI16 (en het muizen-equivalent p204), dat normaal helpt bij het waarnemen van vreemd of beschadigd DNA en bij het beslissen of cellen moeten herstellen, ontsteken of zelfvernietigen. Bij het onderzoeken van nierbiopten van patiënten met acute tubulaire necrose, een ernstige vorm van acute nierinsufficiëntie, vonden zij veel hogere niveaus van IFI16 in tubuluscellen vergeleken met gezonde nieren, en de hoeveelheid IFI16 correleerde met bloedmarkers van verminderde nierfunctie. Bij muizen die aan nier-ischemie/reperfusie werden blootgesteld, nam het muizen-eiwit p204 in de loop van de tijd sterk toe, vooral in de kernen van proximale tubuluscellen, het segment dat het meest door schade wordt getroffen. 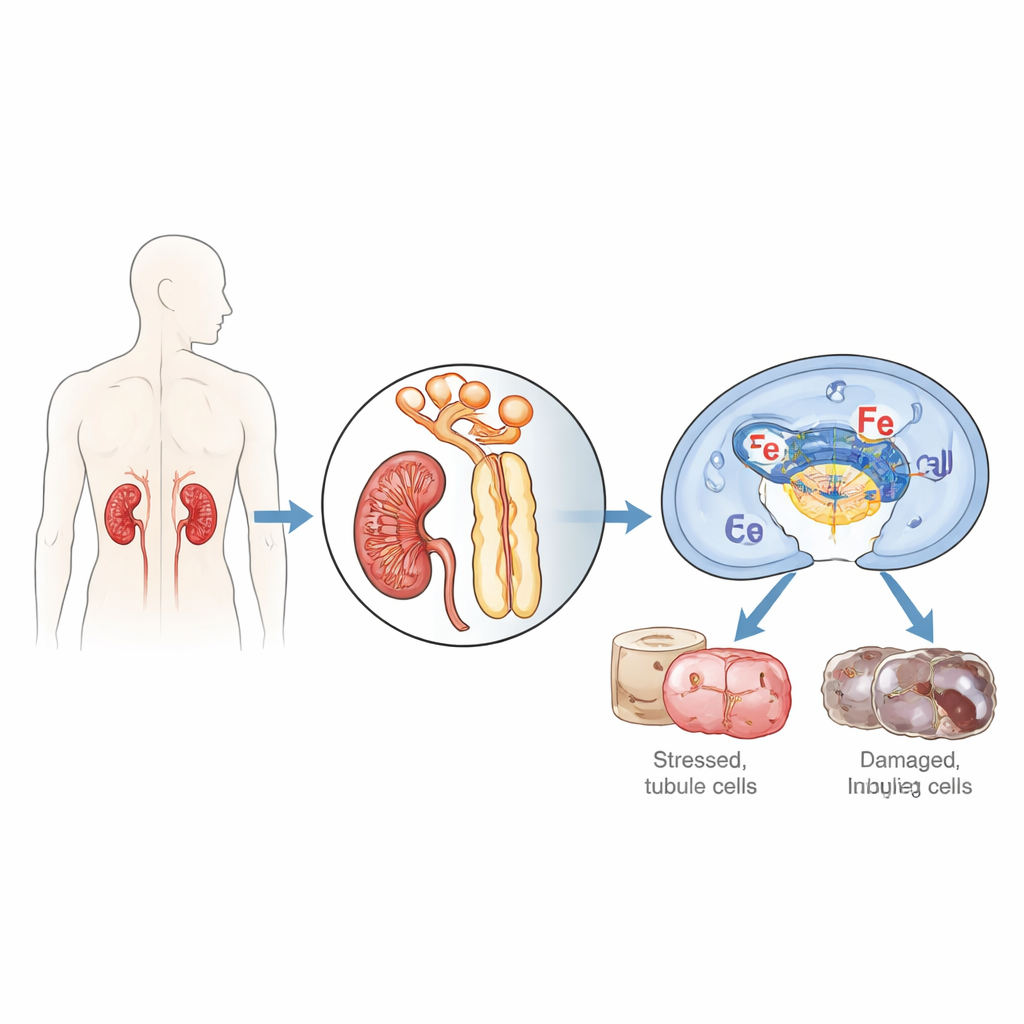
Het uitschakelen van p204 verzacht nierschade
Om te testen of dit eiwit de nieren actief schaadt of slechts een omstander is, maakten de onderzoekers muizen wiens tubuluscellen specifiek geen p204 meer hadden. Deze dieren waren verder gezond, maar wanneer hun nieren aan ischemie/reperfusie werden blootgesteld, deden ze het veel beter dan normale muizen. Bloedtesten toonden lagere creatinine- en ureumwaarden, wat wijst op betere nierfiltratie. Onder de microscoop vertoonden hun tubuli minder structurele schade en minder stressmarkers, en er was minder invasie van ontstekingsbevorderende immuuncellen. In gekweekte humane nier tubuluscellen maakte het verwijderen van IFI16 met CRISPR-genbewerking de cellen ook weerbaarder tegen schade door zuurstoftekort gevolgd door reoxygenatie, en verminderde zowel lekkende, necrotische celdood als geprogrammeerde apoptose.
Ijzer, vetten en een destructieve vorm van celdood
Naast klassieke apoptose toonden de auteurs aan dat IFI16 en p204 sterk bijdragen aan ferroptose, een vorm van celdood aangedreven door ijzer en de oxidatieve schade aan vetten in celmembranen. In beschadigde muizennieren verminderde het ontbreken van p204 chemische sporen van lipidebeschadiging, zoals 4-hydroxynonenal en malondialdehyde, en verlaagde het de niveaus van ACSL4, een enzym dat kwetsbare vetzuren in membranen betrekt. In humane tubuluscellen verlaagde het uitzetten van IFI16 de ophoping van lipidenperoxiden, versterkte beschermende antioxiderende systemen (inclusief het glutathionpad en het enzym GPX4) en herstelde het evenwicht tussen gereduceerd en geoxideerd glutathion. Het beperkt ook de toename van vrij ijzer in cellen door de instandhouding van ijzeropslag-eiwitten en door het helpen van een metaalsensorfactor om naar de kern te migreren. Toen de onderzoekers geneesmiddelen gebruikten om verschillende celdoodroutes te blokkeren, had remming van ferroptose het sterkste effect bij het redden van cellen die te veel IFI16 uitdrukten, wat ferroptose benadrukt als de belangrijkste destructieve route die door dit eiwit wordt aangedreven.
Een moleculaire keten van DNA-schade naar ferroptose
Dieper gravend bracht de studie in kaart hoe IFI16 fungeert als een schakel tussen beschadigd DNA en ferroptose. Na ischemie/reperfusie-achtige stress bindt IFI16 zich aan PARP-1, een belangrijke eerste responder op DNA-breuken, en verhoogt het diens activiteit. Dit overactiviseert een DNA-schade-signaleringsroute gecentreerd rond de ATM-kinase en het bekende bewaker-eiwit p53. Via deze as versterkt IFI16 signalen die cellulaire energiedragers uitputten, de ijzerbeschikbaarheid vergroten, antioxidantverdedigingen verzwakken en oxidatieve membraanschade bevorderen. Chemische remmers van PARP-1 of ATM doorbraken deze schadelijke keten: ze herstelden antioxidant- en ijzerbufferende eiwitten, verminderden ijzer en lipideperoxidatie en beperkten celdood, zelfs wanneer IFI16-niveaus hoog waren. Structurele experimenten toonden verder aan dat zowel de DNA-bindende HIN-domeinen als het eiwit-interacterende PYRIN-domein van IFI16 nodig zijn om PARP-1 te betrekken, de DNA-schaderespons te versterken en ferroptose te stimuleren. 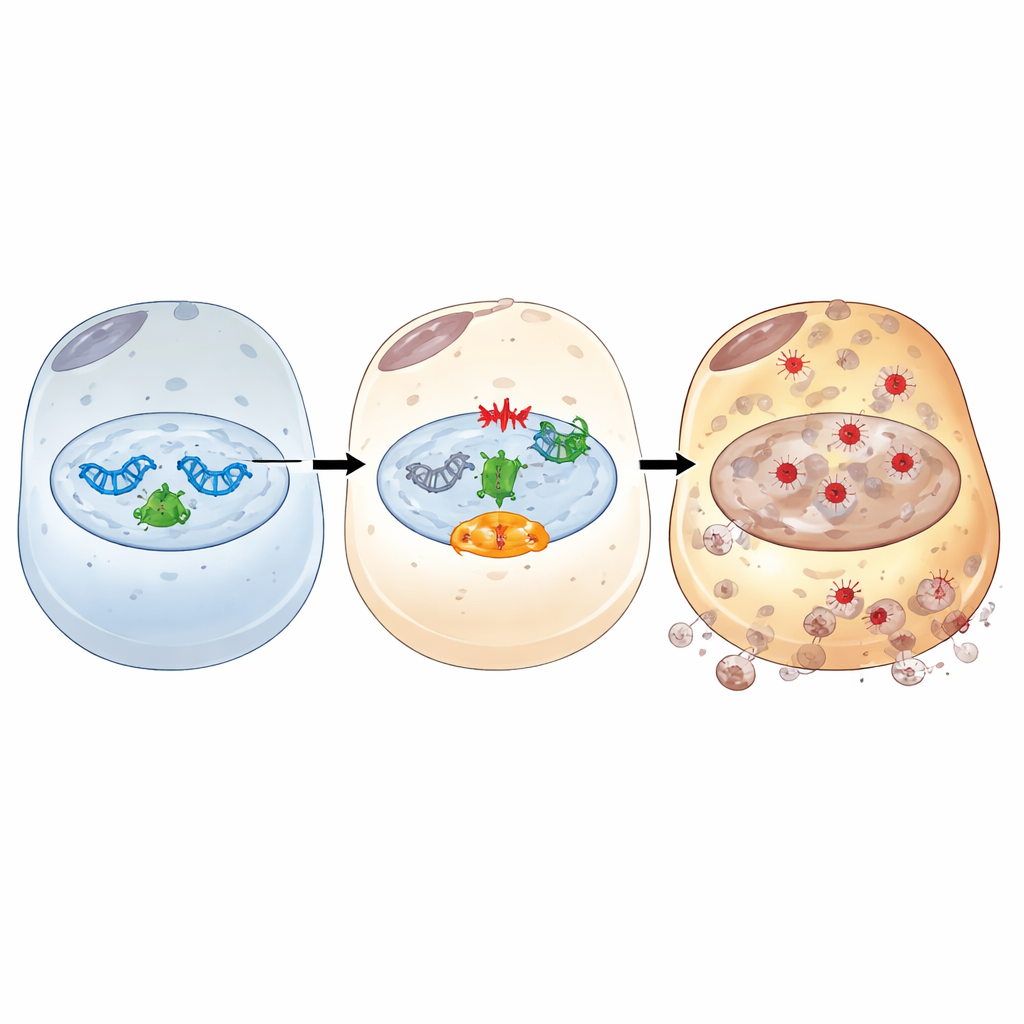
Nieuwe hoop voor het beschermen van beschadigde nieren
Samen positioneren deze bevindingen IFI16/p204 als een centraal knooppunt dat DNA-schade in nier tubuluscellen omzet in een golf van ijzeraangedreven vernietiging. In plaats van de DNA-herstelmachinerie breed te remmen — wat de nieruitkomst juist kan verslechteren — suggereert de studie een preciezere strategie: het temperen van de overmatige, IFI16-gedreven arm van de schaderespons die cellen van overleving naar dood doet kantelen. In praktische termen zouden therapieën die IFI16-activiteit verminderen, de interactie met PARP-1 blokkeren of het vermogen om beschadigd DNA te binden verstoren, de klap van acute nierinsufficiëntie kunnen verzachten en ferroptose evenals andere verweven celdoodroutes kunnen beperken. Hoewel dergelijke behandelingen nog ontwikkeld en bij mensen getest moeten worden, schetst dit werk een duidelijk moleculair routekaart naar gerichte nierbeschermende geneesmiddelen.
Bronvermelding: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Trefwoorden: acute nierinsufficiëntie, ferroptose, DNA-schaderespons, nier tubuluscellen, IFI16