Clear Sky Science · ru
IFI16 имеет ключевое значение для связывания повреждения ДНК и ферроптоза при острой почечной недостаточности
Почему стресс почек и гибель клеток важны
Острая почечная недостаточность — это внезапная потеря функции почек, которая часто возникает у госпитализированных пациентов после крупных операций, инфекций или низкого артериального давления. Она распространена, опасна и в настоящее время лечится в основном поддерживающими мерами, такими как вливания и диализ, а не целевыми лекарствами. В этом исследовании раскрыта ранее неизвестная цепочка событий внутри эпителиальных клеток почечных канальцев, связывающая повреждение их ДНК с новым типом железозависимой гибели клеток — ферроптозом. Указав на одну «переключающую» молекулу, работа предлагает новые подходы к защите почек при нарушении и восстановлении кровотока, как это происходит при многих неотложных медицинских состояниях.
Скрытый триггер внутри клеток почки
Исследователи сосредоточились на клетках, выстилающих небольшие канальцы почки, которые особенно уязвимы при прерывании и восстановлении кровоснабжения и кислородопоступления — процессе, известном как ишемия/реперфузия. Они обратили внимание на белок IFI16 (и его мышиный аналог p204), который обычно помогает клеткам распознавать чужеродную или повреждённую ДНК и решать, ремонтировать её, запускать воспаление или программную гибель. При изучении биопсий почек пациентов с острой тубулярной некрозой, тяжёлой формой острой почечной недостаточности, они обнаружили значительно повышенный уровень IFI16 в клетках канальцев по сравнению со здоровыми почками, причём количество IFI16 коррелировало с кровяными маркерами нарушенной функции почек. У мышей, подвергнутых ишемии/реперфузии почек, уровень p204 резко повышался с течением времени, особенно в ядрах клеток проксимальных канальцев — сегмента, подвергающегося наибольшему повреждению. 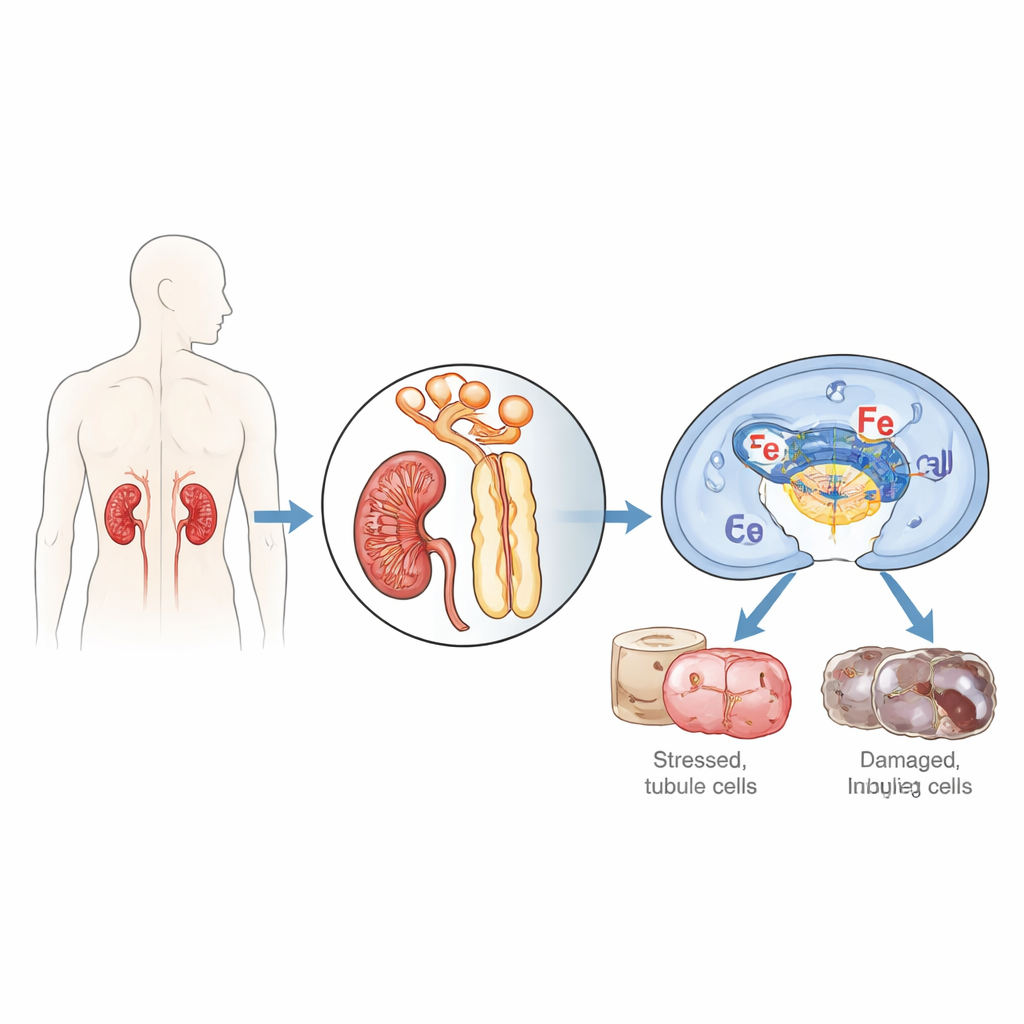
Отключение p204 ослабляет повреждение почек
Чтобы проверить, активно ли этот белок вредит почке или является лишь сопутствующим явлением, группа получила мышей с избирательным отсутствием p204 в клетках канальцев. Эти животные в остальном были здоровы, но при воздействии ишемии/реперфузии их почки переносили стресс намного лучше, чем у контрольных мышей. Анализы крови показали более низкие уровни креатинина и мочевины, что указывает на лучшую фильтрационную функцию почек. Под микроскопом канальцы имели меньше структурных повреждений и меньше маркеров стресса, а также меньшую инвазию воспалительных иммунных клеток. В культурах человеческих клеток канальцев удаление IFI16 с помощью редактирования CRISPR также сделало клетки более устойчивыми к повреждению от гипоксии с последующей реоксигенацией, сократив как некротическую утечку, так и программируемую апоптозную гибель.
Железо, жиры и разрушительный тип гибели клеток
Кроме классической апоптоза авторы показали, что IFI16 и p204 мощно стимулируют ферроптоз — форму гибели клеток, питаемую железом и окислительным повреждением липидов мембран. В повреждённых почках мышей отсутствие p204 снижало химические следы липидного окисления, такие как 4-гидроксиноненаль и малоновый диальдегид, и уменьшало уровни ACSL4 — фермента, который загружает уязвимые жирные кислоты в мембраны. В человеческих клетках канальцев нокаут IFI16 снижал накопление липидных перекисей, усиливал защитные антиоксидантные системы (включая путь глутатиона и фермент GPX4) и восстанавливал соотношение восстановленной и окисленной форм глутатиона. Он также ограничивал всплеск свободного железа в клетках, сохраняя белки, запасающие железо, и помогая металлочувствительному фактору переместиться в ядро. При применении препаратов, блокирующих различные пути гибели, ингибирование ферроптоза давало наибольший эффект по спасению клеток с переэкспрессией IFI16, что подчёркивает ферроптоз как главный путь разрушения, опосредуемый этим белком.
Молекулярная цепочка от повреждения ДНК к ферроптозу
Углублённый анализ показал, как IFI16 функционирует как ретранслятор между повреждённой ДНК и ферроптозом. После стресса, похожего на ишемию/реперфузию, IFI16 связывается с PARP-1 — ключевым первичным ответчиком на разрывы ДНК — и усиливает его активность. Это гиперактивирует сигнальный путь ответа на повреждение ДНК, центром которого является киназа ATM и знаменитый белок-сторож p53. Через эту ось IFI16 усиливает сигналы, которые истощают клеточные энергозапасы, увеличивают доступность железа, ослабляют антиоксидантную защиту и способствуют окислительному повреждению мембран. Химические ингибиторы PARP-1 или ATM разрывали эту вредоносную цепь: они восстанавливали антиоксидантные и буферные белки для железа, снижали уровни свободного железа и перекисное окисление липидов и уменьшали гибель клеток, даже при высоких уровнях IFI16. Структурные эксперименты дополнительно показали, что и ДНК-связывающие домены HIN, и домен PYRIN, взаимодействующий с белками, у IFI16 необходимы для взаимодействия с PARP-1, усиления ответа на повреждение ДНК и индукции ферроптоза. 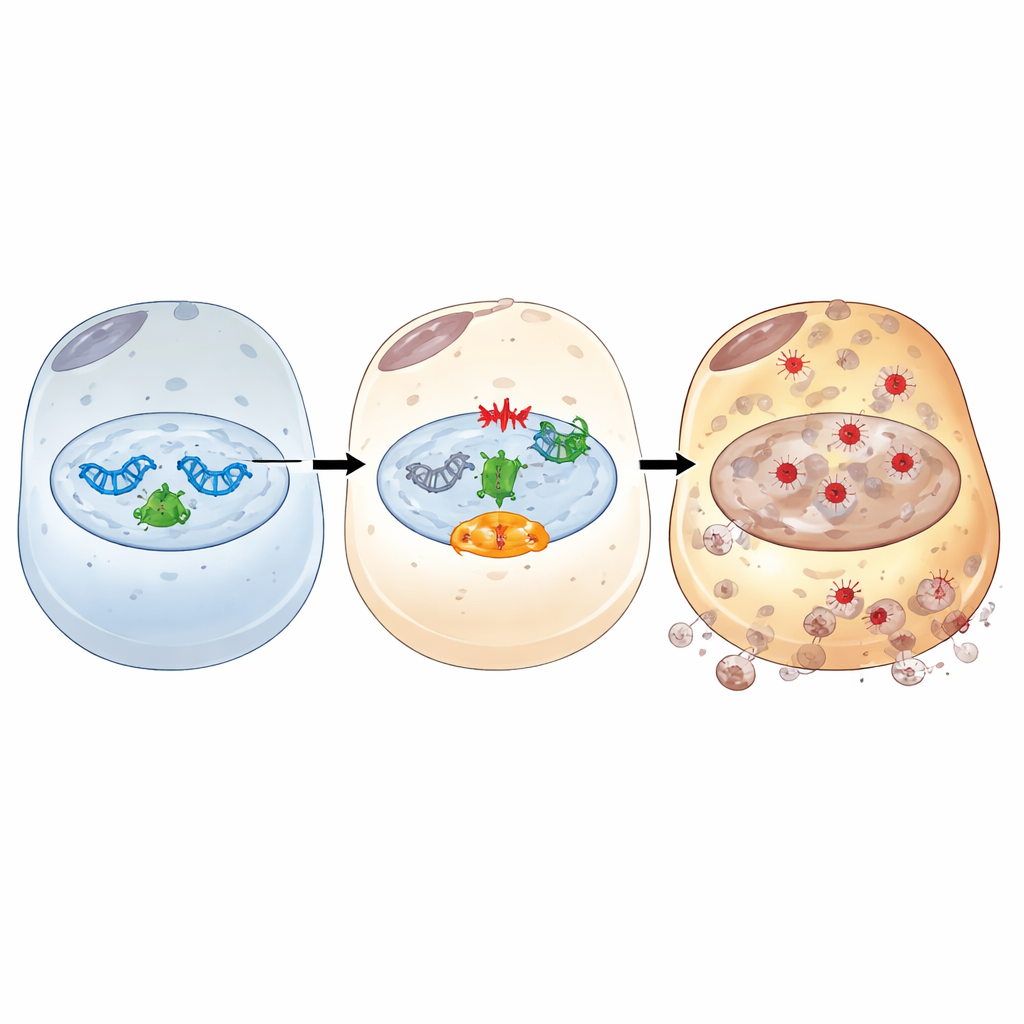
Новая надежда на защиту повреждённых почек
Вместе эти результаты выводят IFI16/p204 как центральный узел, переводящий повреждение ДНК в клетках канальцев почки в волну железозависимого разрушения. Вместо широкого подавления механизмов репарации ДНК — что может усугубить исходы для почек — исследование предлагает более точный подход: ослабление чрезмерной, управляемой IFI16 ветви ответов на повреждение, которая сдвигает клетки с выживания к гибели. На практике терапевтические стратегии, уменьшающие активность IFI16, блокирующие его взаимодействие с PARP-1 или нарушающие способность связываться с повреждённой ДНК, могли бы смягчить последствия острой почечной недостаточности, ограничивая ферроптоз и другие взаимосвязанные пути гибели. Хотя такие препараты ещё предстоит разработать и испытать на людях, эта работа прокладывает ясную молекулярную дорожную карту к целенаправленным почечно-защитным лекарствам.
Цитирование: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Ключевые слова: острое повреждение почек, ферроптоз, ответ на повреждение ДНК, клетки канальцев почки, IFI16