Clear Sky Science · it
IFI16 è essenziale per collegare il danno al DNA e la ferroptosi nell’insufficienza renale acuta
Perché lo stress renale e la morte cellulare sono importanti
L’insufficienza renale acuta è una perdita improvvisa della funzione renale che colpisce spesso persone ricoverate dopo interventi chirurgici importanti, infezioni o ipotensione. È comune, pericolosa e attualmente trattata principalmente con misure di supporto come i liquidi e la dialisi piuttosto che con farmaci mirati. Questo studio scopre una catena di eventi finora nascosta all’interno delle cellule dei tubuli renali che collega il danno al loro DNA a una forma più recente di morte cellulare guidata dal ferro chiamata ferroptosi. Identificando una singola molecola “interruttore”, il lavoro suggerisce nuovi modi per proteggere i reni quando il flusso sanguigno viene interrotto e poi ripristinato, come avviene in molte emergenze mediche.
Un innesco nascosto all’interno delle cellule renali
I ricercatori si sono concentrati sulle cellule che rivestono i microscopici tubuli del rene, particolarmente vulnerabili quando l’afflusso di sangue e ossigeno è interrotto e poi riavviato, un processo noto come ischemia/riperfusione. Hanno focalizzato l’attenzione su una proteina chiamata IFI16 (e il suo omologo murino p204), che normalmente aiuta le cellule a riconoscere DNA estraneo o danneggiato e decidere se riparare, infiammare o autodistruggersi. Esaminando biopsie renali di pazienti con necrosi tubulare acuta, una forma grave di insufficienza renale acuta, hanno riscontrato livelli molto più elevati di IFI16 nelle cellule dei tubuli rispetto a reni sani, e la quantità di IFI16 correla con i marker ematici di cattiva funzione renale. Nei topi sottoposti a ischemia/riperfusione renale, la versione murina p204 è aumentata nel tempo, specialmente nei nuclei delle cellule del tubulo prossimale, il segmento più colpito dal danno. 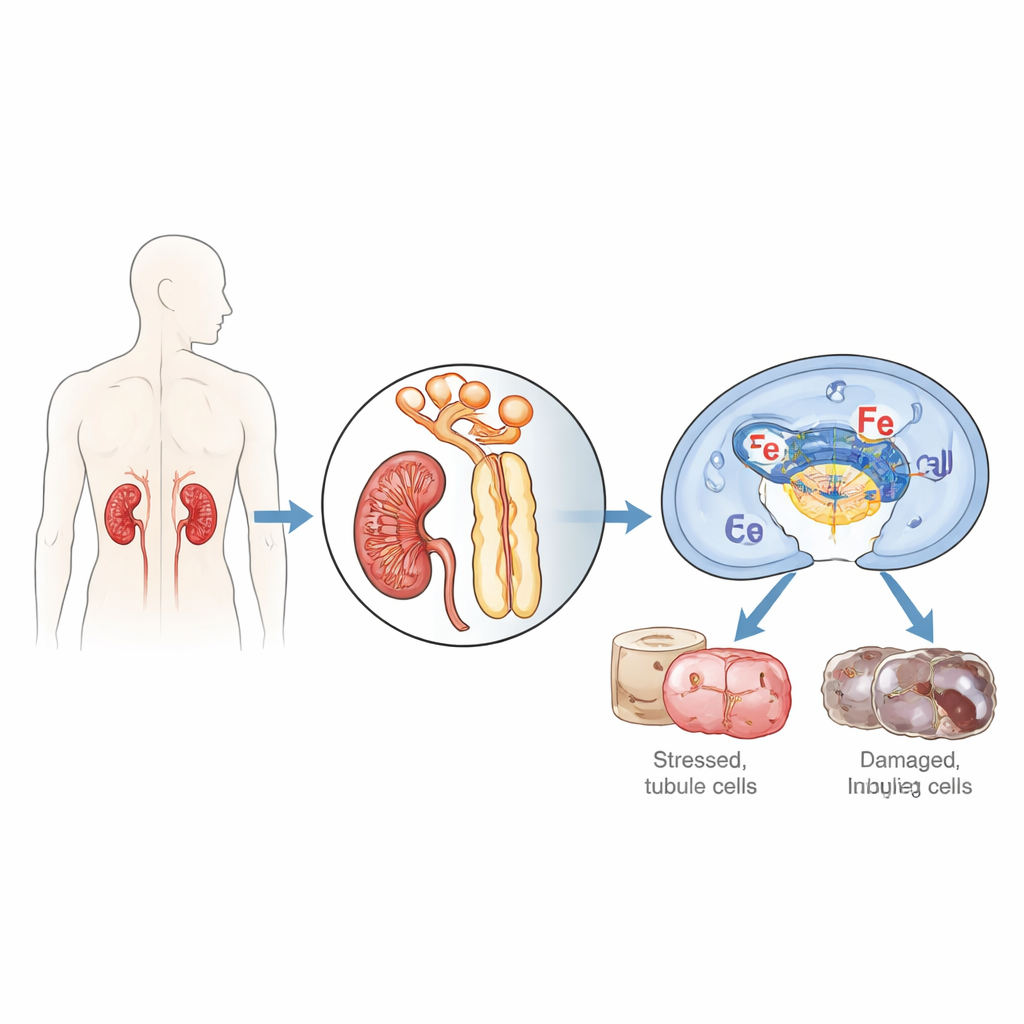
Spegnere p204 attenua il danno renale
Per verificare se questa proteina danneggiasse attivamente il rene o fosse solo una spettatrice, il team ha ingegnerizzato topi i cui tubuli mancavano specificamente di p204. Questi animali erano per il resto sani, ma quando i loro reni sono stati esposti a ischemia/riperfusione, si sono comportati molto meglio rispetto ai topi normali. Gli esami del sangue hanno mostrato creatinina e urea più basse, indicando una migliore filtrazione renale. Al microscopio, i loro tubuli presentavano minori danni strutturali e meno marcatori di stress, e si è osservata una ridotta invasione di cellule immunitarie infiammatorie. In colture di cellule del tubulo renale umano, l’eliminazione di IFI16 mediante editing genetico CRISPR ha reso anch’essa le cellule più resistenti al danno da bassa ossigenazione seguito da riossigenazione, riducendo sia la morte necrotica con perdita di membrana sia l’apoptosi programmata.
Ferro, lipidi e una forma distruttiva di morte cellulare
Oltre all’apoptosi classica, gli autori hanno dimostrato che IFI16 e p204 favoriscono fortemente la ferroptosi, una forma di morte cellulare alimentata dal ferro e dal danno ossidativo ai lipidi delle membrane. Nei reni murini danneggiati, la perdita di p204 ha ridotto le tracce chimiche del danno lipidico, come 4-idrossinonenale e malondialdeide, e ha attenuato i livelli di ACSL4, un enzima che incorpora acidi grassi vulnerabili nelle membrane. Nelle cellule dei tubuli umani, il knockout di IFI16 ha ridotto l’accumulo di perossidi lipidici, potenziato i sistemi antiossidanti protettivi (inclusa la via del glutatione e l’enzima GPX4) e ripristinato l’equilibrio tra glutatione ridotto e ossidato. Ha anche limitato l’aumento di ferro libero all’interno delle cellule preservando le proteine di stoccaggio del ferro e favorendo il transito di un fattore sensibile al metallo nel nucleo. Quando i ricercatori hanno usato farmaci per bloccare diverse vie di morte, l’inibizione della ferroptosi ha avuto l’effetto più marcato nel salvare le cellule con sovraespressione di IFI16, evidenziando la ferroptosi come la principale via di distruzione indotta da questa proteina.
Una catena molecolare dal danno al DNA alla ferroptosi
Approfondendo, lo studio ha mappato come IFI16 agisca da relè tra il DNA danneggiato e la ferroptosi. Dopo uno stress simile all’ischemia/riperfusione, IFI16 si lega a PARP-1, un primo risponditore chiave alle rotture del DNA, e ne potenzia l’attività. Questo iperattiva una via di segnalazione del danno al DNA centrata sulla chinasi ATM e sulla nota proteina guardiana p53. Attraverso questo asse, IFI16 amplifica segnali che esauriscono i vettori energetici cellulari, aumentano la disponibilità di ferro, indeboliscono le difese antiossidanti e favoriscono il danno ossidativo alle membrane. Blocchi chimici di PARP-1 o ATM interrompono questa catena dannosa: ripristinano proteine antiossidanti e di buffer del ferro, riducono ferro e perossidazione lipidica e attenuano la morte cellulare, anche quando i livelli di IFI16 sono elevati. Esperimenti strutturali hanno inoltre rivelato che sia i domini HIN leganti il DNA sia il dominio PYRIN di interazione proteica di IFI16 sono necessari per impegnare PARP-1, potenziare la risposta al danno del DNA e guidare la ferroptosi. 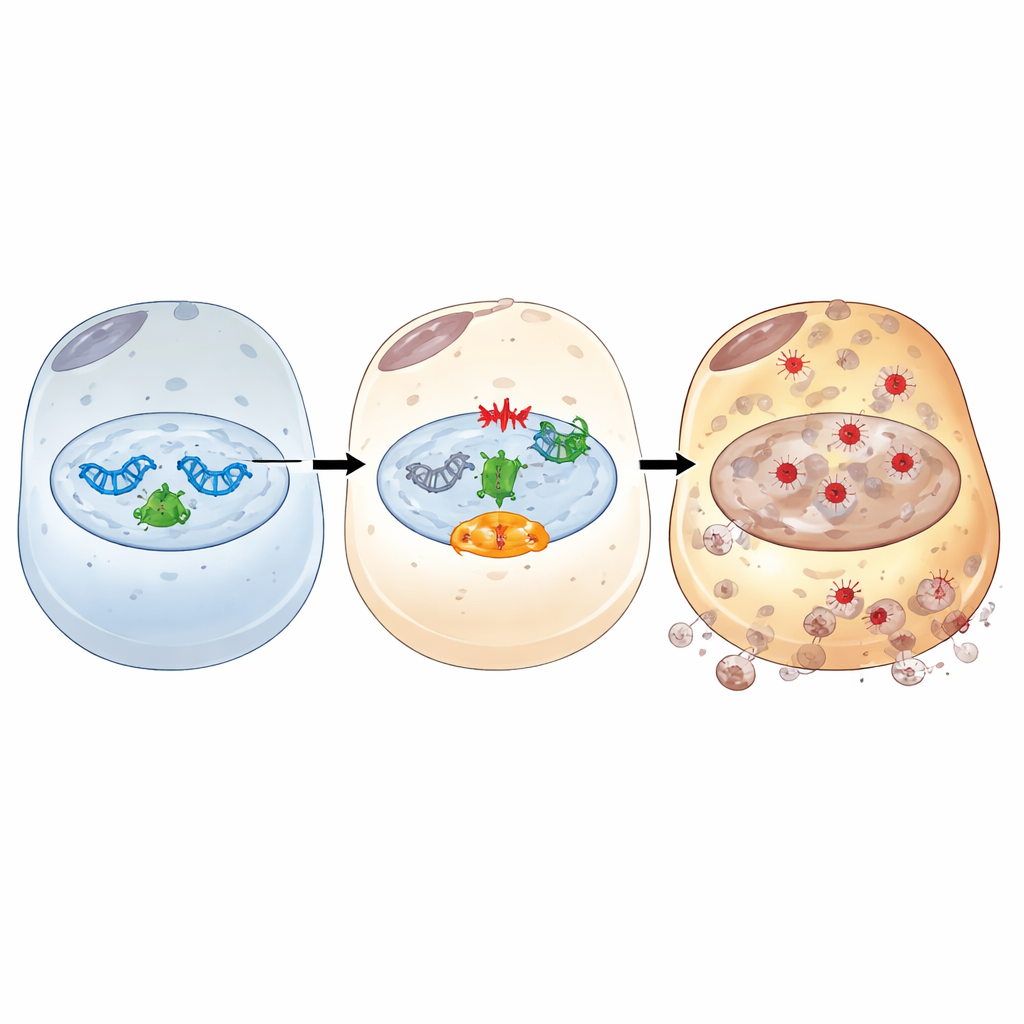
Nuova speranza per proteggere i reni danneggiati
Nel loro insieme, questi risultati pongono IFI16/p204 come un hub centrale che trasforma il danno al DNA nelle cellule dei tubuli renali in un’ondata di distruzione alimentata dal ferro. Piuttosto che sopprimere in modo ampio la macchina di riparazione del DNA—cosa che può peggiorare gli esiti renali—lo studio suggerisce una strategia più precisa: attenuare il braccio eccessivo guidato da IFI16 della risposta al danno che spinge le cellule dalla sopravvivenza verso la morte. In termini pratici, terapie che riducano l’attività di IFI16, blocchino la sua interazione con PARP-1 o interrompano la sua capacità di legare il DNA danneggiato potrebbero attenuare l’impatto dell’insufficienza renale acuta, limitando la ferroptosi oltre ad altre vie di morte interconnesse. Sebbene tali trattamenti debbano ancora essere sviluppati e testati sull’uomo, questo lavoro traccia una chiara mappa molecolare verso farmaci mirati per la protezione renale.
Citazione: Qiao, Z., Zhou, D., Zhang, T. et al. IFI16 is essential to linking DNA damage and ferroptosis in acute kidney injury. Cell Death Dis 17, 350 (2026). https://doi.org/10.1038/s41419-026-08604-5
Parole chiave: insufficienza renale acuta, ferroptosi, risposta al danno del DNA, cellule dei tubuli renali, IFI16