Clear Sky Science · tr
Bir Drosophila RasV12DlgRNAi modelinde SHMT’nin tümör baskılayıcı işlevi: DNA hasarı ve PLP ile sinerjistik gen–besin etkileşimi
Bu meyve sineği öyküsü neden önemli
Kanser sıklıkla hücrelerin besinleri kullanma şeklini yeniden düzenler, ancak tümörleri besleyen aynı moleküller bazen onları sınırlayabilir. Bu çalışmada araştırmacılar, hücre içinde vitaminle bağlantılı kimyayı yöneten tek bir enzimin kanser üzerinde fren görevi görebileceğini ortaya koymak için meyve sineklerini kullandılar. Enzim zayıfladığında DNA’nın kararsızlaştığını, tümörlerin daha agresif büyüdüğünü ve yaygın bir vitamin ile bir antioksidanın tümör büyümesi ile hücre ölümü arasındaki dengeyi değiştirebileceğini gösteriyorlar.
Hücrenin küçük karbon trafiği merkezi
Hücrelerimizin içinde, tek karbon metabolizması olarak bilinen bir ağ, DNA üretimine ve gen aktivitesini kontrol eden kimyasal etiketlere yapı taşları sağlayarak sessizce yaşamı destekler. Bu ağın merkezinde, aktif B6 vitamini ile birlikte çalışan SHMT adlı bir enzim bulunur. SHMT, bir aminoasidi başka birine dönüştürürken DNA yapmak için gereken küçük karbon birimlerini aktarır. Birçok insan kanserinde bu enzimin versiyonları yüksek seviyelerde bulunur ve tümörlerin büyümesine yardım ettiği düşünülür. Ancak bazı kanserlerde SHMT’nin bir formunun düşük seviyeleri daha kötü sonuçlarla ilişkilidir; bu da enzimin bağlama bağlı olarak tümör baskılayıcı olarak da hareket edebileceğine işaret eder.
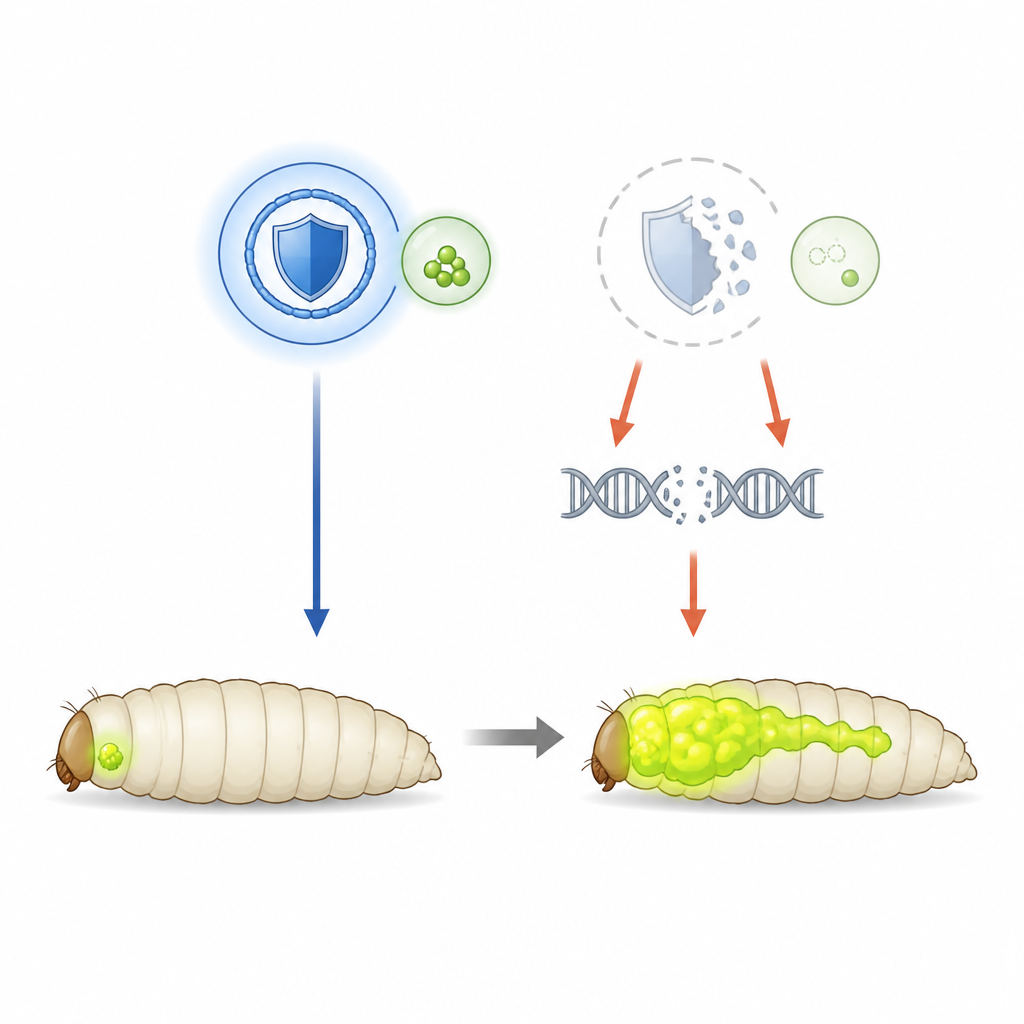
Tümörlerin büyümesini izlemek için meyve sinekleri kullanmak
SHMT’nin koruyucu rolünü çözümlemek için ekip, aşırı aktif bir Ras geni ve bir hücre kutupluluk geninin kaybı tarafından yönlendirilen agresif göz tümörleri geliştirecek şekilde mühendislik yapılmış meyve sineklerine yöneldi. Bu tümörler yeşil parlıyor, bu sayede bilim insanları larvadaki boyutlarını ve yayılımlarını izleyebiliyor. Bu ortamda SHMT seviyeleri normaldir, bu nedenle araştırmacılar RNA interferansı kullanarak enzimi kasıtlı olarak azaltabildiler. SHMT aktivitesi azaldığında, primer tümörler daha büyük büyüdü ve sineğin sinir sistemine daha sık invaze etti; bu da burada SHMT’nin yakıt olmasındansa kanser ilerlemesini frenleyen bir rol oynadığını gösterdi.
DNA yapı taşları, hasar ve oksidatif stres
SHMT normalde timidilat üretimini sağlayan bir yol besler; bu, DNA için gerekli bir yapı taşıdır. SHMT susturulduğunda bu yapı taşının arzı aksadı. Sonuç, DNA çift sarmal kırılmalarında artış ve tümör hücreleri içinde görünür şekilde parçalanmış kromozomlar oldu; bunlar genom kararsızlığının açık işaretleridir. Bu hücreler ayrıca DNA’ya zarar veren X-ışınlarına ve DNA kopyalanmasını yavaşlatan ilaçlara alışılmadık derecede hassaslaştı ve bir kez kırılma oluştuğunda onarmakta zorlandılar. Aynı zamanda reaktif oksijen türlerinin, oksijen içeren zararlı moleküllerin düzeyleri keskin şekilde yükseldi. Larvalara timidilat verilmesi DNA yapı taşlarını geri getirdi ve hem DNA hasarını hem de oksidatif stresi azalttı; antioksidan N-asetil sistein ise reaktif oksijen türlerini, kromozom hasarını ve tümör büyümesini azalttı. Birlikte, bu bulgular zayıf DNA yapı taşı arzunun oksidatif stresi artırdığı, bunun da DNA’ya saldırıp tümörlerin ilerlemesine yardımcı olduğu bir olay zincirine işaret ediyor.
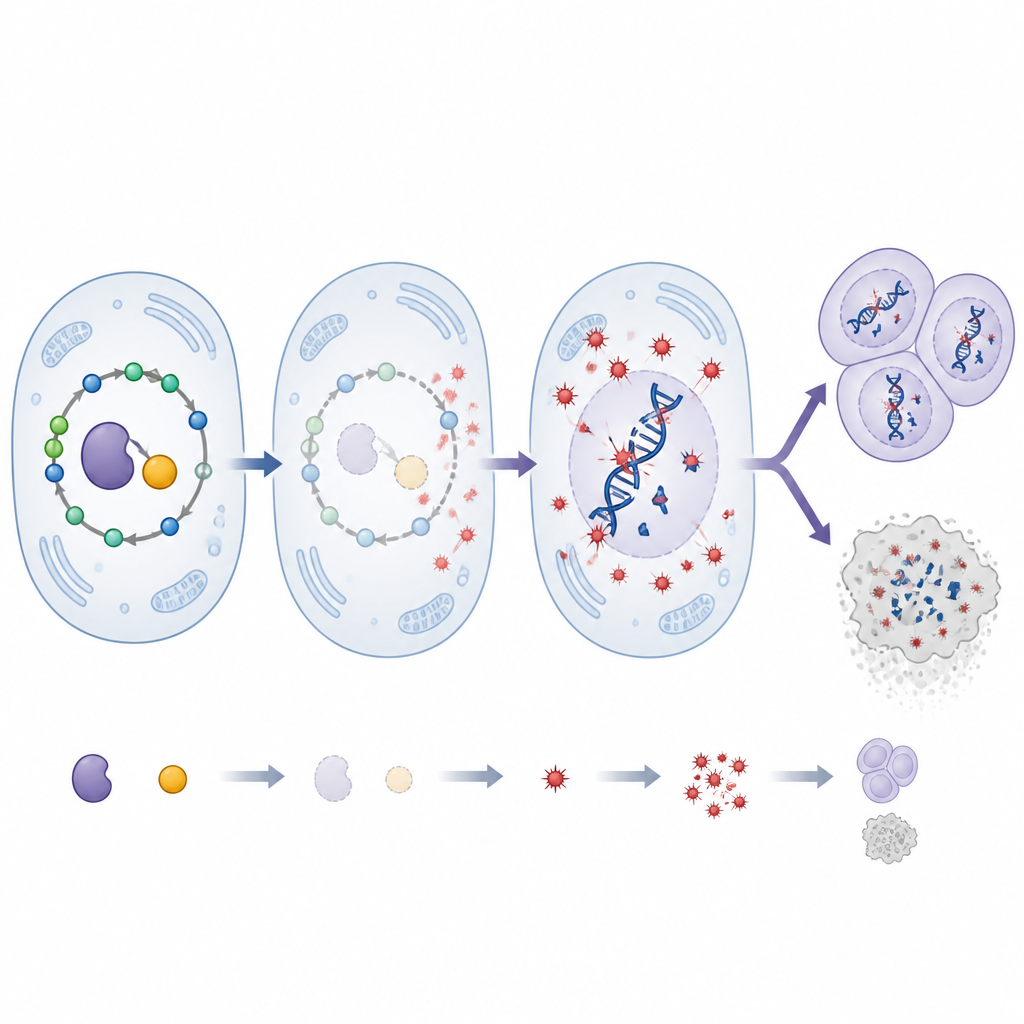
Bir vitamin kofaktörü dengeyi değiştiriyor
SHMT’nin işlevi, B6 vitamininin aktif formu olan piridoksal 5’-fosfata bağlıdır. Araştırmacılar besinsel bir engelleyici kullanarak bu vitamini sineklerde azalttılar ve bunun azalmış SHMT ile nasıl etkileştiğini sordular. Yalnızca SHMT’yi kesmek tümör büyümesini hızlandırdı ve DNA hasarını artırdı. Yalnızca B6 vitamini azaltmak daha hafif etkilere yol açtı. Çarpıcı şekilde, her iki değişikliğin birleşmesi oksidatif stres ve DNA kırılmalarında dramatik bir artışa neden oldu; bu artış her bir etkiden çok daha yüksekti. Ancak bu orantılı olarak daha büyük tümörler üretmedi. Bunun yerine birçok tümör hücresi önemli bir hücre ölümü enzimini etkinleştirdi ve apoptoza girdi; bu, aşırı hasarlı hücrelerin elimine edildiğini düşündürüyor. Yüksek doz antioksidan tedavi yeniden oksidatif stresi, DNA hasarını ve tümör boyutunu azalttı ve reaktif oksijen türlerinin bu sonuçları yönlendirmedeki merkezi rolünü vurguladı.
Kanser ve diyet için bunun anlamı
Bu çalışma, canlı bir hayvanda SHMT’nin DNA kararlılığını sürdürerek ve oksidatif stresi kontrol altında tutarak tümör baskılayıcı olarak hareket edebileceğini gösteriyor. SHMT aktivitesi düştüğünde, özellikle B6 vitamini azaldığında, tümör hücreleri ilerlemeyi destekleyebilecek DNA hasarı biriktirir veya çok ileri giderse kendi ölümünü tetikleyebilir. Çalışma ayrıca SHMT ile B6 vitamini arasında tümör büyümesini şekillendiren doğrudan bir gen–besin etkileşimini açığa çıkarıyor. Bu bulgular meyve sineklerinden elde edilmiş olsa da bazı insan kanserlerinde görülen desenlerle örtüşüyor ve SHMT’yi, onun vitamin kofaktörünü ve reaktif oksijen türlerini birlikte hedeflemenin, bölünen hücreleri öldürmeye tek başına dayanmak yerine tümör büyümesini kontrol etme stratejilerine ışık tutabileceğini öne sürüyor.
Atıf: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Anahtar kelimeler: kanser metabolizması, DNA hasarı, reaktif oksijen türleri, B6 vitamini, Drosophila tümörleri