Clear Sky Science · pl
Funkcja supresora nowotworu SHMT w modelu Drosophila RasV12DlgRNAi: uszkodzenia DNA i synergistyczna interakcja gen‑substancja odżywcza z PLP
Dlaczego ta historia z muszką owocową ma znaczenie
Nowotwory często przeprogramowują sposób, w jaki komórki wykorzystują składniki odżywcze, ale te same związki, które napędzają guzy, czasem mogą je też hamować. W tym badaniu naukowcy wykorzystali muszki owocowe, aby odkryć, jak pojedynczy enzym odpowiadający za reakcje związane z witaminami w komórce może działać jak hamulec dla raka. Pokazują, że gdy ten enzym zawodzi, DNA staje się niestabilne, guzy rosną agresywniej, a powszechna witamina i przeciwutleniacz mogą przesunąć równowagę między wzrostem guza a śmiercią komórek.
Małe węzły węgla w komórce
W naszych komórkach sieć zwana metabolizmem jednego węgla dyskretnie wspiera życie, dostarczając składniki do syntezy DNA i chemiczne znaczniki regulujące aktywność genów. W centrum tej sieci znajduje się enzym zwany SHMT, który współdziała z aktywną formą witaminy B6. SHMT pomaga przekształcać jeden aminokwas w inny, przekazując jednocześnie małe jednostki węglowe niezbędne do produkcji DNA. W wielu ludzkich nowotworach poziomy tego enzymu są podwyższone i przypisuje się im wspieranie wzrostu guzów. Jednak w niektórych nowotworach niskie poziomy jednej formy SHMT wiążą się z gorszym rokowaniem, co sugeruje, że enzym może też pełnić funkcję supresora nowotworu, zależnie od kontekstu.
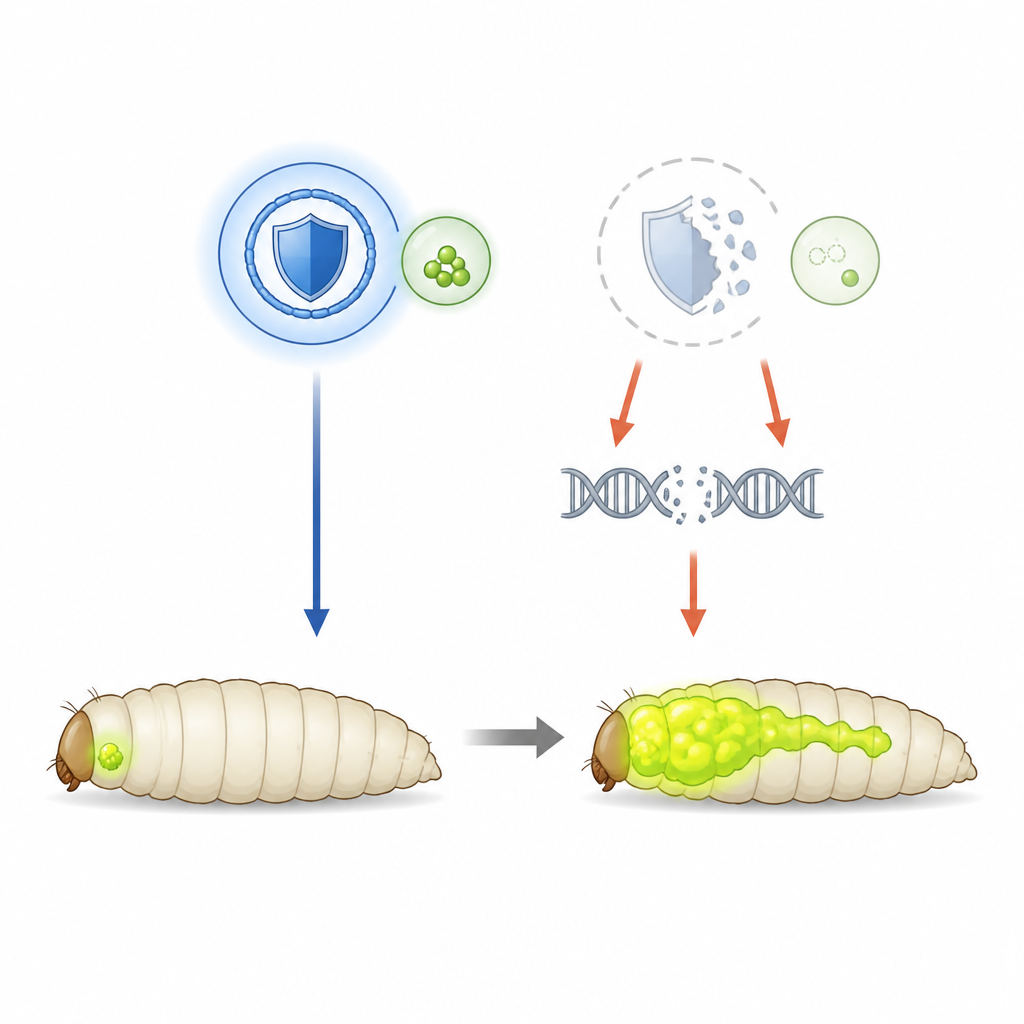
Obserwowanie wzrostu guzów w muszkach
Aby rozplątać ochronną rolę SHMT, zespół zwrócił się do muszek owocowych zaprojektowanych tak, by rozwijały agresywne guzy oka napędzane nadaktywnym genem Ras i utratą genu odpowiedzialnego za polaryzację komórkową. Te guzy świecą na zielono, co pozwala naukowcom śledzić ich rozmiar i rozsiew w larwie. W tym układzie poziomy SHMT są normalne, więc badacze mogli celowo obniżyć aktywność enzymu za pomocą interferencji RNA. Gdy aktywność SHMT została zmniejszona, guzy pierwotne stały się większe i częściej naciekały układ nerwowy muszki, co dowodzi, że w tym kontekście SHMT działa jako hamulec postępu raka, a nie jako jego paliwo.
Składniki budulcowe DNA, uszkodzenia i stres oksydacyjny
SHMT normalnie zasila szlak prowadzący do produkcji tymidylanów — niezbędnych składników budulcowych DNA. Po wyciszeniu SHMT zaopatrzenie w ten składnik osłabło. W efekcie nastąpił wzrost podwójnych pęknięć DNA i widocznych rozdrobnionych chromosomów w komórkach nowotworowych, co jest wyraźnym sygnałem niestabilności genomu. Komórki te stały się też wyjątkowo wrażliwe na uszkodzenia DNA wywoływane promieniowaniem rentgenowskim i na leki spowalniające replikację DNA, oraz miały trudności z naprawą pęknięć. Równocześnie poziomy reaktywnych form tlenu — szkodliwych cząsteczek zawierających tlen — gwałtownie wzrosły. Leczenie larw tymidylanem przywróciło składniki budulcowe DNA i obniżyło zarówno uszkodzenia DNA, jak i stres oksydacyjny, podczas gdy przeciwutleniacz N‑acetylocysteina zmniejszył poziom reaktywnych form tlenu, uszkodzenia chromosomów i wzrost guza. Razem wyniki te wskazują na łańcuch zdarzeń, w którym niedobór składników budulcowych DNA zwiększa stres oksydacyjny, który następnie atakuje DNA i sprzyja postępowi guza.
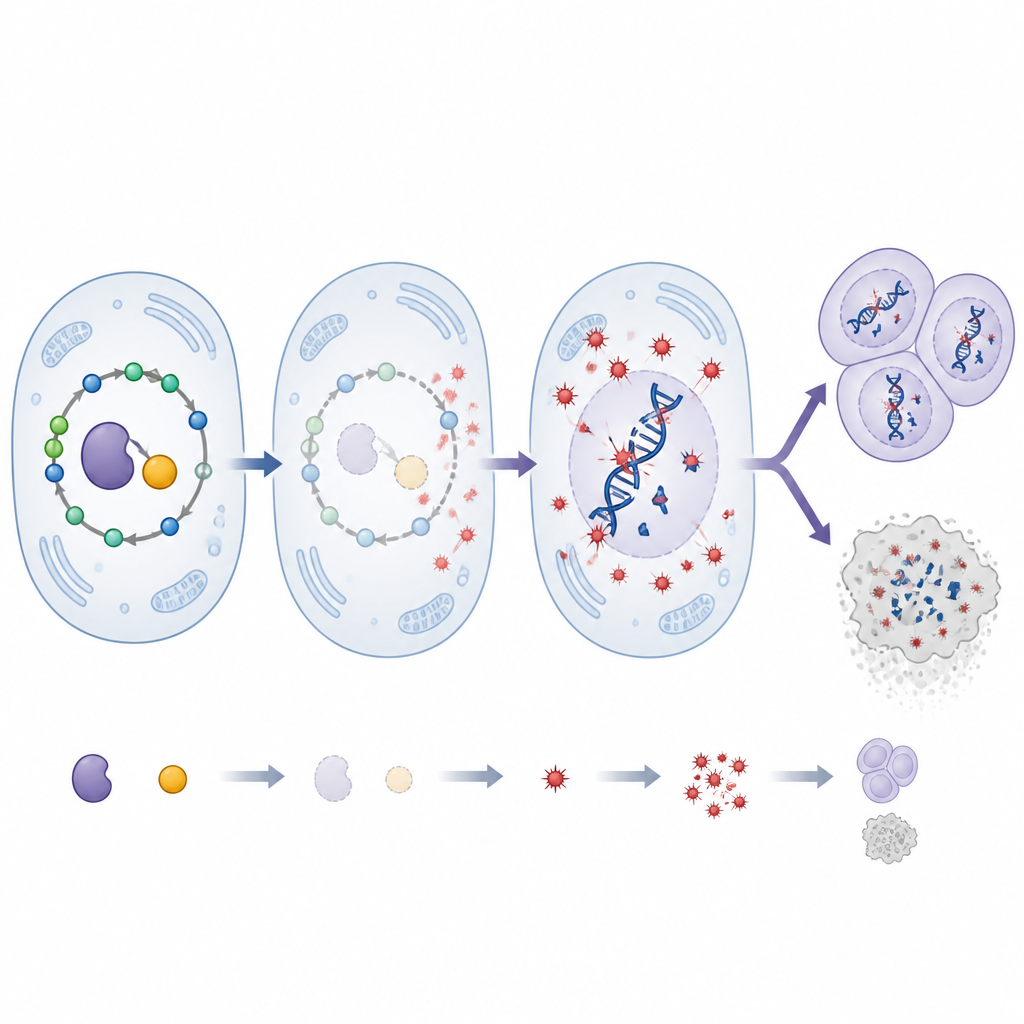
Koenzym witaminowy przechyla szalę
SHMT wymaga pirydoksal‑5′‑fosforanu, aktywnej formy witaminy B6, aby funkcjonować. Badacze obniżyli poziom tej witaminy u much za pomocą dietetycznego inhibitora i sprawdzili, jak to współdziała z redukcją SHMT. Samo obniżenie SHMT przyspieszyło wzrost guza i zwiększyło uszkodzenia DNA. Obniżenie witaminy B6 samo w sobie miało łagodniejsze skutki. Co istotne, połączenie obu zmian wywołało dramatyczny wzrost stresu oksydacyjnego i pęknięć DNA, znacznie większy niż każde z tych zaburzeń osobno. Jednak nie przełożyło się to proporcjonalnie na większe guzy. Zamiast tego wiele komórek nowotworowych włączyło kluczowy enzym śmierci komórkowej i uległo apoptozie, co sugeruje, że silnie uszkodzone komórki były eliminowane. Leczenie wysoką dawką przeciwutleniacza ponownie zmniejszyło stres oksydacyjny, uszkodzenia DNA i rozmiar guza, podkreślając centralną rolę reaktywnych form tlenu w kształtowaniu tych efektów.
Co to znaczy dla raka i diety
Praca ta pokazuje, że in vivo SHMT może działać jako supresor nowotworu, pomagając utrzymać stabilność DNA i kontrolować stres oksydacyjny. Gdy aktywność SHMT spada, szczególnie w połączeniu z niedoborem witaminy B6, komórki nowotworowe gromadzą uszkodzenia DNA, które mogą albo napędzać progresję raka, albo — jeśli są zbyt rozległe — doprowadzić do ich samozniszczenia. Badanie ujawnia też bezpośrednią interakcję gen‑substancja odżywcza między SHMT a witaminą B6, która kształtuje sposób wzrostu guzów. Chociaż wyniki pochodzą z muszek owocowych, odzwierciedlają wzorce obserwowane w niektórych ludzkich nowotworach i sugerują, że jednoczesne ukierunkowanie SHMT, jego koenzymu witaminowego i reaktywnych form tlenu mogłoby w przyszłości pomóc kontrolować wzrost guzów bez polegania wyłącznie na zabijaniu dzielących się komórek.
Cytowanie: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Słowa kluczowe: metabolizm nowotworów, uszkodzenia DNA, reaktywne formy tlenu, witamina B6, nowotwory Drosophila