Clear Sky Science · it
Funzione oncosoppressiva di SHMT in un modello Drosophila RasV12DlgRNAi: danno al DNA e interazione genico-nutriente sinergica con PLP
Perché questa storia della mosca della frutta è importante
Il cancro spesso riorganizza il modo in cui le cellule usano i nutrienti, ma le stesse molecole che alimentano i tumori a volte possono anche frenarli. In questo studio, i ricercatori hanno usato Drosophila per scoprire come un singolo enzima che gestisce la chimica legata alle vitamine nelle cellule possa funzionare come freno al cancro. Mostrano che quando questo enzima viene compromesso, il DNA diventa instabile, i tumori crescono in modo più aggressivo e una comune vitamina insieme a un antiossidante possono spostare l’equilibrio tra crescita tumorale e morte cellulare.
Il piccolo snodo del carbonio nella cellula
All’interno delle nostre cellule, una rete nota come metabolismo a un carbonio sostiene silenziosamente la vita fornendo mattoni per la produzione del DNA e marcatori chimici che controllano l’attività genica. Al centro di questa rete si trova un enzima chiamato SHMT, che lavora insieme alla forma attiva della vitamina B6. SHMT aiuta a convertire un amminoacido in un altro trasferendo unità carboniose necessarie per fabbricare il DNA. In molti tumori umani, versioni di questo enzima sono presenti a livelli elevati e si ritiene che favoriscano la crescita tumorale. Tuttavia, in alcuni tumori bassi livelli di una forma di SHMT sono associati a prognosi peggiori, suggerendo che l’enzima può anche funzionare come oncosoppressore, a seconda del contesto.
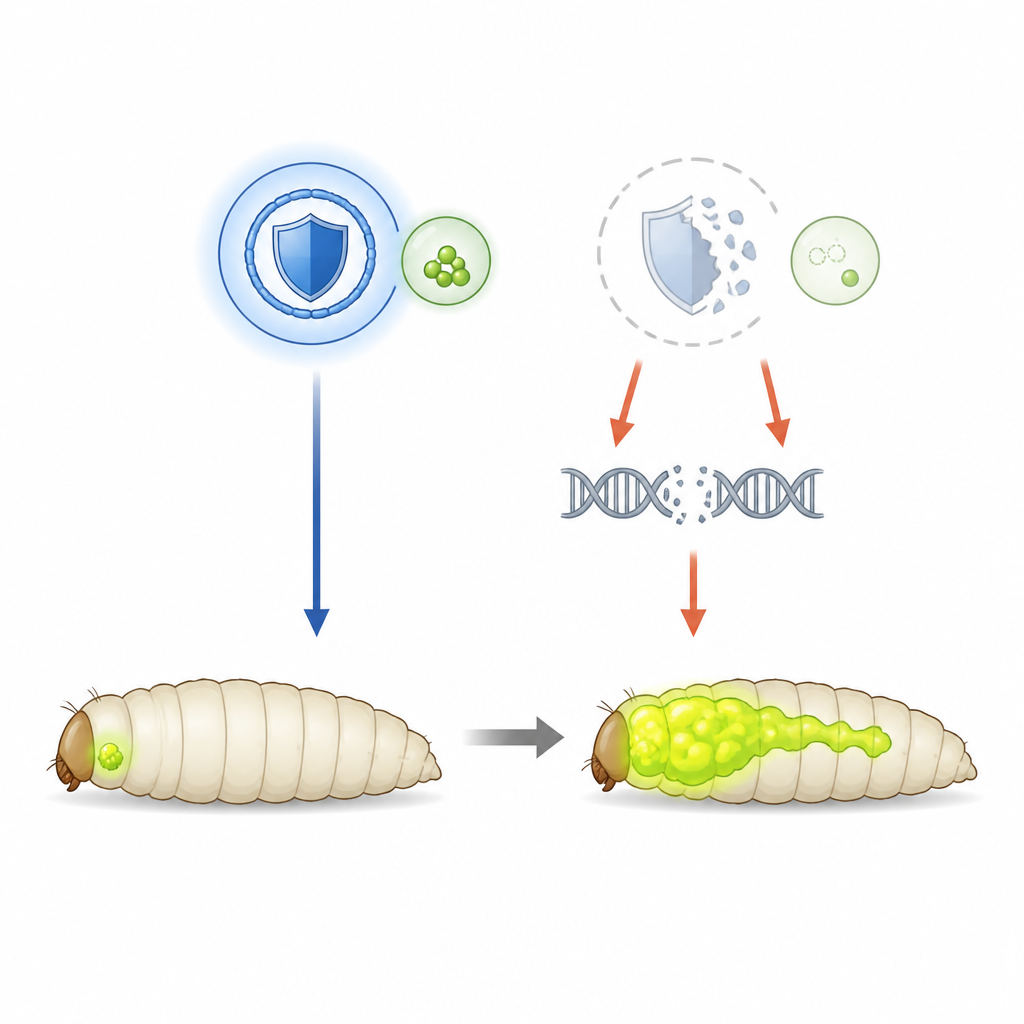
Usare la mosca della frutta per osservare la crescita tumorale
Per districare il ruolo protettivo di SHMT, il gruppo ha scelto mosche della frutta ingegnerizzate per sviluppare tumori oculari aggressivi guidati da un gene Ras iperattivo e dalla perdita di un gene di polarità cellulare. Questi tumori brillano di verde, permettendo agli scienziati di monitorarne dimensione e diffusione nelle larve. In questo contesto, i livelli di SHMT sono normali, così i ricercatori hanno potuto ridurre deliberatamente l’enzima tramite interferenza a RNA. Quando l’attività di SHMT è stata ridotta, i tumori primari sono cresciuti di più e hanno invaso il sistema nervoso della mosca più frequentemente, mostrando che, in questo modello, SHMT agisce come freno alla progressione tumorale piuttosto che come carburante.
Mattoni del DNA, danno e stress ossidativo
SHMT alimenta normalmente una via che produce timidilato, un mattoncino essenziale del DNA. Quando SHMT è stato spento, la fornitura di questo componente è venuta meno. Il risultato è stato un aumento di rotture a doppio filamento del DNA e cromosomi visibilmente frammentati nelle cellule tumorali, chiari segnali di instabilità del genoma. Queste cellule sono risultate anche insolitamente sensibili ai raggi X che danneggiano il DNA e a farmaci che rallentano la replicazione, e hanno faticato a riparare le rotture una volta verificatesi. Contemporaneamente, i livelli di specie reattive dell’ossigeno, molecole contenenti ossigeno dannose, sono aumentati notevolmente. Trattare le larve con timidilato ha ripristinato i mattoni del DNA e ridotto sia il danno al DNA sia lo stress ossidativo, mentre un antiossidante, la N-acetilcisteina, ha diminuito le specie reattive, i danni cromosomici e la crescita tumorale. Nel complesso, questi risultati indicano una catena di eventi in cui una cattiva fornitura di mattoni del DNA aumenta lo stress ossidativo, che a sua volta attacca il DNA e favorisce l’avanzamento tumorale.
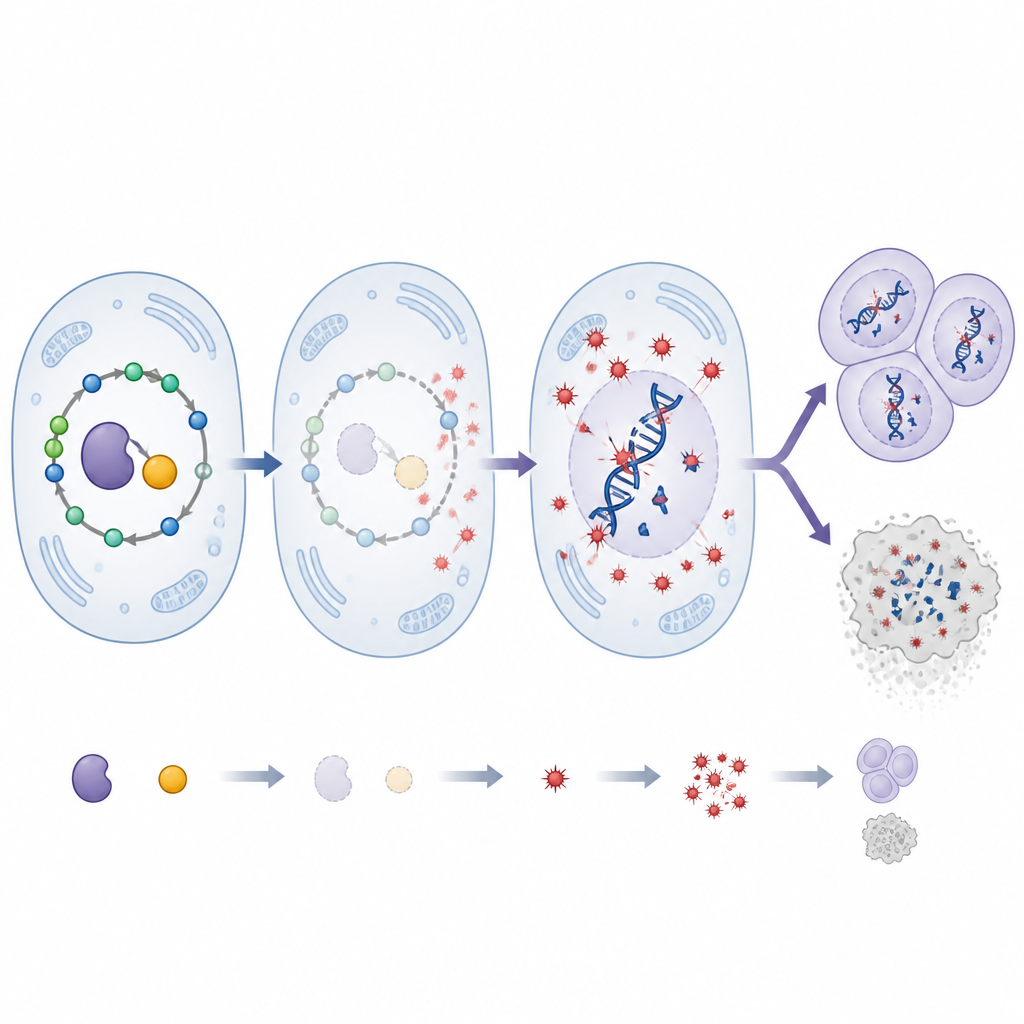
Un cofattore vitaminico che cambia l’equilibrio
SHMT dipende dal piridossal 5’-fosfato, la forma attiva della vitamina B6, per funzionare. I ricercatori hanno ridotto questa vitamina nelle mosche usando un bloccante dietetico e hanno valutato come interagisse con la riduzione di SHMT. Tagliare solo SHMT ha accelerato la crescita tumorale e aumentato il danno al DNA. Ridurre soltanto la vitamina B6 ha avuto effetti più lievi. Colpendo entrambe le componenti, però, si è verificato un picco drammatico di stress ossidativo e di rotture del DNA, molto maggiore rispetto a ciascun singolo intervento. Tuttavia ciò non ha prodotto tumori proporzionalmente più grandi. Al contrario, molte cellule tumorali hanno attivato un enzima chiave della morte cellulare e sono andate in apoptosi, suggerendo che le cellule eccessivamente danneggiate venivano eliminate. Un trattamento ad alto dosaggio con antiossidanti ha nuovamente ridotto stress ossidativo, danno al DNA e dimensione tumorale, sottolineando il ruolo centrale delle specie reattive dell’ossigeno nel guidare questi risultati.
Cosa significa per cancro e dieta
Questo lavoro mostra che, in un animale vivente, SHMT può comportarsi da oncosoppressore aiutando a mantenere la stabilità del DNA e a tenere sotto controllo lo stress ossidativo. Quando l’attività di SHMT diminuisce, specialmente insieme a una riduzione della vitamina B6, le cellule tumorali accumulano danni al DNA che possono o alimentare la progressione del cancro o, se spinti oltre, innescare la loro stessa morte. Lo studio rivela anche un’interazione diretta genico–nutriente tra SHMT e la vitamina B6 che modula la crescita tumorale. Pur provenendo da Drosophila, questi risultati riecheggiano pattern osservati in alcuni tumori umani e suggeriscono che mirare contemporaneamente a SHMT, al suo cofattore vitaminico e alle specie reattive dell’ossigeno potrebbe orientare strategie future per controllare la crescita tumorale senza fare affidamento esclusivo sull’uccisione delle cellule in divisione.
Citazione: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Parole chiave: metabolismo del cancro, danno al DNA, specie reattive dell'ossigeno, vitamina B6, tumori di Drosophila