Clear Sky Science · de
Tumor-suppressive Funktion von SHMT in einem Drosophila RasV12DlgRNAi-Modell: DNA-Schäden und synergistische Gen‑Nährstoff‑Interaktion mit PLP
Warum diese Fruchtfliegen‑Geschichte wichtig ist
Krebs verändert oft, wie Zellen Nährstoffe nutzen; doch dieselben Moleküle, die Tumoren antreiben, können sie teils auch bremsen. In dieser Studie nutzten Forschende Fruchtfliegen, um zu zeigen, wie ein einzelnes Enzym, das vitaminabhängige Reaktionen in Zellen vermittelt, als Bremsklotz gegen Krebs wirken kann. Sie demonstrieren, dass bei Versagen dieses Enzyms die DNA instabil wird, Tumoren aggressiver wachsen und ein verbreitetes Vitamin sowie ein Antioxidans das Gleichgewicht zwischen Tumorwachstum und Zelltod verschieben können.
Die winzige Kohlenstoff‑Verkehrsdrehscheibe der Zelle
Im Inneren unserer Zellen unterstützt ein Netzwerk, das als Ein‑Kohlenstoff‑Stoffwechsel bekannt ist, unauffällig das Leben, indem es Bausteine für die DNA‑Synthese und chemische Gruppen liefert, die die Genaktivität steuern. Im Zentrum dieses Netzwerks steht ein Enzym namens SHMT, das mit der aktiven Form von Vitamin B6 zusammenarbeitet. SHMT hilft, eine Aminosäure in eine andere umzuwandeln und übergibt dabei kleine Kohlenstoffeinheiten, die für die DNA‑Herstellung nötig sind. In vielen menschlichen Krebsarten liegen erhöhte Mengen dieses Enzyms vor und werden als förderlich für Tumorwachstum angesehen. In einigen Krebsformen ist jedoch ein niedriger Spiegel einer SHMT‑Form mit schlechteren Ergebnissen verknüpft, was darauf hindeutet, dass das Enzym je nach Kontext auch tumorunterdrückend wirken kann.
Fruchtfliegen nutzen, um Tumoren wachsen zu sehen
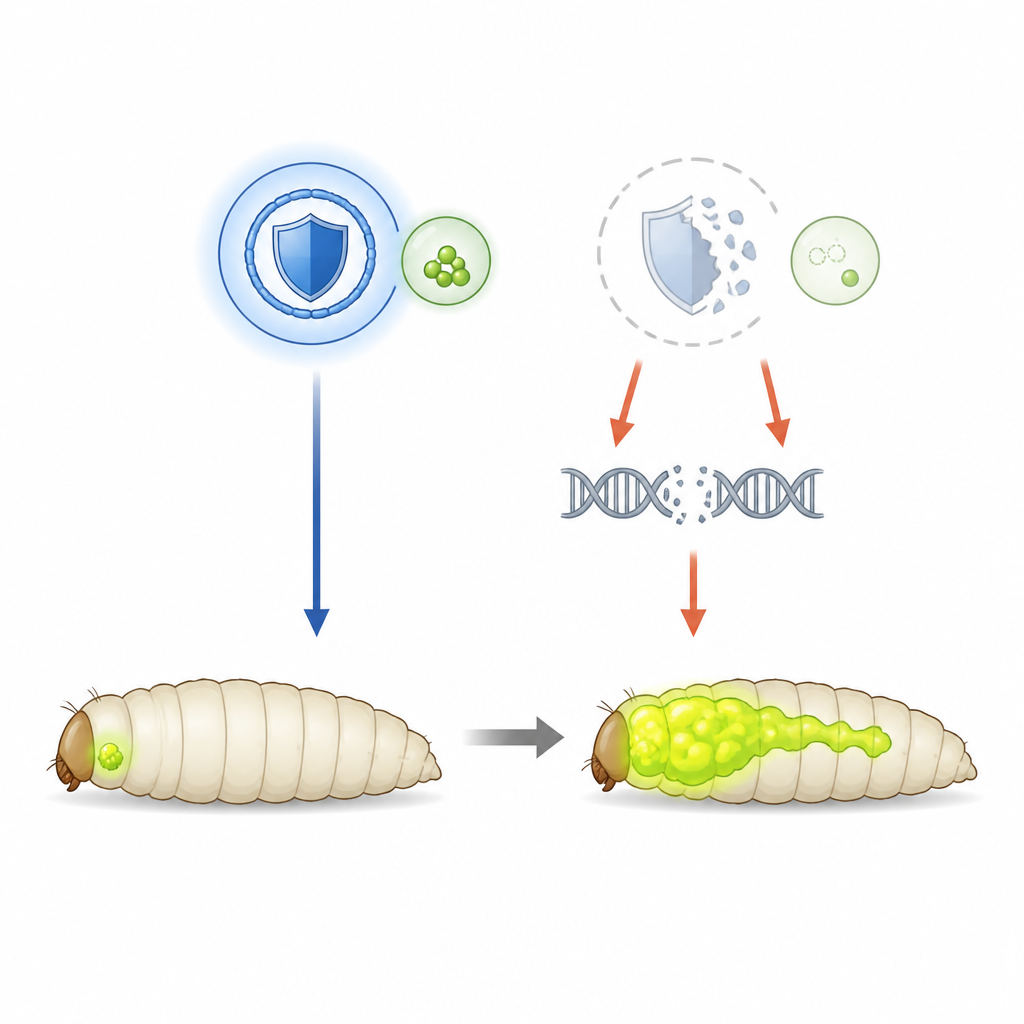
Um SHMTs schützende Rolle zu entwirren, verwendete das Team Fruchtfliegen, die so genetisch verändert waren, dass sie aggressive Augentumoren entwickeln – angetrieben durch ein überaktives Ras‑Gen und Verlust eines Zellpolaritätsgens. Diese Tumoren leuchten grün, sodass Forschende ihre Größe und Ausbreitung im Larvenstadium verfolgen konnten. In diesem Modell sind die SHMT‑Spiegel normal, weshalb die Forschenden das Enzym gezielt mittels RNA‑Interferenz herunterregeln konnten. Bei verminderter SHMT‑Aktivität wuchsen die Primärtumoren größer und drangen häufiger in das Nervensystem der Fliegen ein, was zeigt, dass hier SHMT eher als Bremse für die Krebsfortschreitung denn als Treibstoff wirkt.
DNA‑Bausteine, Schäden und oxidativer Stress
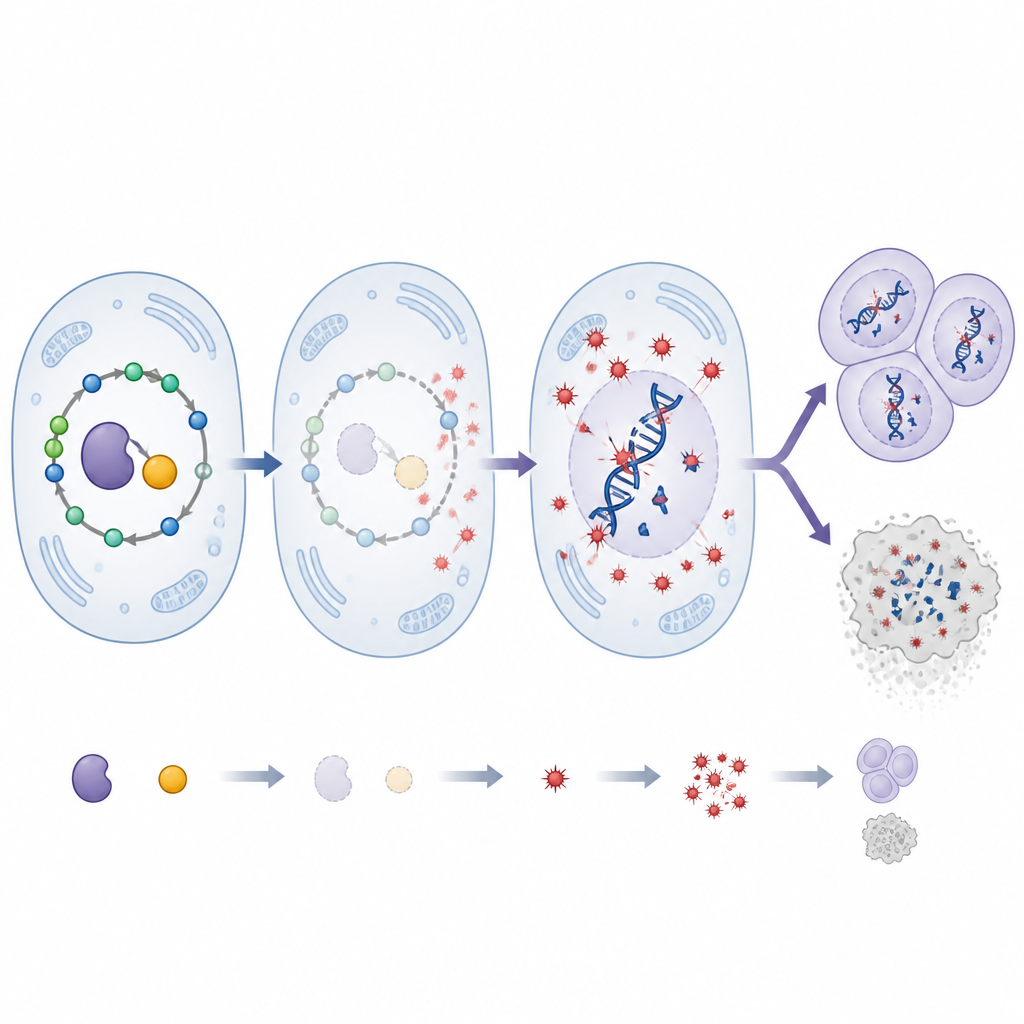
SHMT speist normalerweise einen Weg, der Thyminylat (Thymidylat) produziert, einen essenziellen Baustein der DNA. Wurde SHMT ausgeschaltet, versagte die Versorgung mit diesem Baustein. Das Ergebnis war ein Anstieg an DNA‑Doppelstrangbrüchen und sichtbar zerstörten Chromosomen in Tumorzellen – deutliche Anzeichen genomischer Instabilität. Diese Zellen wurden außerdem ungewöhnlich empfindlich gegenüber DNA‑schädigender Röntgenstrahlung und gegenüber Wirkstoffen, die die DNA‑Replikation bremsen, und sie konnten Brüche schlechter reparieren. Gleichzeitig stiegen die Werte reaktiver Sauerstoffspezies – schädlicher, sauerstoffhaltiger Moleküle – stark an. Die Behandlung der Larven mit Thyminylat stellte die DNA‑Bausteinversorgung wieder her und senkte sowohl DNA‑Schäden als auch oxidativen Stress, während das Antioxidans N‑Acetylcystein die reaktiven Sauerstoffspezies, Chromosomenschäden und das Tumorwachstum reduzierte. Zusammen deuten diese Befunde auf eine Kaskade hin, bei der eine mangelhafte Versorgung mit DNA‑Bausteinen den oxidativen Stress erhöht, der wiederum die DNA angreift und das Tumorfortschreiten fördert.
Ein Vitamin‑Kofaktor verschiebt das Gleichgewicht
SHMT ist auf Pyridoxal‑5′‑phosphat (PLP), die aktive Form von Vitamin B6, angewiesen, um zu funktionieren. Die Forschenden reduzierten dieses Vitamin in Fliegen durch einen diätetischen Blocker und untersuchten, wie es mit vermindertem SHMT interagiert. Allein die Reduktion von SHMT beschleunigte das Tumorwachstum und erhöhte DNA‑Schäden. Eine alleinige Verminderung von Vitamin B6 hatte mildere Effekte. Auffällig war, dass die Kombination beider Veränderungen zu einem dramatischen Anstieg von oxidativem Stress und DNA‑Brüchen führte, weit stärker als jeder einzelne Eingriff. Dies führte jedoch nicht zu entsprechend größeren Tumoren. Stattdessen schalteten viele Tumorzellen ein zentrales Zelltodenzym ein und durchliefen Apoptose, was darauf hindeutet, dass extrem geschädigte Zellen eliminiert wurden. Eine hochdosierte Antioxidans‑Behandlung verringerte erneut oxidativen Stress, DNA‑Schäden und Tumorgröße und unterstreicht die zentrale Rolle reaktiver Sauerstoffspezies für diese Effekte.
Was das für Krebs und Ernährung bedeutet
Die Studie zeigt, dass SHMT in einem lebenden Organismus als Tumorsuppressor wirken kann, indem es zur Stabilität der DNA beiträgt und oxidativen Stress in Schach hält. Fällt die SHMT‑Aktivität ab, insbesondere zusammen mit reduziertem Vitamin B6, häufen Tumorzellen DNA‑Schäden an, die entweder das Krebswachstum fördern oder, wenn sie zu groß werden, den Zelltod auslösen. Die Arbeit offenbart zudem eine direkte Gen–Nährstoff‑Interaktion zwischen SHMT und Vitamin B6, die das Tumorwachstum mitbestimmt. Obwohl diese Befunde aus Fruchtfliegen stammen, spiegeln sie Muster, die in einigen menschlichen Krebsarten beobachtet werden, und legen nahe, dass die gleichzeitige Beeinflussung von SHMT, seinem Vitamin‑Kofaktor und reaktiven Sauerstoffspezies künftige Strategien zur Kontrolle von Tumoren informieren könnte, ohne sich ausschließlich aufs Abtöten teilender Zellen zu stützen.
Zitation: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Schlüsselwörter: Krebsstoffwechsel, DNA‑Schäden, reaktive Sauerstoffspezies, Vitamin B6, Drosophila‑Tumoren