Clear Sky Science · ar
وظيفة كابحة للأورام لإنزيم SHMT في نموذج Drosophila RasV12DlgRNAi: تلف الحمض النووي وتفاعل جيني-مغذّي تآزري مع PLP
لماذا تهمنا هذه قصة ذبابة الفاكهة
غالبًا ما تعيد السرطانات توصيل كيفية استخدام الخلايا للمغذيات، لكن الجزيئات نفسها التي تغذي الأورام قد تكبحها أحيانًا أيضًا. في هذه الدراسة، استخدم الباحثون ذبابة الفاكهة لكشف كيف يمكن لإنزيم واحد يتعامل مع كيمياء مرتبطة بالفيتامين داخل الخلايا أن يعمل كفرامل على السرطان. يظهرون أنه عندما يضعف هذا الإنزيم، يصبح الحمض النووي غير مستقر، وتنمو الأورام بشكل أكثر عدوانية، ويمكن لفيتامين شائع ومضاد أكسدة أن يحوّل التوازن بين نمو الورم وموت الخلايا.
مركز حركة الكربون الصغير في الخلية
داخل خلايانا، يدعم شبكة تعرف باستقلاب الكربون الواحد الحياة بهدوء من خلال تزويد لبنات بناء إلى إنتاج الحمض النووي والعلامات الكيميائية التي تتحكم في نشاط الجينات. في مركز هذه الشبكة يوجد إنزيم يسمى SHMT، الذي يعمل مع فيتامين B6 في صورته النشطة. يساعد SHMT في تحويل حمض أميني إلى آخر أثناء تمرير وحدات كربون صغيرة لازمة لصنع الحمض النووي. في العديد من سرطانات الإنسان، توجد نسخ من هذا الإنزيم بمستويات عالية ويُعتقد أنها تساعد الأورام على النمو. ومع ذلك في بعض السرطانات، يرتبط انخفاض مستوى شكل واحد من SHMT بنتائج أسوأ، مما يشير إلى أن الإنزيم يمكن أن يعمل أيضًا كمثبط للورم بحسب السياق.
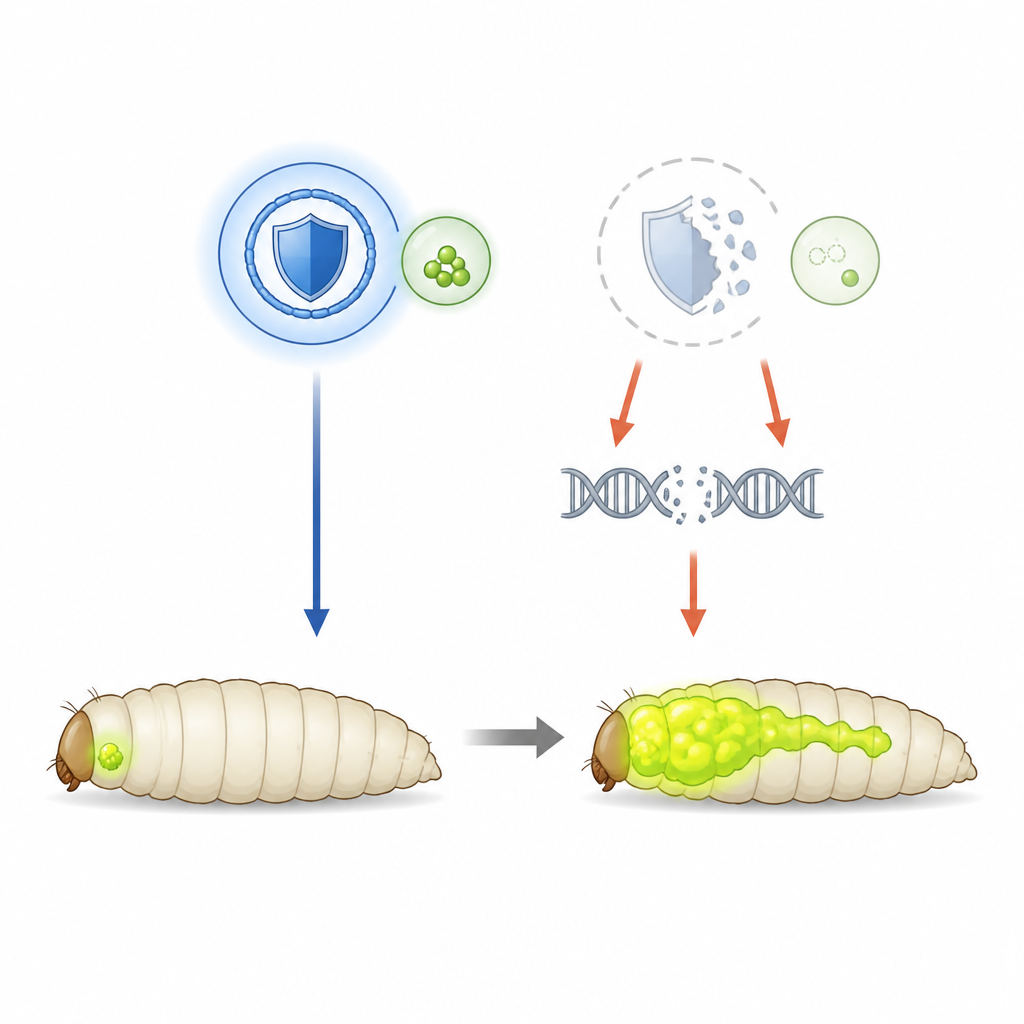
استخدام ذبابتين لمراقبة نمو الأورام
لفك دور SHMT الوقائي، لجأ الفريق إلى ذبابة الفاكهة المُهندسة لتطوّر أورامًا عينية عدوانية يحفزها جين Ras مفرط النشاط وفقدان جين قطبية الخلايا. تتوهج هذه الأورام باللون الأخضر، مما يسمح للعلماء بتتبع حجمها وانتشارها في اليرقة. في هذا الإعداد، تكون مستويات SHMT طبيعية، لذلك كان بإمكان الباحثين تقليل نشاط الإنزيم عمدًا باستخدام التدخّل بالتداخل الريبي. عندما انخفض نشاط SHMT، نمت الأورام الأولية بشكل أكبر وغزت الجهاز العصبي للذبابة بشكل متكرر أكثر، مما يبيّن أن SHMT هنا يعمل كفرامل لتقدّم السرطان بدلاً من أن يكون وقودًا له.
لبنات بناء الحمض النووي، التلف، والإجهاد التأكسدي
يغذي SHMT عادةً مسارًا ينتج ثيميديلات، وهي لبنة أساسية في الحمض النووي. عندما تم كبح SHMT، تعثّرت إمدادات هذه اللبنة. وكانت النتيجة زيادة كبيرة في كسور الحمض النووي مزدوجة السلسلة وكروموسومات متكسّرة بصريًا داخل خلايا الورم، وهي علامات واضحة لعدم استقرار الجينوم. كما أصبحت هذه الخلايا حسّاسة بشكل غير معتاد للأشعة السينية المسببة لتلف الحمض النووي ولأدوية تبطئ نسخ الحمض النووي، وكافحت لإصلاح الكسور بعد حدوثها. في الوقت نفسه، ارتفعت مستويات الجذور الحرة الأكسجينية، الجزيئات المؤذية الحاوية على الأكسجين، بشكل حاد. علاج اليرقات بالثيميديلات أعاد لبنات بناء الحمض النووي وخفض كلًا من تلف الحمض النووي والإجهاد التأكسدي، بينما خفّض مضاد أكسدة، حمض N-أسيتيل سيستئين، الجذور الحرة الأكسجينية وتلف الكروموسومات ونمو الورم. معًا تشير هذه النتائج إلى سلسلة من الأحداث حيث يؤدي نقص لبنات بناء الحمض النووي إلى زيادة الإجهاد التأكسدي، الذي يهاجم الحمض النووي ويساعد الأورام على التقدّم.
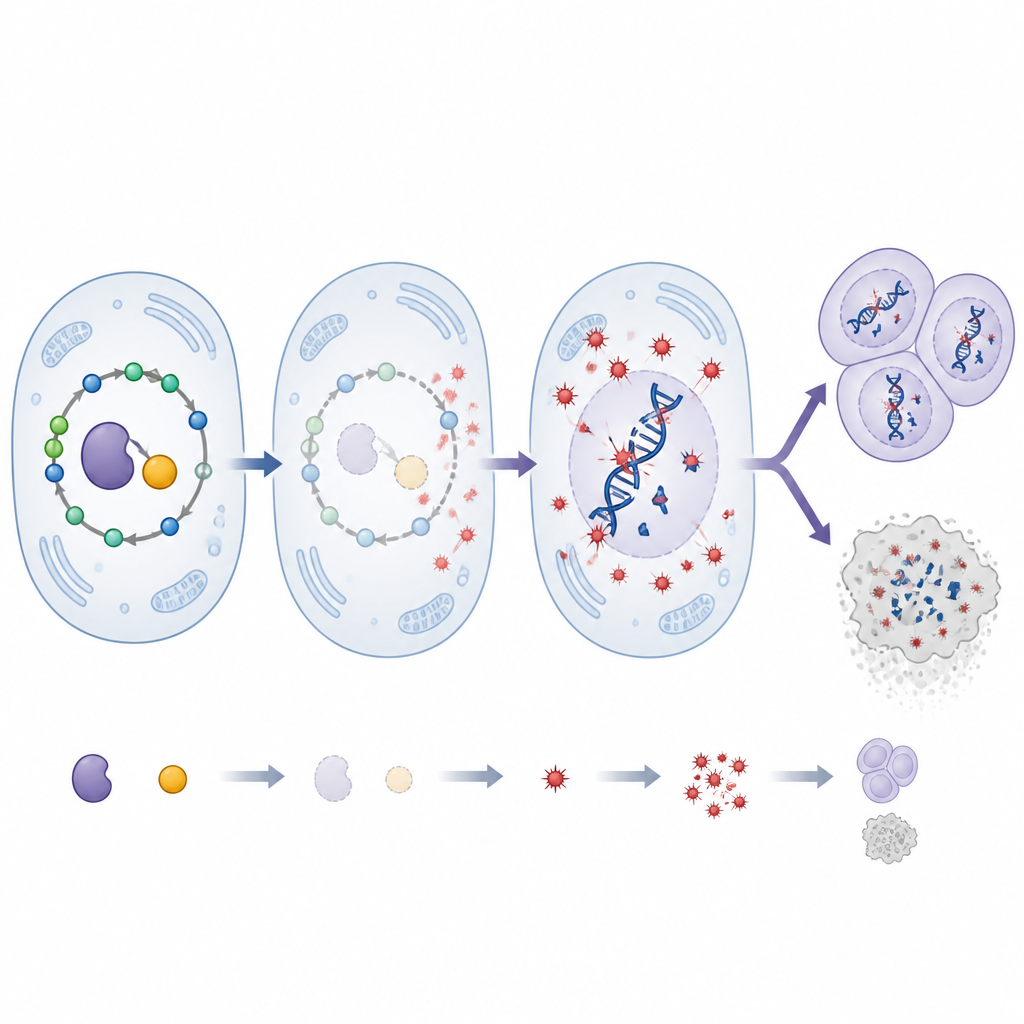
عامل مساعد فيتاميني يغيّر الميزان
يعتمد SHMT على بيريدوكسال 5’-فوسفات، الشكل النشط لفيتامين B6، ليعمل. خفض الباحثون هذا الفيتامين داخل الذباب باستخدام حاجز غذائي ودرسوا كيف يتفاعل ذلك مع تقليل SHMT. أدى خفض SHMT بمفرده إلى تسارع نمو الورم وزيادة تلف الحمض النووي. أما خفض فيتامين B6 بمفرده فكان له تأثيرات أخف. اللافت أن الجمع بين التغيرين تسبب في قفزة دراماتيكية في الإجهاد التأكسدي وتكسّر الحمض النووي، أكثر بكثير من كل ضربة على حدة. ومع ذلك لم ينتج عن ذلك أورامًا أكبر بنسبة متناسبة. بدلًا من ذلك، شغّلت العديد من خلايا الورم إنزيم موت خلوي رئيسي وخضعت للموت المبرمج، مما يشير إلى أن الخلايا المتضررة للغاية كانت تُستبعد. خفضت معالجة بمضاد أكسدة بجرعة عالية مرة أخرى الإجهاد التأكسدي وتلف الحمض النووي وحجم الورم، مؤكدة الدور المركزي للجذور الحرة الأكسجينية في قيادة هذه النتائج.
ماذا يعني ذلك بالنسبة للسرطان والنظام الغذائي
تُظهر هذه الدراسة أنه في حيوان حي، يمكن أن يعمل SHMT كمثبط للورم عبر المساعدة في الحفاظ على استقرار الحمض النووي ومراقبة الإجهاد التأكسدي. عندما ينخفض نشاط SHMT، خصوصًا مع انخفاض فيتامين B6، تتراكم أضرار الحمض النووي في خلايا الورم التي قد تغذّي تقدم السرطان أو، إذا دفعت إلى حدّها، تثير موتها الذاتي. تكشف الدراسة أيضًا عن تفاعل جيني–مغذّي مباشر بين SHMT وفيتامين B6 يشكّل كيفية نمو الأورام. ورغم أن هذه النتائج مستمدة من ذبابة الفاكهة، إلا أنها تعكس أنماطًا مرصودة في بعض سرطانات الإنسان وتقترح أن استهداف SHMT، وعاملها المساعد الفيتاميني، والجذور الحرة الأكسجينية معًا قد يوجّه استراتيجيات مستقبلية للسيطرة على نمو الأورام دون الاعتماد فقط على قتل الخلايا المنقسمة.
الاستشهاد: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
الكلمات المفتاحية: استقلاب السرطان, تلف الحمض النووي, الجذور الحرة الأكسجينية, فيتامين B6, أورام ذبابة الفاكهة