Clear Sky Science · pt
Função supressora de tumor da SHMT em um modelo Drosophila RasV12DlgRNAi: dano ao DNA e interação sinérgica gene-nutriente com PLP
Por que essa história da mosca-das-frutas importa
O câncer frequentemente reconfigura como as células utilizam nutrientes, mas as mesmas moléculas que alimentam tumores às vezes podem contê‑los. Neste estudo, pesquisadores usaram moscas-das-frutas para descobrir como uma única enzima que participa da química ligada a vitaminas dentro das células pode funcionar como um freio ao câncer. Eles mostram que, quando essa enzima falha, o DNA fica instável, os tumores crescem de forma mais agressiva e uma vitamina comum e um antioxidante podem deslocar o equilíbrio entre crescimento tumoral e morte celular.
O pequeno centro de tráfego de carbonos da célula
No interior de nossas células, uma rede conhecida como metabolismo de um-carbono sustenta discretamente a vida ao fornecer blocos de construção para a produção de DNA e grupos químicos que controlam a atividade gênica. No centro dessa rede está uma enzima chamada SHMT, que trabalha em conjunto com a forma ativa da vitamina B6. A SHMT ajuda a converter um aminoácido em outro enquanto transfere pequenas unidades de carbono necessárias para fabricar DNA. Em muitos cânceres humanos, versões dessa enzima são encontradas em níveis elevados e acredita-se que favoreçam o crescimento tumoral. Contudo, em alguns cânceres, baixos níveis de uma forma de SHMT estão associados a piores prognósticos, sugerindo que a enzima também pode atuar como supressora de tumor, dependendo do contexto.
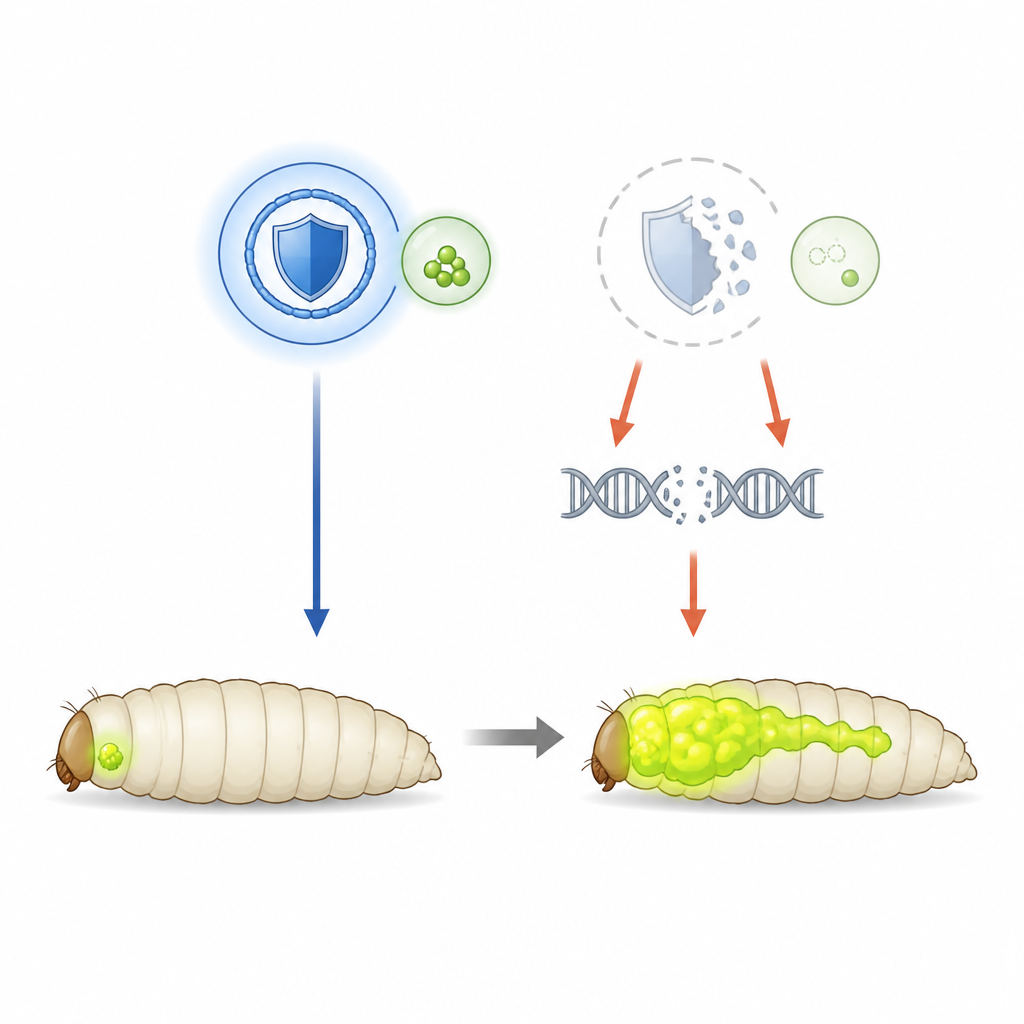
Usando moscas-das-frutas para observar tumores crescerem
Para desvendar o papel protetor da SHMT, a equipe recorreu a moscas-das-frutas geneticamente modificadas para desenvolver tumores oculares agressivos impulsionados por um gene Ras hiperativo e perda de um gene de polaridade celular. Esses tumores brilham em verde, permitindo aos cientistas monitorar seu tamanho e espalhamento na larva. Nesse contexto, os níveis de SHMT são normais, então os pesquisadores puderam diminuir deliberadamente a enzima usando interferência por RNA. Quando a atividade da SHMT foi reduzida, os tumores primários cresceram mais e invadiram o sistema nervoso da mosca com maior frequência, mostrando que, aqui, a SHMT age como um freio à progressão tumoral em vez de como combustível.
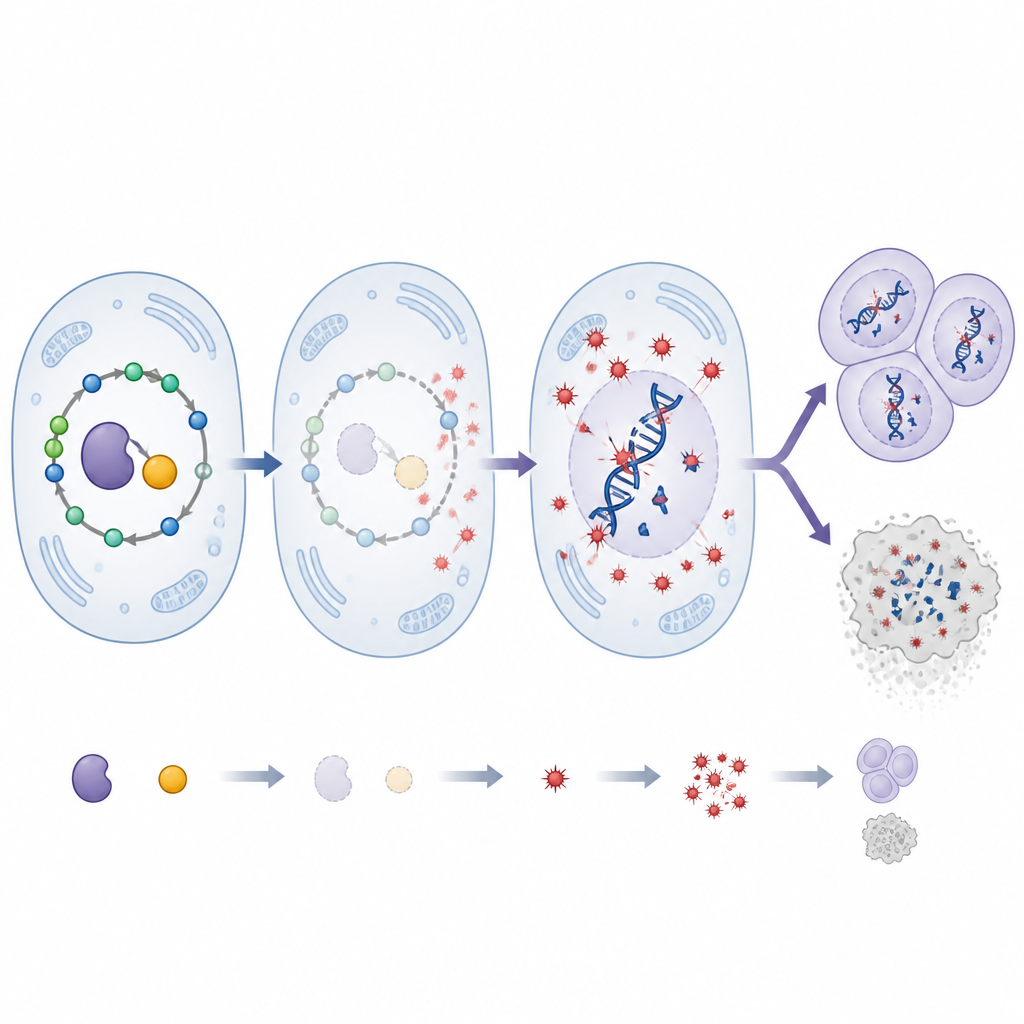
Blocos de construção do DNA, danos e estresse oxidativo
A SHMT normalmente alimenta uma via que produz timidilato, um bloco de construção essencial do DNA. Quando a SHMT foi silenciada, o suprimento desse bloco de construção vacilou. O resultado foi um aumento de quebras de fita dupla no DNA e cromossomos visivelmente fragmentados dentro das células tumorais, sinais claros de instabilidade genômica. Essas células também se tornaram incomumente sensíveis a raios X que danificam o DNA e a drogas que retardam a cópia do DNA, e tiveram dificuldade em reparar quebras uma vez ocorridas. Ao mesmo tempo, os níveis de espécies reativas de oxigênio, moléculas prejudiciais que contêm oxigênio, aumentaram acentuadamente. Tratar as larvas com timidilato restabeleceu os blocos de construção do DNA e reduziu tanto o dano ao DNA quanto o estresse oxidativo, enquanto um antioxidante, N-acetil cisteína, diminuiu as espécies reativas de oxigênio, o dano cromossômico e o crescimento tumoral. Juntos, esses achados apontam para uma cadeia de eventos na qual o fornecimento insuficiente de blocos de construção do DNA aumenta o estresse oxidativo, que então ataca o DNA e ajuda os tumores a avançarem.
Um cofator vitamínico inclina a balança
A SHMT depende do piridoxal 5’-fosfato, a forma ativa da vitamina B6, para funcionar. Os pesquisadores reduziram essa vitamina nas moscas usando um bloqueador dietético e investigaram como isso interagia com a redução da SHMT. Cortar apenas a SHMT acelerou o crescimento tumoral e aumentou o dano ao DNA. Reduzir apenas a vitamina B6 teve efeitos mais leves. Notavelmente, combinar ambas as alterações causou um pico dramático no estresse oxidativo e na fragmentação do DNA, muito maior do que qualquer um dos impactos isolados. Ainda assim, isso não produziu tumores proporcionalmente maiores. Em vez disso, muitas células tumorais ativaram uma enzima chave de morte celular e passaram por apoptose, sugerindo que células extremamente danificadas estavam sendo eliminadas. O tratamento com antioxidante em alta dose novamente reduziu o estresse oxidativo, o dano ao DNA e o tamanho tumoral, evidenciando o papel central das espécies reativas de oxigênio em conduzir esses desfechos.
O que isso significa para câncer e dieta
Este trabalho mostra que, em um animal vivo, a SHMT pode atuar como supressora tumoral ao ajudar a manter a estabilidade do DNA e controlar o estresse oxidativo. Quando a atividade da SHMT cai, especialmente junto com a redução da vitamina B6, as células tumorais acumulam danos ao DNA que podem ou acelerar a progressão do câncer ou, se levados ao extremo, desencadear sua própria morte. O estudo também revela uma interação direta gene–nutriente entre a SHMT e a vitamina B6 que molda como os tumores crescem. Embora esses achados venham de moscas-das-frutas, eles ecoam padrões observados em alguns cânceres humanos e sugerem que mirar simultaneamente na SHMT, em seu cofator vitamínico e nas espécies reativas de oxigênio pode informar estratégias futuras para controlar o crescimento tumoral sem depender exclusivamente de matar células em divisão.
Citação: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Palavras-chave: metabolismo do câncer, danos ao DNA, espécies reativas de oxigênio, vitamina B6, tumores de Drosophila